Clear Sky Science · nl
Quinoline 'turn-on'-sensor voor selectieve detectie van hypochloriet in levende cellen
Een nieuwe manier om een verborgen chemische stof in onze cellen te zien
Onze cellen produceren en breken continu zeer reactieve moleculen af die helpen bij het bestrijden van infecties, maar die zich ook kunnen ophopen en weefsels beschadigen. Een daarvan, hypochloriet, wordt sterk geassocieerd met ontsteking, immuunverdediging en ziekten die samenhangen met oxidatieve stress. Deze studie beschrijft een nieuw ontworpen kleine kleurstofmolecuul dat donker blijft totdat het hypochloriet tegenkomt, en dan aan gaat met een felgroene gloed. Die eenvoudige lichtschakelaar maakt het veel gemakkelijker voor onderzoekers om deze lastige chemische soort in realtime in levende cellen te volgen.
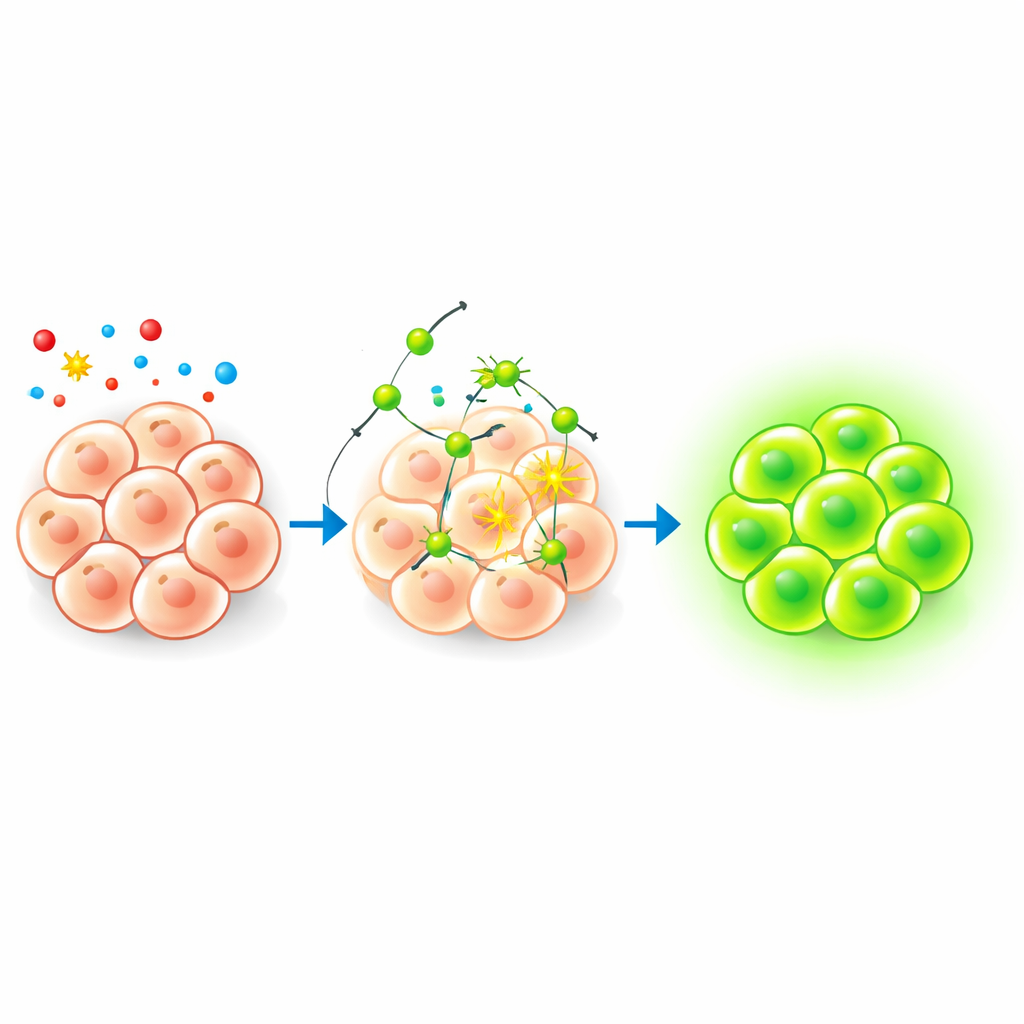
Waarom het volgen van een sterke oxidant belangrijk is
Reactieve zuurstofsoorten zijn chemische bijproducten die ontstaan wanneer onze cellen zuurstof gebruiken. In de juiste concentraties helpen ze witte bloedcellen microben te doden en fungeren ze als signalen die normaal celgedrag sturen. Maar als hun niveaus te hoog worden, vallen ze DNA, eiwitten en vetten aan en dragen ze bij aan aandoeningen variërend van neurodegeneratie tot hartziekten. Hypochloriet is een van die reactieve soorten die door immuuncellen wordt geproduceerd en is binnen weefsels relatief stabiel. Omdat het zowel nuttig als potentieel schadelijk is, willen wetenschappers instrumenten die nauwkeurig kunnen aantonen wanneer, waar en hoeveel hypochloriet in cellen aanwezig is.
Ontwikkeling van een klein, slim lichtschakelaar-molecuul
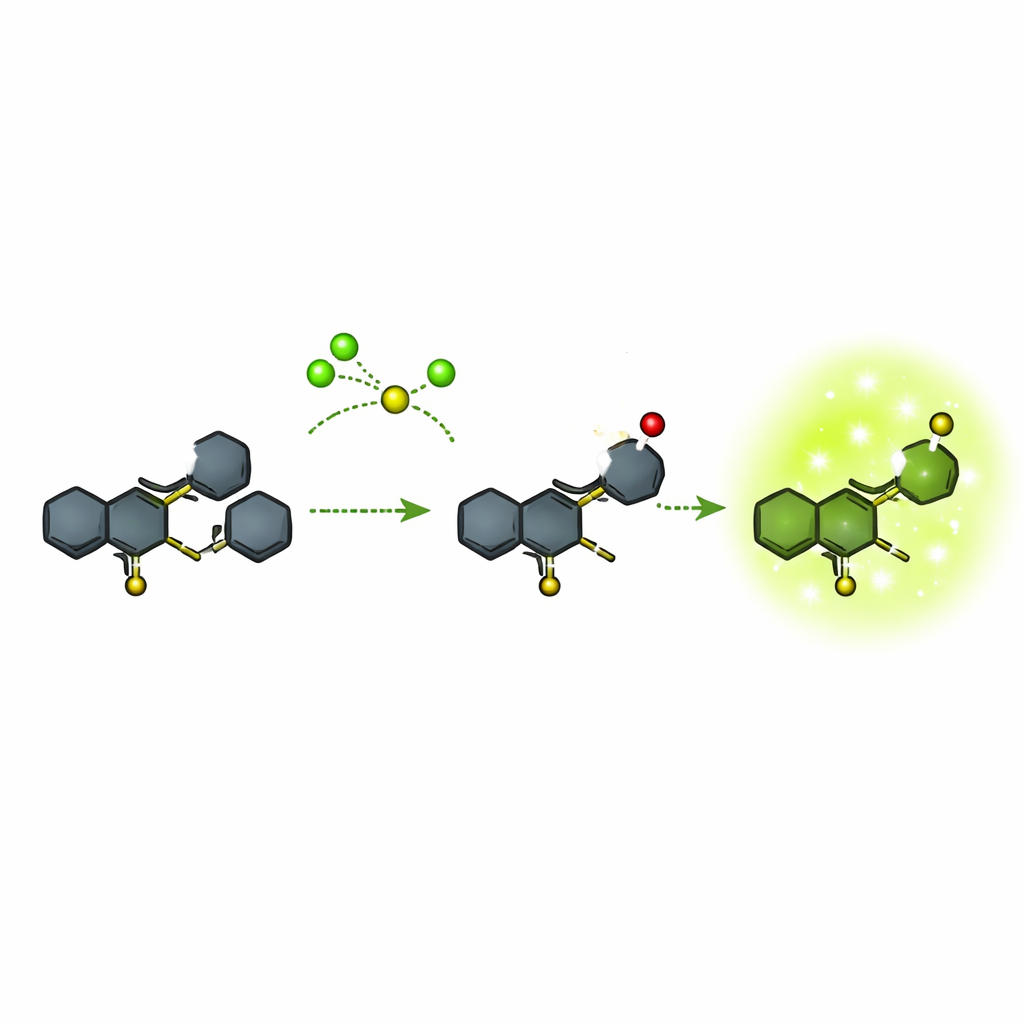
Veel bestaande fluorescente sondes voor hypochloriet zijn vrij omvangrijk of vereisen ingewikkelde kleurveranderingen die precieze metingen bemoeilijken. De auteurs concentreerden zich op een compact chemisch raamwerk gebaseerd op een ringsysteem dat quinoline heet, gekoppeld aan een ander ringsysteem bekend als phenothiazine. Ze bouwden deze structuur in een paar stappen uit commercieel beschikbare beginmaterialen en controleerden elke fase grondig met nucleaire magnetische resonantie, massaspectrometrie en optische metingen. De eindsonde, genoemd verbinding 5, geeft op zichzelf vrijwel geen emissie maar is zodanig ontworpen dat een specifiek zwavelatoom selectief kan worden aangevallen door hypochloriet. Die reactie zet het molecuul om in een nieuwe vorm (verbinding 6) die sterk groen oplicht in het spectrum.
Van donker naar helder in seconden, en alleen voor het juiste doel
Het team testte hoe specifiek en hoe snel de sonde op verschillende chemicaliën reageert. In oplossing vertoonde verbinding 5 vrijwel geen fluorescentie in een breed scala aan oplosmiddelen. Bij blootstelling aan veelvoorkomende ionen, kleine zwavelhoudende moleculen en andere reactieve zuurstofsoorten bleef het donker. Alleen hypochloriet veroorzaakte een sterke, scherpe groene emissie rond 523 nanometer, en de helderheid nam toe met de hypochlorietconcentratie binnen een bruikbaar bereik. De reactie was snel: meetbaar licht verscheen binnen ongeveer 10 seconden en bleef minutenlang toenemen. Bij zeer hoge hypochlorietniveaus kon de sonde nog een stap verder geoxideerd worden tot een overgeoxiderde vorm (een sulfone) die minder fel was, maar dit trad op buiten het belangrijkste werkbereik. Over het geheel genomen lag de detectiegrens zeer laag, ruim onder één micromolair, en het signaal was intens genoeg om met het blote oog waarneembaar te zijn.
Hypochloriet in levende cellen volgen
Om te beoordelen of deze chemie in een biologische omgeving werkte, testten de onderzoekers de sonde in vers geïsoleerde muisbeenmergcellen. Bij een lage sondedosis die de cellen niet schaadde, gebruikten ze flowcytometrie en fluorescentiemicroscopie om het gedrag te volgen. Cellen die alleen met de sonde werden behandeld toonden slechts een lichte toename van groen licht, wat suggereert dat normale interne hypochlorietniveaus laag maar detecteerbaar zijn. Toen dezelfde cellen vervolgens aan oplopende hoeveelheden toegevoegd hypochloriet werden blootgesteld, lichtte een groot deel van de cellen fel op, waarbij het signaal met de dosis mee toenam. Vervolgtesten lieten zien dat het oplichtende product stabiel was onder continue belichting zowel in oplossing als in cellen, en dat de optische eigenschappen bijzonder gunstig waren in waterige, biologisch relevante omstandigheden.
Wat dit betekent voor het bestuderen van gezondheid en ziekte
Samengevat introduceren deze resultaten een compacte, snelwerkende en selectieve "turn-on"-sonde voor hypochloriet die onder milde condities functioneert en betrouwbaar werkt in levende cellen. In plaats van te vertrouwen op subtiele kleurverschuivingen of volumineuze kleurstofstructuren, gebruikt dit ontwerp een eenvoudige schakeling van donker naar helder groen licht die direct gekoppeld is aan een specifieke chemische verandering op één atoom in het molecuul. Omdat de sonde cellen kan markeren die verhoogde hypochlorietwaarden vertonen, biedt het een praktisch instrument om te onderzoeken hoe oxidatieve stress ontstaat tijdens infectie, ontsteking en andere ziektebeelden, en kan het de ontwikkeling van verfijndere sensoren voor andere reactieve chemicaliën in de toekomst begeleiden.
Bronvermelding: Olubiyo, F.F., Klu, S.Y.S., Burgess, R.J. et al. Turn-on quinoline probe for selective sensing of hypochlorite in live cells. Sci Rep 16, 10715 (2026). https://doi.org/10.1038/s41598-026-45327-1
Trefwoorden: detectie van hypochloriet, fluorescente sondes, reactieve zuurstofsoorten, celbeeldvorming, oxidatieve stress