Clear Sky Science · it
Sonda a ‘‘accensione’’ a chinolina per il rilevamento selettivo dell′ipoclorito nelle cellule vive
Un nuovo modo di vedere una sostanza chimica nascosta nelle nostre cellule
Le nostre cellule producono e degradano costantemente molecole altamente reattive che aiutano a combattere le infezioni ma possono anche danneggiare i tessuti se si accumulano. Una di queste, l′ipoclorito, è strettamente legata all′infiammazione, alla difesa immunitaria e a malattie associate allo stress ossidativo. Questo studio descrive una piccola molecola colorante progettata per rimanere spenta fino al contatto con l′ipoclorito, quando si attiva emettendo un brillante bagliore verde. Questo semplice interruttore luminoso rende molto più facile per i ricercatori osservare questa sostanza elusiva in tempo reale all′interno di cellule vive.
Perché è importante tracciare un ossidante aggressivo
Le specie reattive dell′ossigeno sono sottoprodotti chimici formati quando le nostre cellule usano l′ossigeno. A livelli appropriati aiutano i globuli bianchi a uccidere i microrganismi e svolgono funzione di segnali che guidano il comportamento cellulare normale. Ma quando i loro livelli diventano troppo elevati, attaccano DNA, proteine e lipidi, contribuendo a condizioni che vanno dalla neurodegenerazione alle malattie cardiache. L′ipoclorito è una di queste specie reattive prodotta dalle cellule immunitarie, ed è insolitamente stabile nei tessuti viventi. Poiché può essere utile ma anche dannoso, gli scienziati cercano strumenti che rivelino con accuratezza quando, dove e in che quantità l′ipoclorito è presente nelle cellule.
Progettare una piccola molecola interruttore intelligente
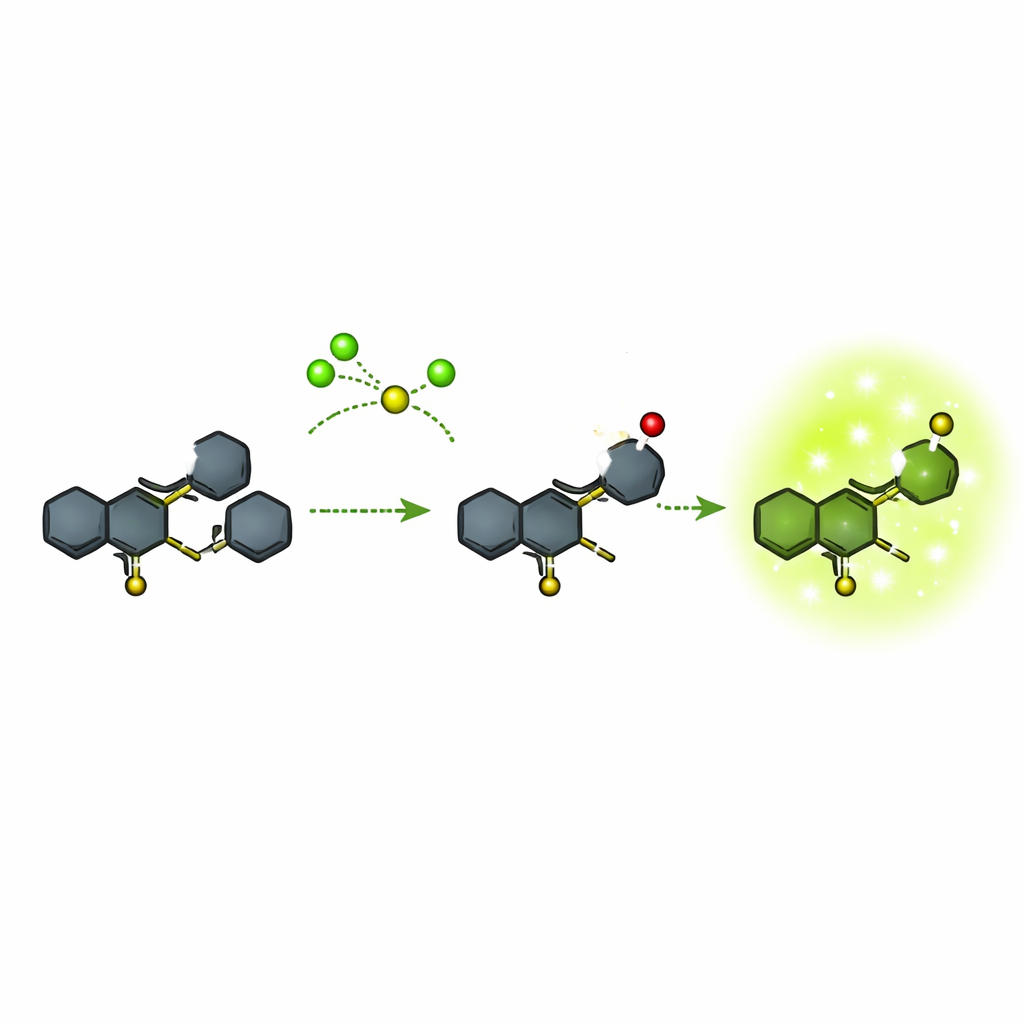
Molte sonde fluorescenti esistenti per l′ipoclorito sono relativamente ingombranti o richiedono cambiamenti cromatici complessi che rendono difficili misure precise. Gli autori si sono concentrati su un cuore chimico compatto basato su un sistema ad anello chiamato chinolina, connesso a un altro sistema ad anello noto come fenotiazina. Hanno costruito questa struttura in pochi passaggi a partire da materiali di partenza commercialmente disponibili, verificando rigorosamente ogni fase con risonanza magnetica nucleare, spettrometria di massa e misure ottiche. La sonda finale, chiamata composto 5, è quasi non luminosa da sola ma è progettata in modo che un particolare atomo di zolfo possa essere attaccato selettivamente dall′ipoclorito. Quella reazione trasforma la molecola in una nuova forma (composto 6) che emette fortemente nella regione verde dello spettro.
Da spento a brillante in pochi secondi, e solo per il bersaglio giusto
Il gruppo ha testato quanto specificamente e quanto rapidamente la sonda risponde a diversi reagenti. In soluzione, il composto 5 non mostrava praticamente fluorescenza in un ampio intervallo di solventi. Esposto a molti ioni comuni, piccoli composti contenenti zolfo e altre specie reattive dell′ossigeno, rimaneva spento. Solo l′ipoclorito provocava una forte e netta emissione verde intorno a 523 nanometri, e l′intensità aumentava in funzione della concentrazione di ipoclorito in un intervallo utile. La reazione era rapida: la luce misurabile compariva in circa 10 secondi e continuava a salire nell′arco di alcuni minuti. A livelli molto alti di ipoclorito, la sonda poteva essere ulteriormente ossidata a uno stadio successivo (un sulfossido/sulfone) meno luminoso, ma ciò avveniva al di fuori dell′intervallo operativo principale. Nel complesso, il limite di rilevazione era estremamente basso, ben al di sotto di un micromolare, e il segnale era abbastanza intenso da essere visibile a occhio nudo.
Osservare l′ipoclorito all′interno di cellule vive
Per verificare se questa chimica funzionasse in un contesto biologico, i ricercatori hanno testato la sonda in cellule del midollo osseo di topo appena isolate. A una bassa dose della sonda che non danneggiava le cellule, hanno usato citometria a flusso e microscopia a fluorescenza per monitorarne il comportamento. Le cellule trattate solo con la sonda mostravano solo un lieve aumento della luce verde, suggerendo che i livelli interni normali di ipoclorito sono bassi ma rilevabili. Quando le stesse cellule sono state quindi esposte a quantità crescenti di ipoclorito aggiunto, una grande frazione di cellule si è illuminata intensamente, con il segnale proporzionale alla dose. Test successivi hanno mostrato che il prodotto luminiscente era stabile sotto illuminazione continua sia in soluzione sia nelle cellule, e che le sue proprietà ottiche erano particolarmente favorevoli in condizioni acquose e biologicamente rilevanti.
Cosa significa per lo studio della salute e della malattia
Nel loro insieme, questi risultati presentano una sonda «turn-on» compatta, rapida e selettiva per l′ipoclorito che opera in condizioni miti e funziona in modo affidabile in cellule vive. Piuttosto che fare affidamento su sottili spostamenti di colore o su strutture di coloranti ingombranti, questo progetto utilizza un semplice passaggio da spento a verde brillante legato direttamente a un cambiamento chimico specifico su un singolo atomo della molecola. Poiché la sonda può evidenziare le cellule che presentano ipoclorito elevato, offre uno strumento pratico per esplorare come lo stress ossidativo si sviluppa durante infezioni, infiammazioni e altri stati patologici, e potrebbe guidare lo sviluppo di sensori più raffinati per altre specie reattive in futuro.
Citazione: Olubiyo, F.F., Klu, S.Y.S., Burgess, R.J. et al. Turn-on quinoline probe for selective sensing of hypochlorite in live cells. Sci Rep 16, 10715 (2026). https://doi.org/10.1038/s41598-026-45327-1
Parole chiave: rilevamento ipoclorito, sonde fluorescenti, specie reattive dell′ossigeno, imaging cellulare, stress ossidativo