Clear Sky Science · ru
Атомистические и электронные представления о интеркаляции Ca2+ и Li+ в TiS2: подход первого принципа с электрохимической валидацией
Почему важна новая химия аккумуляторов
От смартфонов до электромобилей современные перезаряжаемые батареи в основном основаны на литии. Однако литий относительно редок и дорог, а улучшать существующие технологии становится все труднее. В этой работе рассматривается альтернатива: аккумуляторы, в которых транспортируют ионы кальция вместо литиевых. Снижая масштаб до атомной и электронной структуры классического материала для батарей — дисульфида титана (TiS2), — исследователи задают простой, но важный вопрос: может ли кальций, неся двойной заряд на ион, легко перемещаться в TiS2 и эффективно хранить энергию, не разрушая кристаллическую решетку?
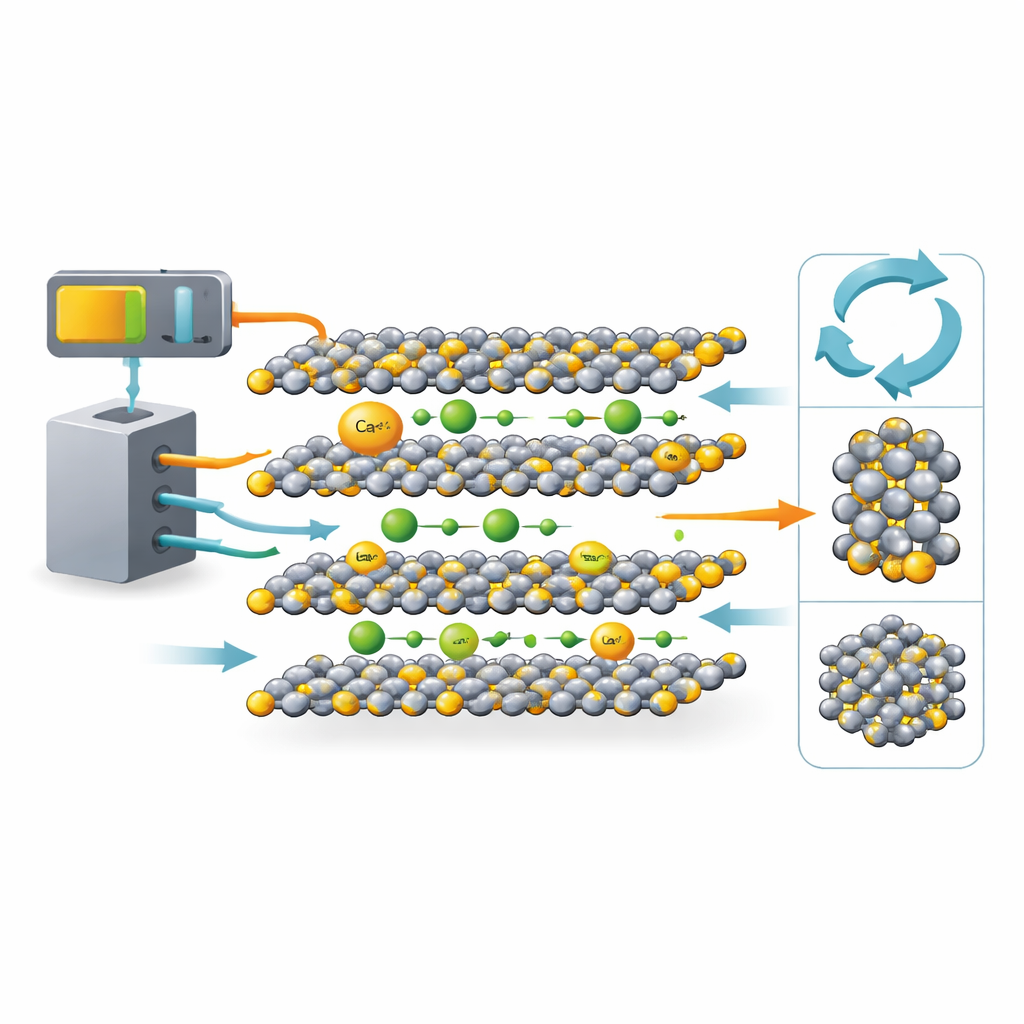
Знакомый материал аккумуляторов — в новом свете
TiS2 имеет длительную историю исследований в области литий-ионных систем. Его кристаллическая структура состоит из плоских слоев, уложенных как листы бумаги, с открытыми пространствами между ними, куда ионы могут встраиваться и выходить. Такая архитектура сделала TiS2 классическим хостом для литиевых ионов. Новая идея этой работы — прямое сравнение лития и кальция в одной и той же матрице TiS2. Ионы кальция крупнее и несут двойной заряд, поэтому многие ученые опасались, что они будут двигаться медленно или повредят решетку хоста. Выбрав хорошо изученный TiS2, авторы смогли отделить эффекты, вызванные самими ионами, от тех, что обусловлены хост-структурой.
Атомы и электроны — вместе
Исследователи комбинировали продвинутые компьютерные моделирования с реальными электрохимическими испытаниями. С помощью расчетов первого принципа они оптимизировали атомные положения в TiS2 при заполнении либо литием, либо кальцием и отслеживали расширение слоев. Затем они рассчитали, насколько легко каждый ион перепрыгивает с одного положения на другое внутри материала, и изучили, как перераспределяются электроны по мере встраивания ионов. Второй блок расчетов сосредоточен на локальных химических связях — насколько сильно ионы взаимодействуют с ближайшими атомами серы и как реагирует титан-серная сеть. Параллельно авторы собрали реальные монеточные элементы с электродами из TiS2 и электролитами, несущими либо литиевые, либо кальциевые ионы, измеряя емкость, напряжение, скорости диффузии ионов и стабильность при циклировании.
Кальций раскрывает каналы, но сохраняет каркас
Атомная картина, которая возникает, парадоксальна. Когда кальций входит в TiS2, он больше раздвигает слои, чем литий, расширяя каналы для движения ионов. В то же время кальций слабее взаимодействует с атомами серы, чем литий, то есть ионы менее «привязаны» и могут перемещаться свободнее. Тем не менее титан-серные связи, удерживающие слои вместе, в случае кальция фактически слегка усиливаются, так что общая структура остается прочной. Расчеты показывают, что энергетический барьер для диффузии ионов кальция ниже, чем для литиевых, а электронные состояния вблизи рабочей энергии материала становятся более плотными и связными, что благоприятствует электронной проводимости.
Что это значит для реальных батарей
Электрохимические тесты подтверждают теоретические предсказания. В элементах на основе TiS2 интеркаляция кальция дает начальную разрядную емкость около 201 мА·ч на грамм — заметно выше примерно 134 мА·ч на грамм, получаемых при работе с литием при схожих условиях. Кальций также показывает более быструю диффузию ионов, судя по циклической вольтамперометрии, и лучшую скоростную характеристику: при увеличении и последующем снижении токов заряд-разряд элементы с кальцием сохраняют более 96% начальной емкости против ≈89% для литиевых. В течение 100 циклов обе системы постепенно теряют емкость, но кальций поддерживает слегка более высокие значения, сохраняя процесс заряд-разряд высокообратимым.
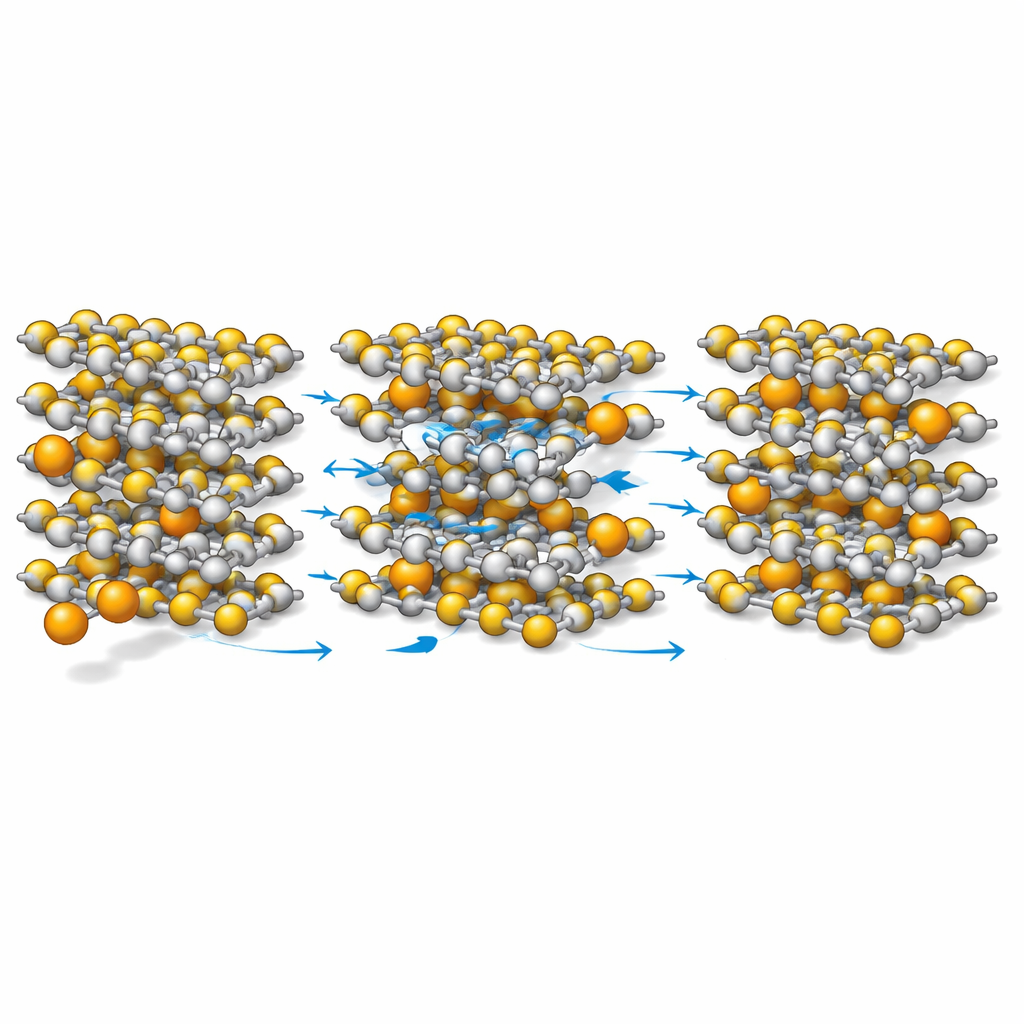
Баланс между энергией, стабильностью и практичностью
В исследовании выявлен один компромисс: среднее напряжение кальция в TiS2 ниже, чем у лития в том же хосте, то есть каждый зарядовый эквивалент дает несколько меньше энергии. Однако поскольку каждый ион кальция переносит два электрона вместо одного, и благодаря тому, что структура остается стабильной и ионы движутся быстро, общее энергохранилище остается конкурентоспособным. Еще важнее с точки зрения практики — кальций распространен, недорог и экологически безопасен. Показав в микроскопических деталях, как кальций может легко перемещаться через TiS2 при сохранении целостности решетки хоста, эта работа формулирует правила проектирования для следующего поколения мультивалентных батарей: сохранять прочную матрицу хоста, обеспечивать достаточно слабое связывание ионов для быстрого движения и настраивать электронную структуру для плавного протекания заряда. Эти принципы теперь можно применять к другим слоистым материалам в поисках практических кальциевых аккумуляторов.
Цитирование: Yang, S., Lee, S., Nogales, P.M. et al. Atomistic and electronic insights into Ca2+ and Li+ intercalation in TiS2: a first-principles approach supported by electrochemical validation. Sci Rep 16, 14605 (2026). https://doi.org/10.1038/s41598-026-42087-w
Ключевые слова: кальциевые аккумуляторы, дисульфид титана, мультивалентные ионы, материалы для аккумуляторов, диффузия ионов