Clear Sky Science · it
Approfondimenti atomistici ed elettronici sull'intercalazione di Ca2+ e Li+ in TiS2: un approccio first-principles supportato da validazione elettrochimica
Perché una nuova chimica delle batterie conta
Dagli smartphone alle auto elettriche, le batterie ricaricabili odierne si basano in gran parte sul litio. Ma il litio è relativamente raro e costoso, e portare la tecnologia attuale a prestazioni superiori diventa sempre più difficile. Questo studio esplora un’alternativa: batterie che trasportano ioni calcio invece di ioni litio. Analizzando la struttura atomica ed elettronica di un materiale classico per batterie, il disolfuro di titanio (TiS2), i ricercatori pongono una domanda semplice ma di grande portata: il calcio, che porta il doppio di carica per ione, può muoversi agevolmente attraverso TiS2 e immagazzinare energia in modo efficiente senza danneggiare il materiale?
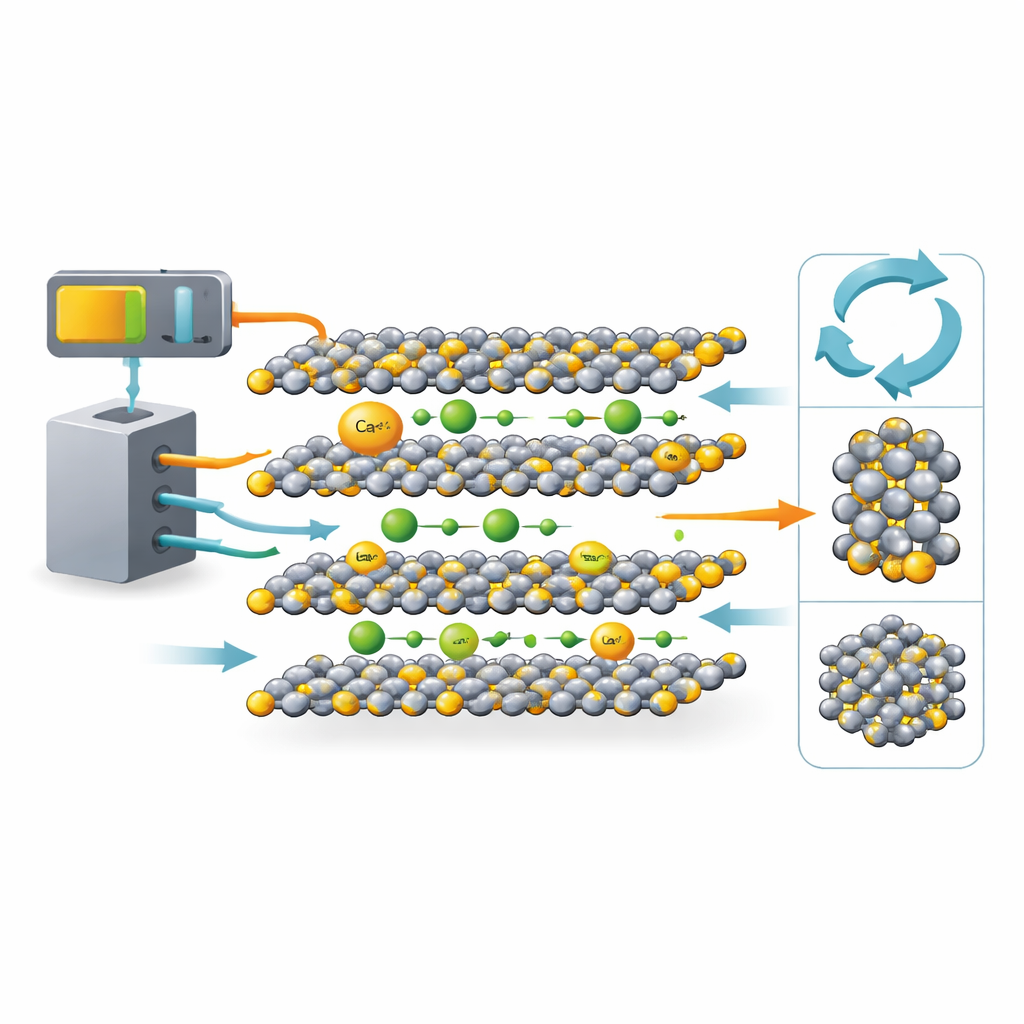
Un materiale per batterie familiare sotto una nuova luce
TiS2 ha una lunga storia nella ricerca sulle batterie al litio. La sua struttura cristallina è costituita da strati piatti impilati come fogli di carta, con spazi aperti tra di essi dove gli ioni possono inserirsi e uscire. Questa architettura ha reso TiS2 un ospite canonico per gli ioni litio. La novità di questo lavoro è il confronto diretto fra litio e calcio all'interno dello stesso reticolo di TiS2, affiancati. Gli ioni calcio sono più grandi e portano il doppio di carica, perciò molti scienziati hanno temuto che si muovessero lentamente o danneggiassero il reticolo ospite. Scegliendo TiS2, un materiale ben compreso, il team può distinguere quali comportamenti dipendono dagli ioni e quali dal materiale ospite.
Osservare atomi ed elettroni insieme
I ricercatori hanno combinato simulazioni computazionali avanzate con test sperimentali su batterie reali. Utilizzando calcoli first-principles, hanno ottimizzato le posizioni atomiche in TiS2 quando è caricato con litio o con calcio e hanno monitorato l’espansione degli strati. Hanno quindi calcolato quanto facilmente ogni ione salta da un sito all'altro all'interno del materiale e hanno esaminato come gli elettroni si riorganizzano durante l'inserimento ionico. Un secondo insieme di calcoli si è concentrato sui legami chimici locali: quanto forte è l'interazione degli ioni con gli atomi di zolfo vicini e come risponde il reticolo titanio–zolfo. Parallelamente, hanno assemblato celle a bottone reali con elettrodi di TiS2 ed elettroliti contenenti ioni litio o calcio, misurando capacità, tensione, velocità di diffusione ionica e stabilità durante i cicli.
Il calcio apre i canali ma preserva l'impalcatura
L’immagine su scala atomica che emerge è controintuitiva. Quando il calcio entra in TiS2, spinge gli strati più lontano rispetto al litio, allargando i canali per il moto ionico. Allo stesso tempo, il calcio interagisce in modo più debole con gli atomi di zolfo rispetto al litio, il che significa che gli ioni sono meno «ancorati» e possono muoversi con maggiore libertà. Tuttavia i legami titanio–zolfo che tengono insieme gli strati diventano in realtà leggermente più forti nel caso del calcio, quindi l'impalcatura complessiva resta robusta. I calcoli mostrano che la barriera energetica per la diffusione degli ioni calcio è inferiore a quella per gli ioni litio, e gli stati elettronici vicini al livello energetico operativo del materiale diventano più densi e più connessi, favorendo la conduzione elettronica.
Cosa significa per le batterie reali
I test elettrochimici rispecchiano le previsioni teoriche. Nelle celle a base di TiS2, l'intercalazione di calcio fornisce una capacità al primo scarico di circa 201 mAh per grammo—notevolmente superiore ai circa 134 mAh per grammo osservati con il litio in condizioni simili. Il calcio mostra anche una diffusione ionica più rapida, come suggerito dalla voltammetria ciclica, e migliori prestazioni a diverso regime di corrente: quando la corrente di carica–scarica viene aumentata e poi riportata ai livelli iniziali, le celle al calcio mantengono oltre il 96% della capacità originale, rispetto a circa l'89% per le celle al litio. Per oltre 100 cicli entrambe le chimiche perdono gradualmente capacità, ma il calcio mantiene valori leggermente più elevati pur mantenendo il processo carica–scarica altamente reversibile.
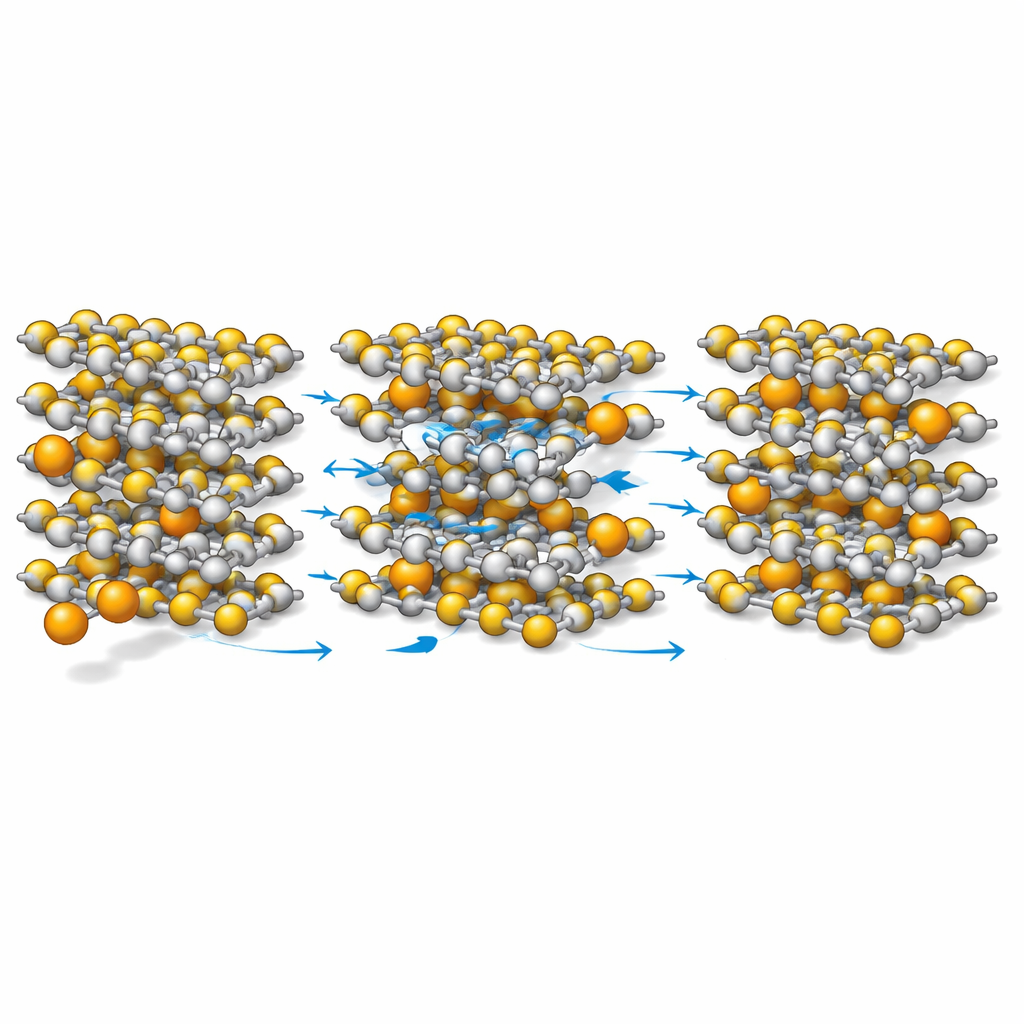
Bilanciare energia, stabilità e praticità
Lo studio rileva un compromesso: la tensione media del calcio in TiS2 è inferiore a quella del litio nello stesso ospite, il che significa che ogni unità di carica fornisce un po’ meno energia. Tuttavia, poiché ogni ione calcio trasferisce due elettroni invece di uno, e perché la struttura rimane stabile e gli ioni si muovono rapidamente, l’immagazzinamento energetico complessivo resta competitivo. Più importante per le tecnologie future, il calcio è abbondante, a basso costo e benigno per l'ambiente. Mostrando in dettaglio microscopico come il calcio possa muoversi facilmente attraverso TiS2 mentre il reticolo ospite resta intatto, questo lavoro delinea regole di progettazione per le batterie multivalenti di nuova generazione: mantenere il framework ospite robusto, permettere agli ioni di legarsi lo stretto necessario per muoversi velocemente e sintonizzare la struttura elettronica in modo che la carica fluisca agevolmente. Questi principi possono ora essere applicati ad altri materiali stratificati nella ricerca di batterie pratiche a ioni di calcio.
Citazione: Yang, S., Lee, S., Nogales, P.M. et al. Atomistic and electronic insights into Ca2+ and Li+ intercalation in TiS2: a first-principles approach supported by electrochemical validation. Sci Rep 16, 14605 (2026). https://doi.org/10.1038/s41598-026-42087-w
Parole chiave: batterie a ioni di calcio, disolfuro di titanio, ioni multivalenti, materiali per batterie, diffusione ionica