Clear Sky Science · ar
رؤى ذرية وإلكترونية في تداخل Ca2+ و Li+ داخل TiS2: نهج أولي مدعوم بالتحقق الكهروكيميائي
لماذا تهم كيمياء البطاريات الجديدة
من الهواتف الذكية إلى السيارات الكهربائية، تعتمد البطاريات القابلة لإعادة الشحن اليوم بدرجة كبيرة على الليثيوم. لكن الليثيوم نادر نسبياً ومكلف، وإخراج أداء أعلى من التقنيات الحالية يزداد صعوبة. يستكشف هذا البحث بديلاً: بطاريات تنقل أيونات الكالسيوم بدلاً من أيونات الليثيوم. من خلال التكبير إلى بنية ذرية وإلكترونية لمادة بطارية كلاسيكية تسمى ثنائى كبريتيد التيتانيوم (TiS2)، يطرح الباحثون سؤالاً بسيطاً ذو تداعيات كبيرة: هل يمكن للكالسيوم، الذي يحمل ضعف الشحنة لكل أيون، أن يتحرك بسهولة داخل TiS2 ويخزن الطاقة بكفاءة دون أن يتلف المادة المضيفة؟
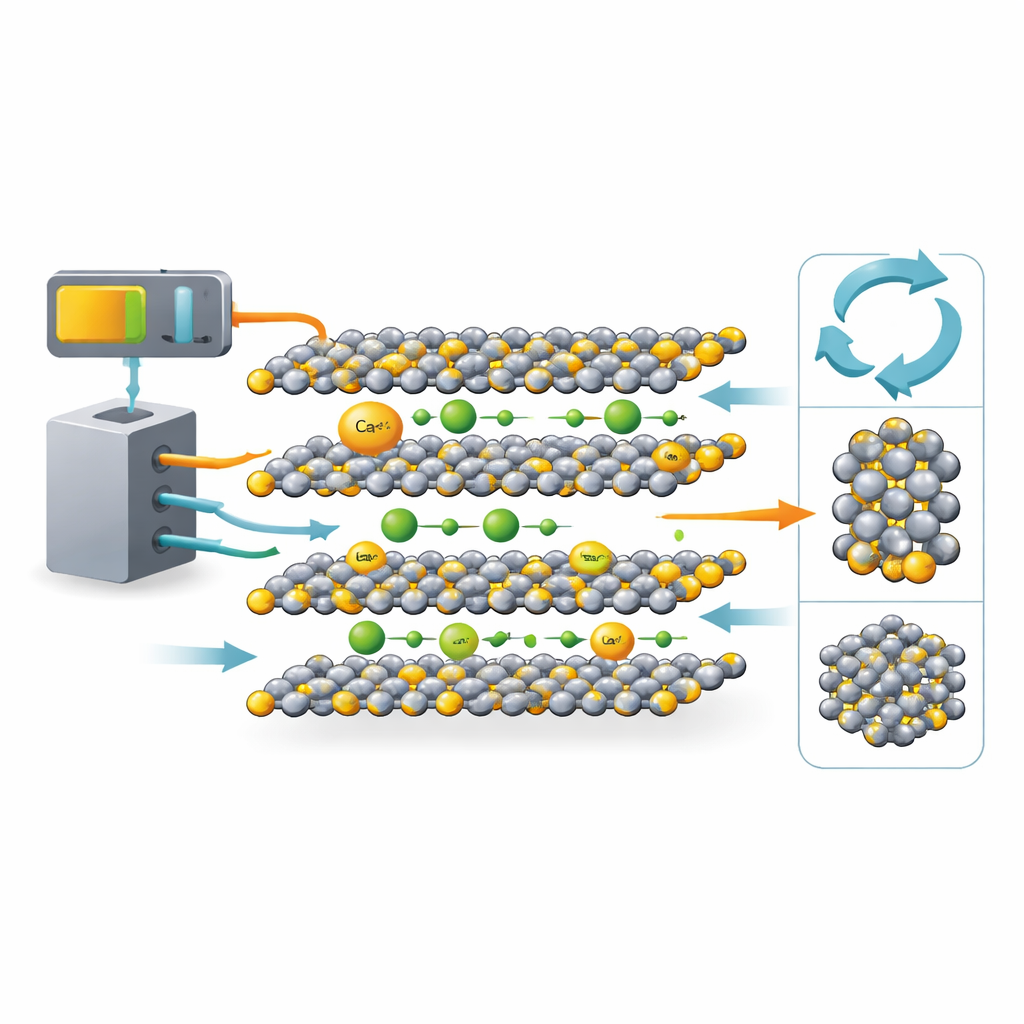
مادة بطارية مألوفة في ضوء جديد
لـ TiS2 تاريخ طويل في أبحاث بطاريات الليثيوم. بنيته البلورية تتكون من طبقات مسطحة مكدسة مثل أوراق الورق، مع فراغات بينها حيث يمكن للأيونات الانزلاق للداخل والخارج. جعلت هذه البنية منه مضيفاً نموذجياً لأيونات الليثيوم. التحول في هذا العمل هو مقارنة الليثيوم والكالسيوم داخل نفس هيكل TiS2، جنباً إلى جنب. أيونات الكالسيوم أكبر وتحمل ضعف الشحنة، لذا قلق العديد من العلماء من أنها قد تتحرك ببطء أو تخلّ بالشبكة المضيفة. باختيار TiS2، وهي مادة مفهومة جيداً، يمكن للفريق أن يفرّق أي السلوكيات ناتجة عن الأيونات نفسها وأيها ناتج عن المضيف.
النظر إلى الذرات والإلكترونات معاً
جمع الباحثون بين محاكيات حاسوبية متقدمة وتجارب بطارية فعلية. باستخدام حسابات أولية، أمّنوا المواضع الذرية في TiS2 عندما تمتلئ إما بالليثيوم أو بالكالسيوم وتتبّعوا كيف تتوسع الطبقات. ثم حسبوا مدى سهولة تنقل كل أيون من موقع إلى آخر داخل المادة وفحصوا كيف تعيد الإلكترونات ترتيب نفسها عندما تتحرك الأيونات إلى الداخل. ركّزت مجموعة ثانية من الحسابات على الروابط الكيميائية المحلية — مدى قوة تفاعل الأيونات مع ذرات الكبريت القريبة وكيف يستجيب إطار التيتانيوم–الكبريت. بالتوازي، بنوا خلايا عمل فعلية من نوع coin باستخدام أقطاب TiS2 وإلكتروليتات تحمل إما أيونات الليثيوم أو الكالسيوم، وقاسوا السعة والجهد ومعدلات انتشار الأيونات وثبات الدورة.
يفتح الكالسيوم القنوات ويحافظ على الإطار
الصورة على المستوى الذري التي تبرز تبدو غير بديهية. عندما يدخل الكالسيوم إلى TiS2، يدفع الطبقات بعيداً أكثر مما يفعل الليثيوم، موسعاً القنوات لحركة الأيونات. في الوقت نفسه، يتفاعل الكالسيوم أضعف مع ذرات الكبريت مقارنة بالليثيوم، ما يعني أن الأيونات أقل «تثبيتاً» ويمكنها أن تتحرك بحرية أكبر. ومع ذلك، تصبح روابط التيتانيوم–الكبريت التي تمسك الطبقات معاً أقوى قليلاً في حالة الكالسيوم، لذلك يظل الإطار الإجمالي متيناً. تُظهر الحسابات أن حاجز الطاقة لانتشار أيونات الكالسيوم أقل من الليثيوم، وتصبح الحالات الإلكترونية بالقرب من مستوى طاقة تشغيل المادة أكثر كثافة وترابطاً، مما يفضّل التوصيل الإلكتروني.
ماذا يعني هذا للبطاريات الحقيقية
التجارب الكهروكيميائية تتناغم مع التنبؤات النظرية. في خلايا تعتمد على TiS2، يعطي تداخل الكالسيوم سعة تفريغ أولية تقارب 201 ملي أمبير ساعة لكل غرام — أعلى بشكل ملحوظ من نحو 134 ملي أمبير ساعة لكل غرام المرصودة مع الليثيوم تحت ظروف مماثلة. يظهر الكالسيوم أيضاً انتشار أيونات أسرع كما يستدل من القياسات الدورانية (cyclic voltammetry)، وأداءً أفضل عند معدلات عالية: عندما تُزاد ثم تُخفض شدة تيار الشحن–التفريغ، تحتفظ خلايا الكالسيوم بأكثر من 96% من سعتها الأصلية، مقارنة بنحو 89% لخلايا الليثيوم. على مدى 100 دورة، تفقد كلتا الكيميائيتين السعة تدريجياً، لكن الكالسيوم يحافظ على قيم أعلى قليلاً مع بقاء عملية الشحن–التفريغ قابلة للعكس بدرجة كبيرة.
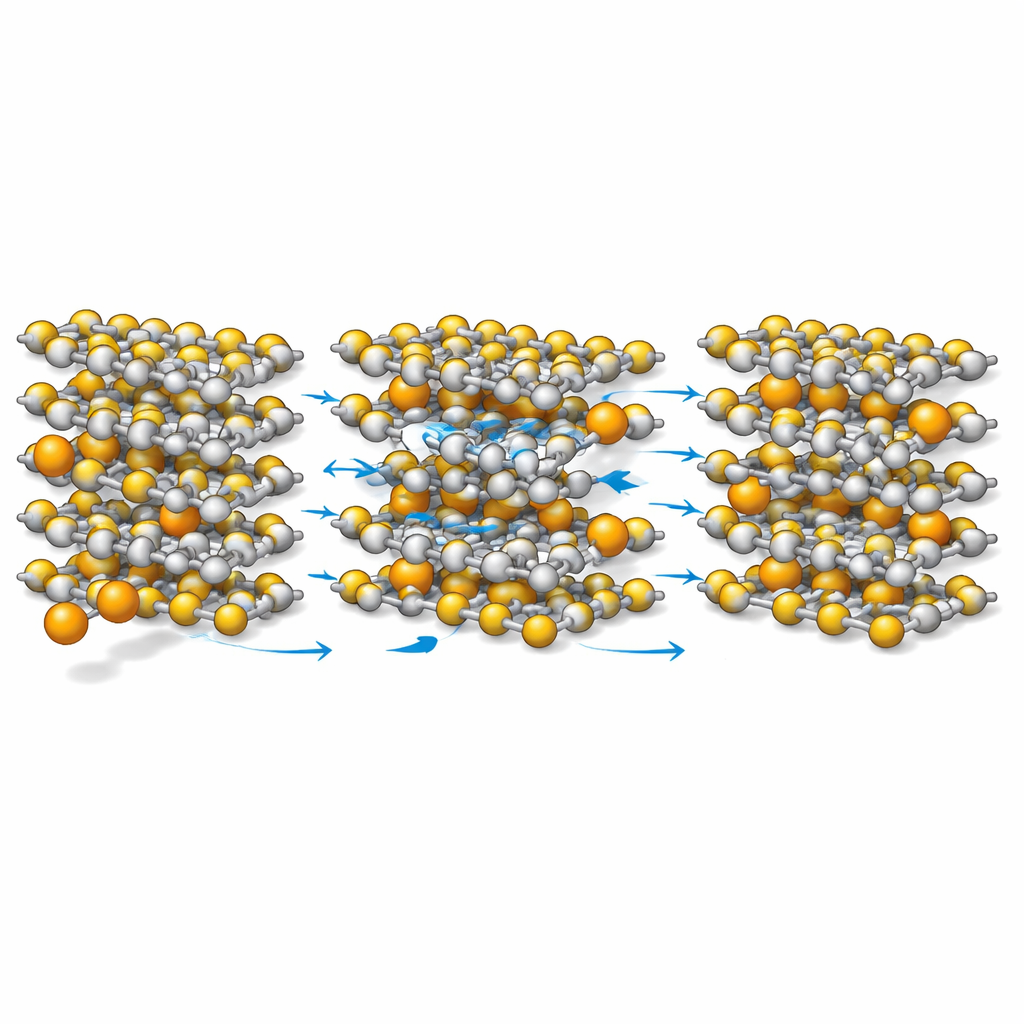
موازنة الطاقة، الاستقرار والعملية
تجد الدراسة تبادلاً واحداً: الجهد المتوسط للكالسيوم في TiS2 أقل من جهد الليثيوم في نفس المضيف، ما يعني أن كل وحدة شحنة تعطي طاقة أقل قليلاً. ومع ذلك، لأن كل أيون كالسيوم يحرك إلكترونين بدلاً من إلكترون واحد، ولأن البنية تبقى مستقرة وتتحرك الأيونات بسرعة، تبقى سعة تخزين الطاقة تنافسية. والأهم للمستقبل، الكالسيوم متوافر بكثرة ومنخفض التكلفة وغير ضار بيئياً. من خلال إظهار بالتفصيل المجهرى كيف يمكن للكالسيوم أن يتحرك بسهولة عبر TiS2 بينما تظل الشبكة المضيفة سليمة، يرسم هذا العمل قواعد تصميم لبطاريات متعددة التكافؤ من الجيل القادم: حافظ على إطار المضيف قوياً، دع الأيونات ترتبط بما يكفي لتتحرك بسرعة ولكن بشكل ضعيف بما يكفي لسهولة الحركة، واضبط البنية الإلكترونية بحيث يتدفق الشحن بسلاسة. يمكن الآن تطبيق هذه المبادئ على مواد طبقية أخرى في البحث عن بطاريات أيون الكالسيوم العملية.
الاستشهاد: Yang, S., Lee, S., Nogales, P.M. et al. Atomistic and electronic insights into Ca2+ and Li+ intercalation in TiS2: a first-principles approach supported by electrochemical validation. Sci Rep 16, 14605 (2026). https://doi.org/10.1038/s41598-026-42087-w
الكلمات المفتاحية: بطاريات أيون الكالسيوم, ثنائى كبريتيد التيتانيوم, أيونات متعددة التكافؤ, مواد البطاريات, انتشار الأيونات