Clear Sky Science · fr
Perspectives atomistiques et électroniques sur l’intercalation de Ca2+ et Li+ dans TiS2 : une approche par premiers principes soutenue par une validation électrochimique
Pourquoi une nouvelle chimie pour les batteries importe
Des smartphones aux voitures électriques, les batteries rechargeables actuelles reposent majoritairement sur le lithium. Mais le lithium est relativement rare et coûteux, et améliorer encore la technologie actuelle devient de plus en plus difficile. Cette étude explore une alternative : des batteries qui véhiculent des ions calcium plutôt que des ions lithium. En zoomant jusqu’à la structure atomique et électronique d’un matériau de batterie classique, le disulfure de titane (TiS2), les chercheurs posent une question simple aux implications larges : le calcium, qui transporte deux fois la charge par ion, peut‑il se déplacer facilement dans TiS2 et stocker l’énergie efficacement sans endommager le matériau ?
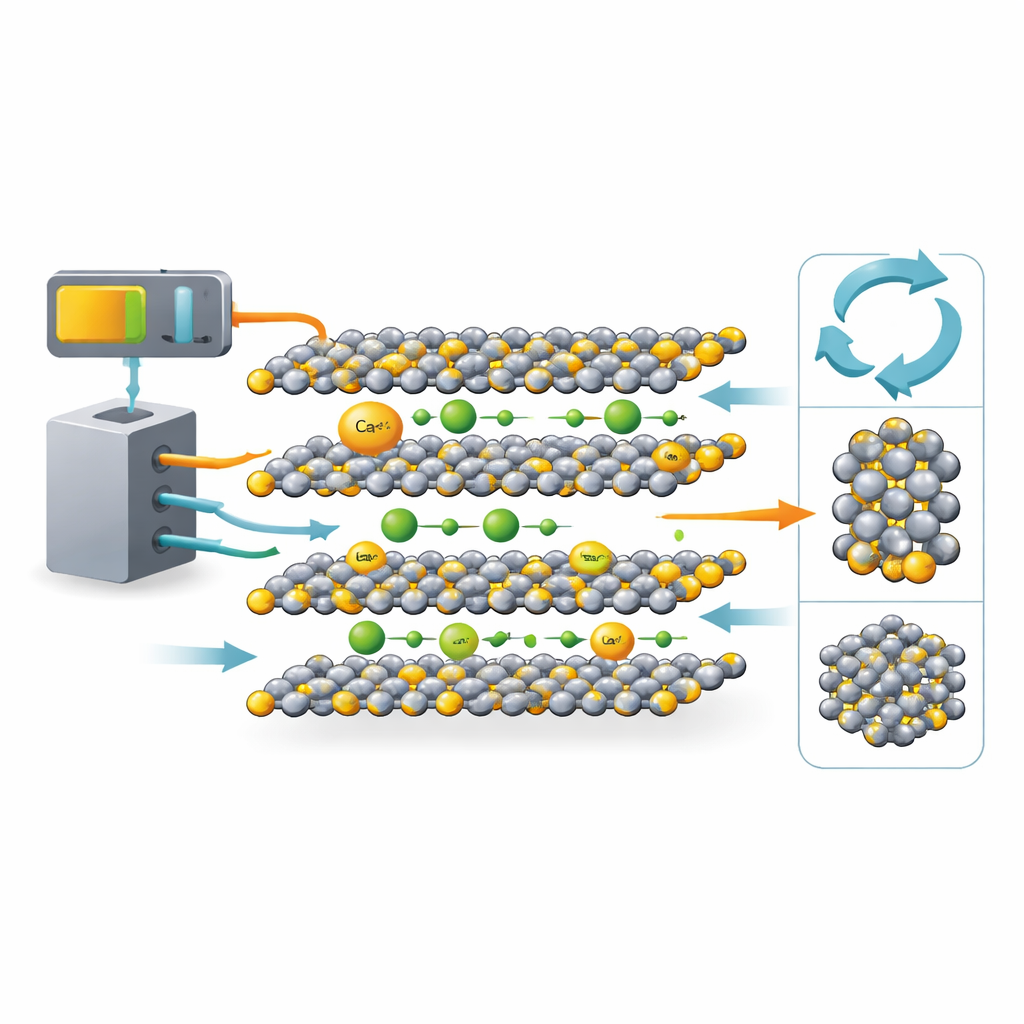
Un matériau de batterie familier sous un nouveau jour
Le TiS2 possède une longue histoire dans la recherche sur les batteries lithium‑ion. Sa structure cristalline est composée de couches plates empilées comme des feuilles de papier, avec des espaces entre elles où les ions peuvent s’insérer et ressortir. Cette architecture a fait du TiS2 un hôte classique pour les ions lithium. L’originalité de ce travail est de comparer le lithium et le calcium à l’intérieur du même réseau TiS2, côte à côte. Les ions calcium sont plus volumineux et portent une charge double, si bien que beaucoup de chercheurs craignaient qu’ils ne se déplacent lentement ou n’endommagent le réseau hôte. En choisissant le TiS2, un matériau bien compris, l’équipe peut distinguer les comportements intrinsèques aux ions de ceux liés à l’hôte.
Regarder les atomes et les électrons ensemble
Les chercheurs ont combiné des simulations informatiques avancées avec des tests de batteries réels. À l’aide de calculs de premiers principes, ils ont optimisé les positions atomiques dans TiS2 lorsqu’il est chargé soit de lithium soit de calcium, et ont suivi l’expansion des couches. Ils ont ensuite calculé la facilité avec laquelle chaque ion saute d’un site à un autre à l’intérieur du matériau et examiné comment les électrons se réarrangent à mesure que les ions s’insèrent. Un second jeu de calculs s’est concentré sur les liaisons chimiques locales : la force d’interaction des ions avec les atomes de soufre proches et la réponse du réseau titane–soufre. En parallèle, ils ont assemblé de véritables cellules bouton utilisant des électrodes TiS2 et des électrolytes portant soit des ions lithium soit des ions calcium, mesurant capacité, tension, vitesses de diffusion ionique et stabilité en cyclage.
Le calcium ouvre les voies tout en préservant l’ossature
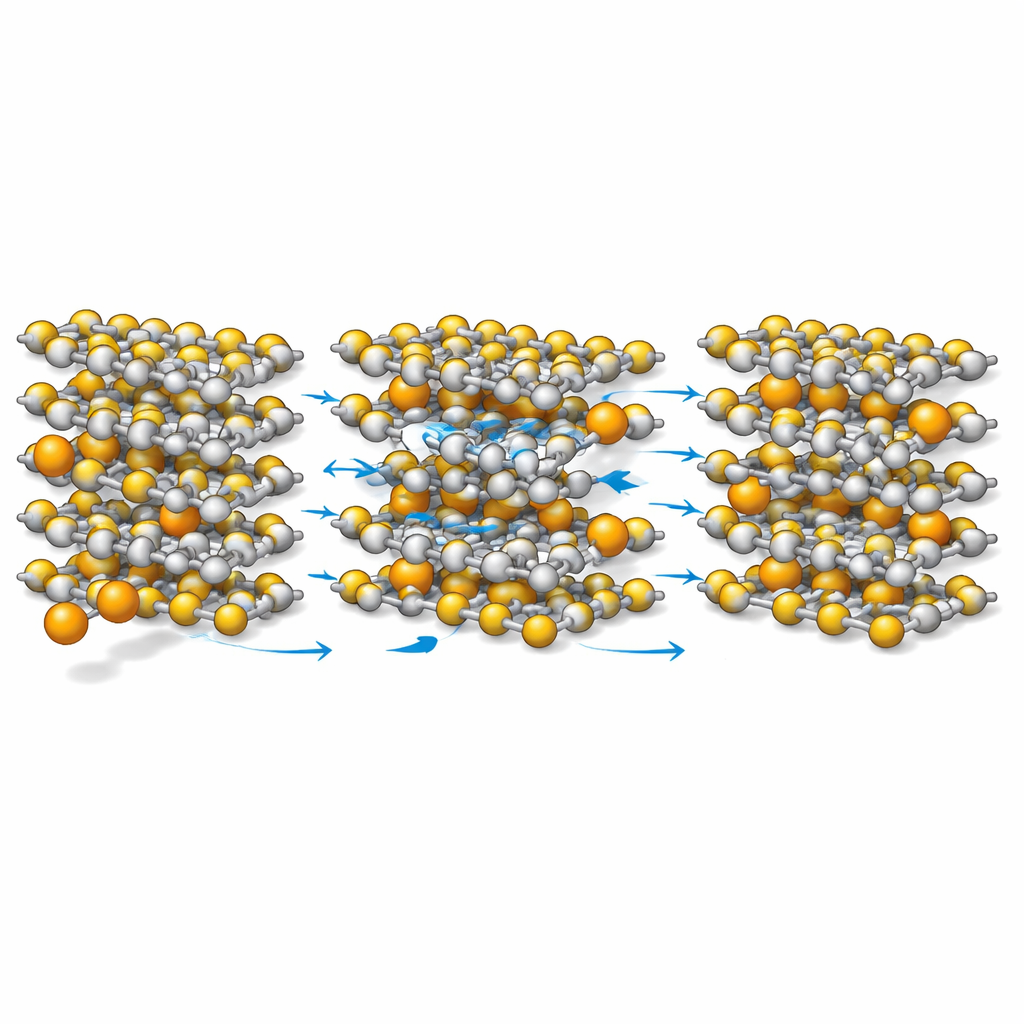
L’image à l’échelle atomique qui émerge est contre‑intuitive. Quand le calcium s’insère dans le TiS2, il écarte les couches davantage que le lithium, élargissant les canaux de déplacement des ions. En même temps, le calcium interagit plus faiblement avec les atomes de soufre que le lithium, ce qui signifie que les ions sont moins fortement « ancrés » et peuvent se déplacer plus librement. Pourtant, les liaisons titane–soufre qui maintiennent les couches se renforcent légèrement dans le cas du calcium, de sorte que le réseau global reste robuste. Les calculs montrent que la barrière énergétique pour la diffusion des ions calcium est inférieure à celle des ions lithium, et les états électroniques proches du niveau d’opération du matériau deviennent plus denses et mieux connectés, ce qui favorise la conduction électronique.
Ce que cela signifie pour les batteries réelles
Les tests électrochimiques confirment les prédictions théoriques. Dans des cellules à base de TiS2, l’intercalation du calcium fournit une première capacité de décharge d’environ 201 mAh par gramme — nettement supérieure aux ~134 mAh/g observés avec le lithium dans des conditions similaires. Le calcium montre aussi une diffusion ionique plus rapide, déduite de voltammétries cycliques, et de meilleures performances en taux : lorsque le courant de charge–décharge est augmenté puis réduit, les cellules au calcium conservent plus de 96 % de leur capacité initiale, contre environ 89 % pour les cellules au lithium. Sur 100 cycles, les deux chimies perdent progressivement de la capacité, mais le calcium maintient des valeurs légèrement supérieures tout en gardant un processus charge–décharge très réversible.
Équilibrer énergie, stabilité et aspect pratique
L’étude identifie toutefois un compromis : la tension moyenne du calcium dans TiS2 est plus faible que celle du lithium dans le même hôte, ce qui signifie que chaque unité de charge fournit un peu moins d’énergie. Cependant, parce que chaque ion calcium transporte deux électrons au lieu d’un, et parce que la structure reste stable et que les ions se déplacent rapidement, le stockage d’énergie global reste compétitif. Plus important pour la technologie future, le calcium est abondant, peu coûteux et respectueux de l’environnement. En montrant en détail microscopique comment le calcium peut circuler facilement dans TiS2 tout en laissant le réseau hôte intact, ce travail établit des règles de conception pour les batteries multivalentes de nouvelle génération : maintenir le réseau hôte solide, laisser les ions se lier suffisamment faiblement pour se mouvoir vite, et ajuster la structure électronique pour que le flux de charge soit fluide. Ces principes peuvent désormais être appliqués à d’autres matériaux en couches dans la quête de batteries au calcium pratiques.
Citation: Yang, S., Lee, S., Nogales, P.M. et al. Atomistic and electronic insights into Ca2+ and Li+ intercalation in TiS2: a first-principles approach supported by electrochemical validation. Sci Rep 16, 14605 (2026). https://doi.org/10.1038/s41598-026-42087-w
Mots-clés: batteries au calcium, disulfure de titane, ions multivalents, matériaux pour batteries, diffusion ionique