Clear Sky Science · pt
Percepções atomísticas e eletrônicas sobre a intercalação de Ca2+ e Li+ em TiS2: uma abordagem de primeiros princípios apoiada por validação eletroquímica
Por que uma nova química de baterias importa
De smartphones a carros elétricos, as baterias recarregáveis atuais dependem majoritariamente do lítio. Mas o lítio é relativamente raro e caro, e aumentar o desempenho das tecnologias vigentes está ficando mais difícil. Este estudo explora uma alternativa: baterias que transportam íons de cálcio em vez de íons de lítio. Ao examinar a estrutura atômica e eletrônica de um material clássico de baterias, o dissulfeto de titânio (TiS2), os pesquisadores fazem uma pergunta simples com grandes implicações: o cálcio, que carrega o dobro da carga por íon, pode se mover facilmente através do TiS2 e armazenar energia de forma eficiente sem danificar o material?
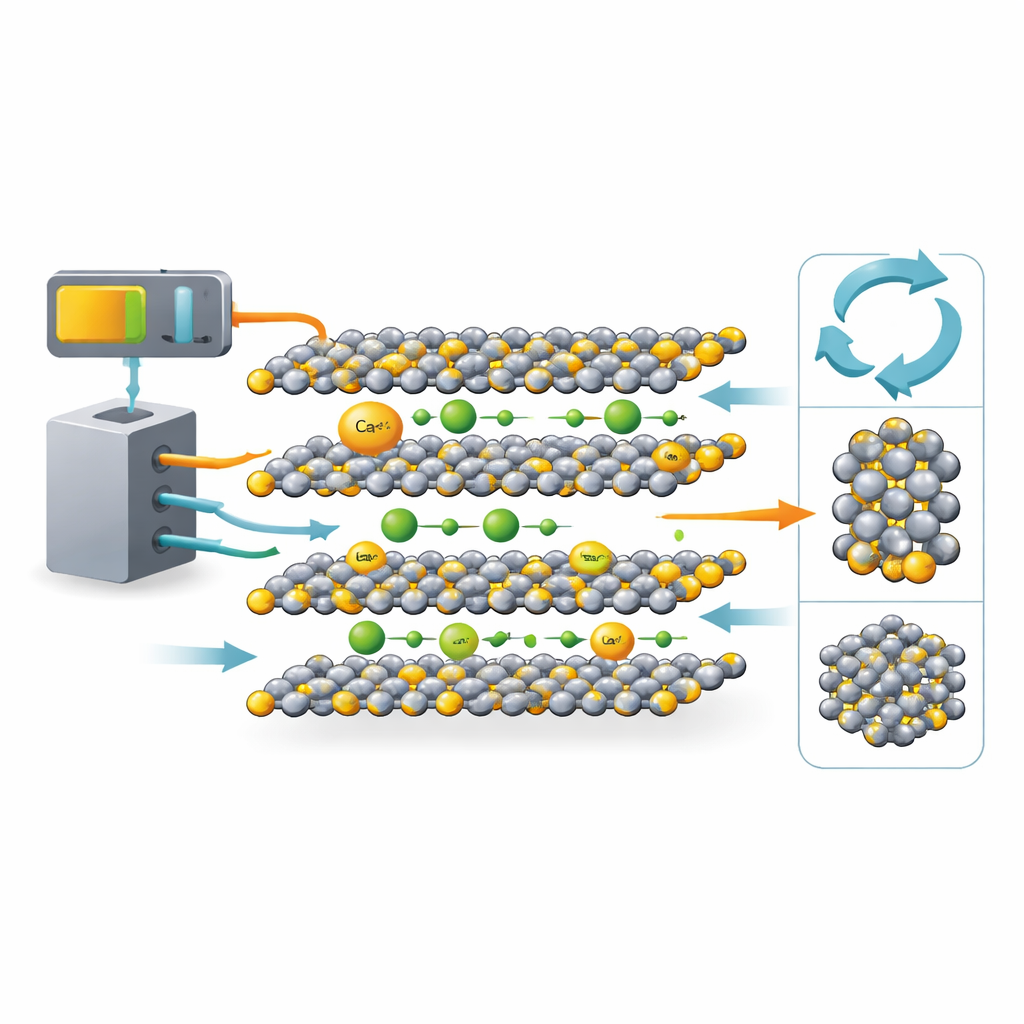
Um material de bateria familiar sob nova perspectiva
O TiS2 tem longa história na pesquisa com íons de lítio. Sua estrutura cristalina é formada por camadas planas empilhadas como folhas de papel, com espaços abertos entre elas onde os íons podem entrar e sair. Essa arquitetura tornou o TiS2 um hospedeiro clássico para íons de lítio. A novidade deste trabalho é comparar lítio e cálcio dentro do mesmo arcabouço de TiS2, lado a lado. Íons de cálcio são maiores e carregam carga dupla, então muitos cientistas temiam que se movessem lentamente ou danificassem a rede hospedeira. Ao escolher o TiS2, um material bem compreendido, a equipe consegue separar quais comportamentos derivam dos íons e quais provêm do hospedeiro.
Observando átomos e elétrons juntos
Os pesquisadores combinaram simulações computacionais avançadas com testes experimentais em baterias. Usando cálculos de primeiros princípios, otimizaram as posições atômicas no TiS2 quando preenchido com lítio ou cálcio e acompanharam como as camadas se expandem. Em seguida, calcularam com que facilidade cada íon salta de um sítio para outro dentro do material e examinaram como os elétrons se reordenam à medida que os íons entram. Um segundo conjunto de cálculos focou nas ligações químicas locais — quão fortemente os íons interagem com átomos de enxofre próximos e como a estrutura titânio–enxofre responde. Em paralelo, construíram células-cédula reais usando eletrodos de TiS2 e eletrólitos contendo íons de lítio ou cálcio, medindo capacidade, tensão, taxas de difusão iônica e estabilidade durante ciclos.
O cálcio abre os canais sem comprometer a estrutura
A imagem em escala atômica que emerge é contraintuitiva. Quando o cálcio entra no TiS2, ele separa as camadas mais do que o lítio, alargando os canais para o movimento iônico. Ao mesmo tempo, o cálcio interage mais fracamente com os átomos de enxofre do que o lítio, o que significa que os íons ficam menos “ancorados” e podem se mover com mais liberdade. Ainda assim, as ligações titânio–enxofre que mantêm as camadas juntas tornam-se ligeiramente mais fortes no caso do cálcio, de modo que a estrutura global permanece robusta. Os cálculos mostram que a barreira energética para a difusão de íons de cálcio é menor do que para os de lítio, e os estados eletrônicos próximos ao nível de operação do material ficam mais densos e conectados, favorecendo a condução eletrônica.
O que isso significa para baterias reais
Os testes eletroquímicos confirmam as previsões teóricas. Em células à base de TiS2, a intercalação de cálcio entrega uma capacidade de descarga inicial de cerca de 201 mAh por grama — substancialmente maior do que os cerca de 134 mAh por grama observados com lítio em condições semelhantes. O cálcio também mostra difusão iônica mais rápida, inferida por voltametria cíclica, e melhor desempenho em altas taxas: quando a corrente de carga–descarga é aumentada e depois reduzida, as células com cálcio retêm mais de 96% da capacidade original, contra cerca de 89% para as células com lítio. Ao longo de 100 ciclos, ambas as químicas perdem capacidade gradualmente, mas o cálcio mantém valores ligeiramente superiores enquanto mantém o processo carga–descarga altamente reversível.
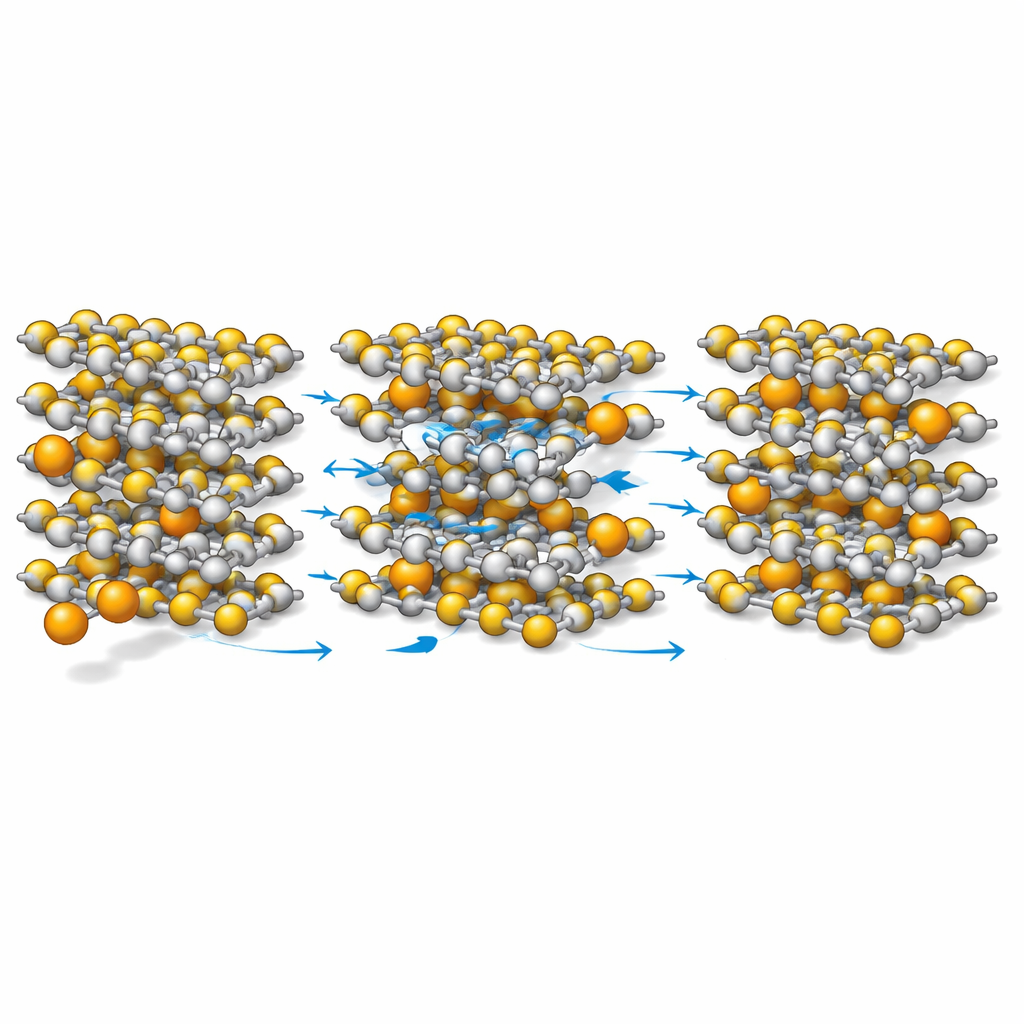
Equilibrando energia, estabilidade e praticidade
O estudo encontra um compromisso: a tensão média do cálcio em TiS2 é menor do que a do lítio no mesmo hospedeiro, o que significa que cada unidade de carga gera um pouco menos de energia. Contudo, porque cada íon de cálcio transfere dois elétrons em vez de um, e porque a estrutura permanece estável e os íons se movem rapidamente, o armazenamento energético global continua competitivo. Mais importante para a tecnologia futura, o cálcio é abundante, de baixo custo e ambientalmente benigno. Ao mostrar em detalhe microscópico como o cálcio pode se mover facilmente pelo TiS2 enquanto a rede hospedeira permanece intacta, este trabalho estabelece regras de projeto para baterias multivalentes de próxima geração: manter a estrutura do hospedeiro forte, permitir que os íons se liguem apenas o suficiente para se moverem rapidamente e ajustar a estrutura eletrônica para que a carga flua com facilidade. Esses princípios podem agora ser aplicados a outros materiais em camadas na busca por baterias íon-cálcio práticas.
Citação: Yang, S., Lee, S., Nogales, P.M. et al. Atomistic and electronic insights into Ca2+ and Li+ intercalation in TiS2: a first-principles approach supported by electrochemical validation. Sci Rep 16, 14605 (2026). https://doi.org/10.1038/s41598-026-42087-w
Palavras-chave: baterias íon-cálcio, dissulfeto de titânio, íons multivalentes, materiais para baterias, difusão iônica