Clear Sky Science · nl
Atomistische en elektronische inzichten in Ca2+ en Li+ intercalatie in TiS2: een first-principles-benadering ondersteund door elektrochimische validatie
Waarom nieuwe batterijchemie ertoe doet
Van smartphones tot elektrische auto’s: de meeste oplaadbare batterijen van vandaag zijn grotendeels afhankelijk van lithium. Maar lithium is relatief schaars en duur, en het verder verbeteren van de huidige technologie wordt steeds moeilijker. Deze studie verkent een alternatief: batterijen die calciumionen heen en weer transporteren in plaats van lithiumionen. Door in te zoomen op de atomaire en elektronische structuur van een klassiek batterijmateriaal, titaniumdisulfide (TiS2), stellen de onderzoekers een eenvoudige vraag met grote implicaties: kan calcium, dat per ion twee keer zoveel lading draagt, zich gemakkelijk door TiS2 verplaatsen en efficiënt energie opslaan zonder het materiaal te beschadigen?
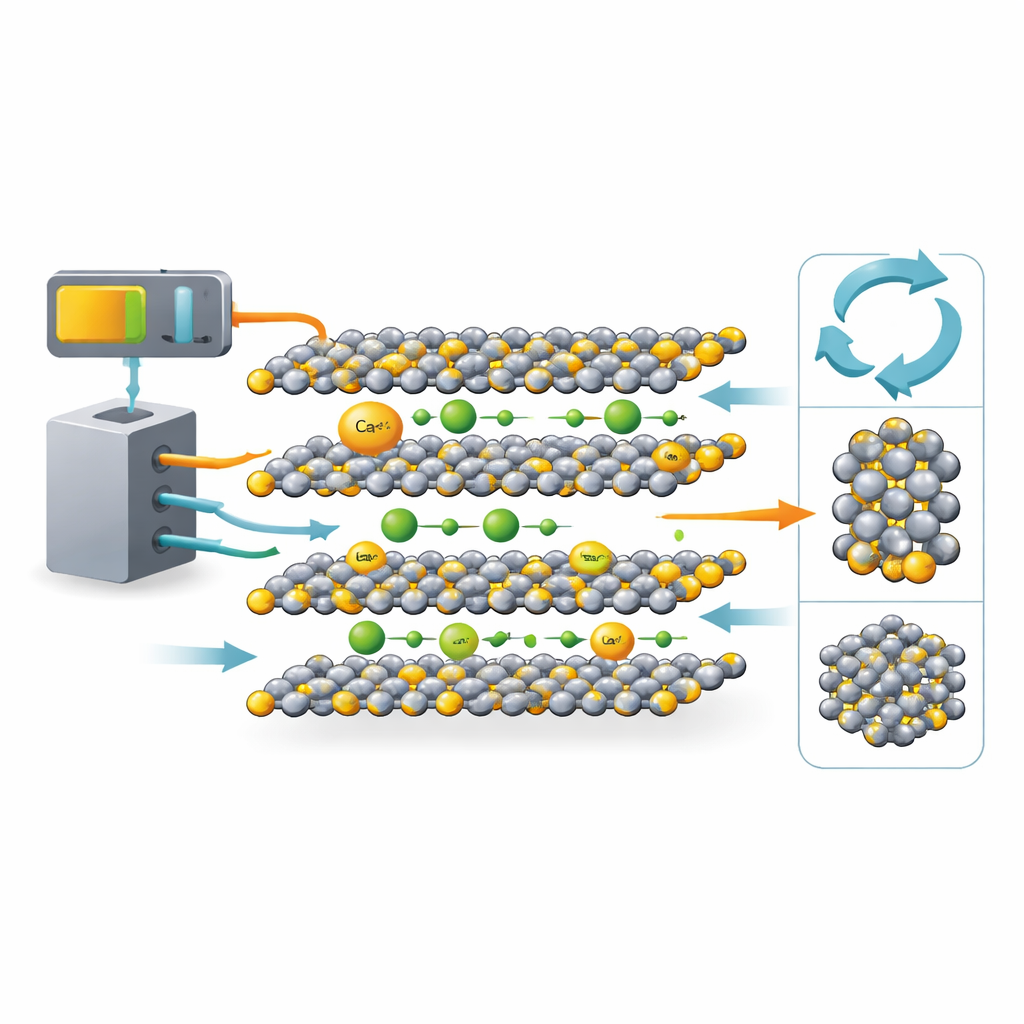
Een bekend batterijmateriaal in een nieuw daglicht
TiS2 heeft een lange geschiedenis in lithium-iononderzoek. De kristalstructuur bestaat uit vlakke lagen die als vellen papier op elkaar gestapeld zijn, met open ruimtes ertussen waar ionen in en uit kunnen schuiven. Die architectuur heeft van TiS2 een standaard gastheer voor lithiumionen gemaakt. De twist in dit werk is dat lithium en calcium in precies hetzelfde TiS2-raamwerk naast elkaar worden vergeleken. Calciumionen zijn groter en dragen een dubbele lading, waardoor veel wetenschappers vreesden dat ze traag zouden bewegen of het draagrooster zouden beschadigen. Door TiS2 te kiezen — een goed begrepen materiaal — kan het team uitsluiten welke gedragingen voortkomen uit de ionen zelf en welke uit het gastmateriaal.
Atomen en elektronen samen bekeken
De onderzoekers combineerden geavanceerde computersimulaties met echte batterijtesten. Met first-principles-berekeningen optimaliseerden ze de atomaire posities in TiS2 wanneer het gevuld is met ofwel lithium of calcium en volgden hoe de lagen uitzetten. Vervolgens berekenden ze hoe gemakkelijk elk ion van de ene naar de andere plaats springt binnen het materiaal en onderzochten ze hoe de elektronen zich herschikken als ionen binnendringen. Een tweede reeks berekeningen richtte zich op lokale chemische bindingen — hoe sterk de ionen met nabije zwavelatomen interacteren en hoe het titanium–zwavelraamwerk reageert. Parallel bouwden ze echte knoopcelletjes met TiS2-elektroden en elektrolyten die ofwel lithium- ofwel calciumionen bevatten, waarbij ze capaciteit, spanning, iondiffusiesnelheden en cyclusstabiliteit maten.
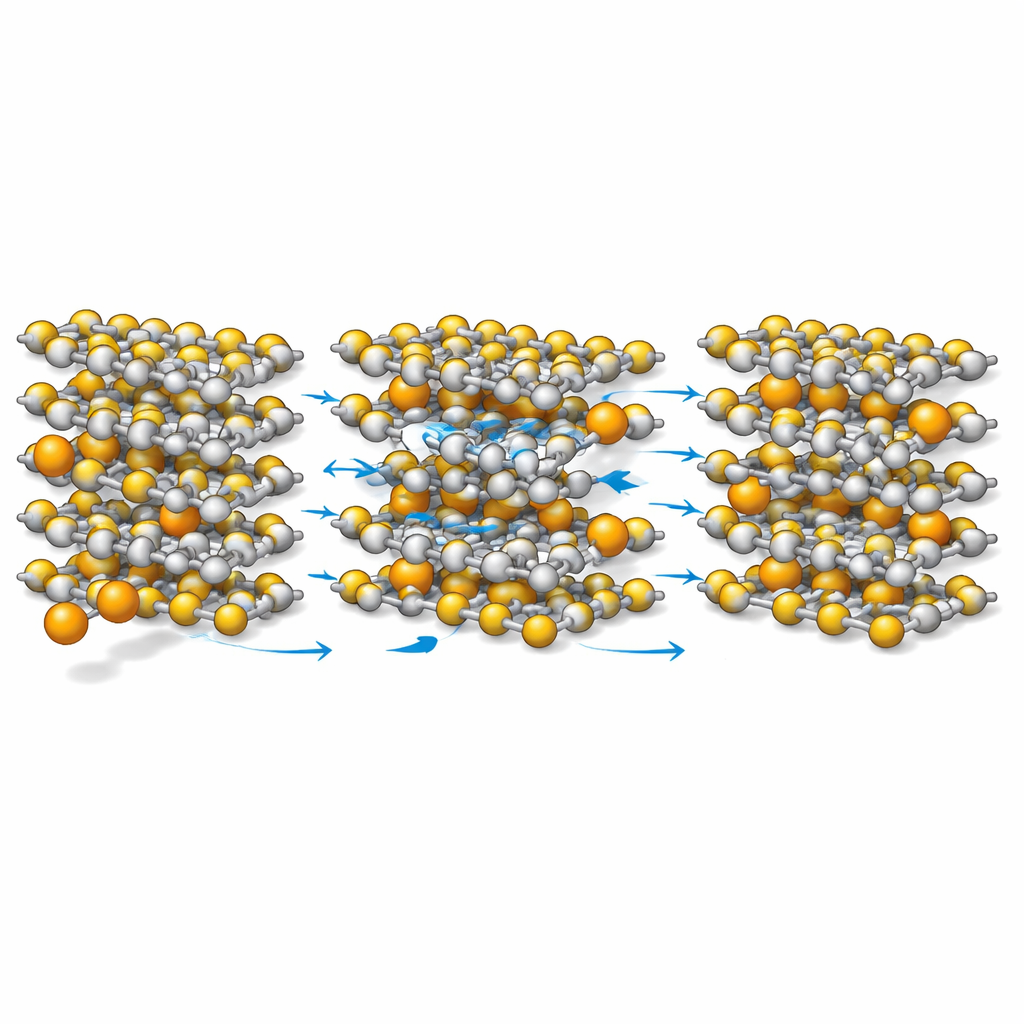
Calcium opent de kanalen maar behoudt het frame
Het atomaire beeld dat naar voren komt is contra-intuïtief. Wanneer calcium TiS2 binnendringt, duwt het de lagen verder uit elkaar dan lithium, waardoor de kanalen voor ionbeweging worden verbreed. Tegelijkertijd interageert calcium zwakker met de zwavelatomen dan lithium, wat betekent dat de ionen minder sterk verankerd zijn en vrijer kunnen bewegen. Toch worden de titanium–zwavelbindingen die de lagen bij elkaar houden in het calciumgeval juist iets sterker, zodat het algehele raamwerk robuust blijft. Berekeningen tonen aan dat de energiedrempel voor calciumdiffusie lager is dan voor lithium, en dat de elektronische toestanden nabij het bedrijfspeil van het materiaal dichter en beter verbonden raken, wat gunstig is voor elektronische geleiding.
Wat dit betekent voor echte batterijen
Elektrochemische tests weerspiegelen de theoretische voorspellingen. In TiS2-gebaseerde cellen levert calcium-intercalatie een eerste ontlaadcapaciteit van ongeveer 201 mAh per gram — aanzienlijk hoger dan de ongeveer 134 mAh per gram die bij lithium onder vergelijkbare omstandigheden wordt waargenomen. Calcium vertoont ook snellere iondiffusie, af te leiden uit cyclische voltammetrie, en betere snelheidsprestaties: wanneer de laad–ontlaadstroom wordt opgevoerd en daarna weer verlaagd, behouden de calciumcellen meer dan 96% van hun oorspronkelijke capaciteit, vergeleken met ongeveer 89% voor lithiumcellen. Over 100 cycli verliezen beide chemieën geleidelijk capaciteit, maar calcium handhaaft iets hogere waarden terwijl het laad–ontlaadproces zeer reversibel blijft.
Balanceren van energie, stabiliteit en bruikbaarheid
De studie vindt één compromis: de gemiddelde spanning van calcium in TiS2 is lager dan die van lithium in dezelfde gastheer, wat betekent dat elke ladingseenheid iets minder energie oplevert. Omdat elk calciumion echter twee elektronen verplaatst in plaats van één, en omdat de structuur stabiel blijft en de ionen snel bewegen, blijft de totale energiebuffer competitief. Belangrijker voor toekomstige technologie is dat calcium overvloedig, goedkoop en milieuvriendelijk is. Door in microniveau te laten zien hoe calcium gemakkelijk door TiS2 kan bewegen terwijl het gastrooster intact blijft, presenteert dit werk ontwerprichtlijnen voor de volgende generatie multivalente batterijen: houd het gastframework sterk, laat ionen net zwak genoeg binden om snel te bewegen, en stem de elektronische structuur zo af dat lading soepel stroomt. Die principes kunnen nu op andere gelaagde materialen worden toegepast in de zoektocht naar praktische calcium-ionbatterijen.
Bronvermelding: Yang, S., Lee, S., Nogales, P.M. et al. Atomistic and electronic insights into Ca2+ and Li+ intercalation in TiS2: a first-principles approach supported by electrochemical validation. Sci Rep 16, 14605 (2026). https://doi.org/10.1038/s41598-026-42087-w
Trefwoorden: calcium-ion batterijen, titaniumdisulfide, multivalente ionen, batterijmaterialen, iondiffusie