Clear Sky Science · de
Atomistische und elektronische Einblicke in die Interkalation von Ca2+ und Li+ in TiS2: ein erstprinzipieller Ansatz unterstützt durch elektrochemische Validierung
Warum neue Batteriech chemie zählt
Von Smartphones bis zu Elektroautos beruhen heutige wiederaufladbare Batterien größtenteils auf Lithium. Lithium ist jedoch relativ knapp und teuer, und es wird zunehmend schwieriger, die vorhandene Technologie weiter zu verbessern. Diese Studie untersucht eine Alternative: Batterien, die Kalziumionen statt Lithiumionen transportieren. Indem die Forschenden auf atomarer und elektronischer Ebene in ein klassisches Batteriematerial, das Titandisulfid (TiS2), hineinzoomen, stellen sie eine einfache Frage mit großen Folgen: Kann Kalzium — das pro Ion die doppelte Ladung trägt — sich leicht durch TiS2 bewegen und effizient Energie speichern, ohne das Material zu zerstören?
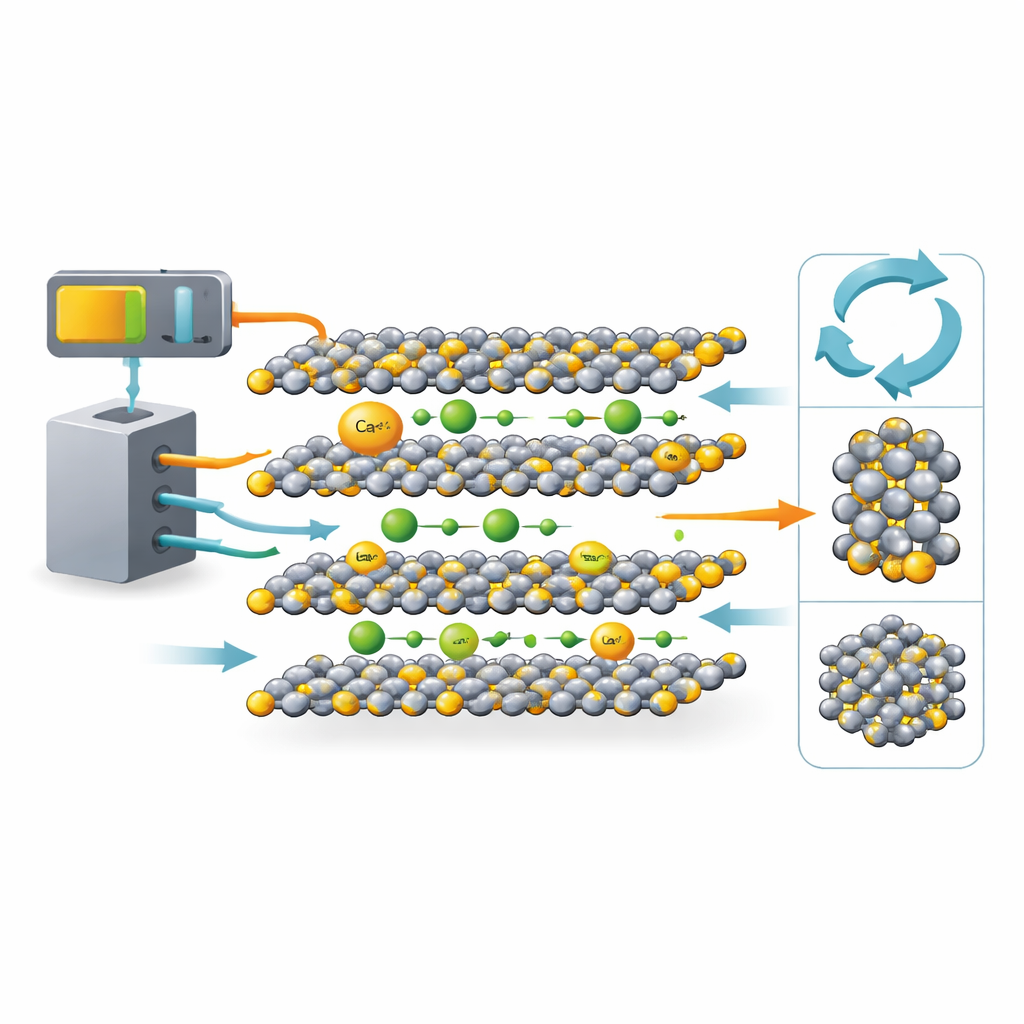
Ein vertrautes Batteriematerial im neuen Licht
TiS2 hat eine lange Geschichte in der Lithium-Ionen-Forschung. Seine Kristallstruktur besteht aus flachen Schichten, die wie Papierblätter gestapelt sind, mit offenen Zwischenräumen, in die Ionen ein- und austreten können. Diese Architektur machte TiS2 zu einem Lehrbuchbeispiel als Wirtsmaterial für Lithiumionen. Die Neuheit dieser Arbeit besteht darin, Lithium und Kalzium innerhalb desselben TiS2‑Gerüsts nebeneinander zu vergleichen. Kalziumionen sind größer und tragen die doppelte Ladung, weshalb viele Forschende befürchteten, sie würden sich träge bewegen oder das Wirtgitter beschädigen. Durch die Wahl von TiS2, einem gut verstandenen Material, kann das Team trennen, welche Verhaltensweisen von den Ionen selbst und welche vom Wirt ausgehen.
Atome und Elektronen gemeinsam betrachten
Die Forschenden kombinierten fortgeschrittene Computersimulationen mit realen Batterietests. Mithilfe erstprinzipieller Rechnungen optimierten sie die atomaren Positionen in TiS2, wenn es entweder mit Lithium oder Kalzium befüllt ist, und verfolgten, wie sich die Schichten ausdehnen. Anschließend berechneten sie, wie leicht jedes Ion von einem Platz zum anderen im Material springt, und untersuchten, wie sich die Elektronen neu anordnen, während Ionen einwandern. Eine zweite Rechnungsreihe konzentrierte sich auf lokale chemische Bindungen — wie stark die Ionen mit benachbarten Schwefelatomen wechselwirken und wie das Titan‑Schwefel‑Gerüst darauf reagiert. Parallel dazu bauten sie echte Knopfzellen mit TiS2‑Elektroden und Elektrolyten, die entweder Lithium‑ oder Kalziumionen transportierten, und maßen Kapazität, Spannung, Ionen‑Diffusionsraten und Zyklusstabilität.
Kalzium öffnet die Kanäle, erhält aber den Rahmen
Das auf atomarer Ebene entstehende Bild ist kontraintuitiv. Wenn Kalzium in TiS2 eintritt, drückt es die Schichten weiter auseinander als Lithium und erweitert so die Kanäle für die Ionenbewegung. Gleichzeitig wechselwirkt Kalzium schwächer mit den Schwefelatomen als Lithium, was bedeutet, dass die Ionen weniger stark „verankert“ sind und sich freier bewegen können. Dennoch werden die Titan‑Schwefel‑Bindungen, die die Schichten zusammenhalten, im Falle von Kalzium tatsächlich leicht stärker, sodass das Gesamtgerüst robust bleibt. Rechnungen zeigen, dass die Energiebarriere für die Diffusion von Kalziumionen niedriger ist als die für Lithiumionen, und die elektronischen Zustände in der Nähe des Betriebsenergielevels des Materials dichter und stärker vernetzt werden, was die elektronische Leitfähigkeit begünstigt.
Was das für reale Batterien bedeutet
Elektrochemische Tests bestätigen die theoretischen Vorhersagen. In TiS2‑basierten Zellen liefert die Kalzium‑Interkalation eine erste Entladekapazität von etwa 201 mAh pro Gramm — deutlich höher als die rund 134 mAh pro Gramm, die mit Lithium unter ähnlichen Bedingungen beobachtet wurden. Kalzium zeigt zudem schnellere Ionen‑Diffusion, abgeleitet aus zyklischer Voltammetrie, und bessere Leistungsfähigkeit bei höheren Strömen: Wenn der Lade‑/Entladestrom erhöht und anschließend wieder gesenkt wird, behalten die Kalziumzellen über 96 % ihrer ursprünglichen Kapazität, verglichen mit etwa 89 % bei Lithiumzellen. Über 100 Zyklen verlieren beide Chemien allmählich an Kapazität, aber Kalzium hält leicht höhere Werte bei und bewahrt gleichzeitig einen hoch reversiblen Lade‑/Entladeprozess.
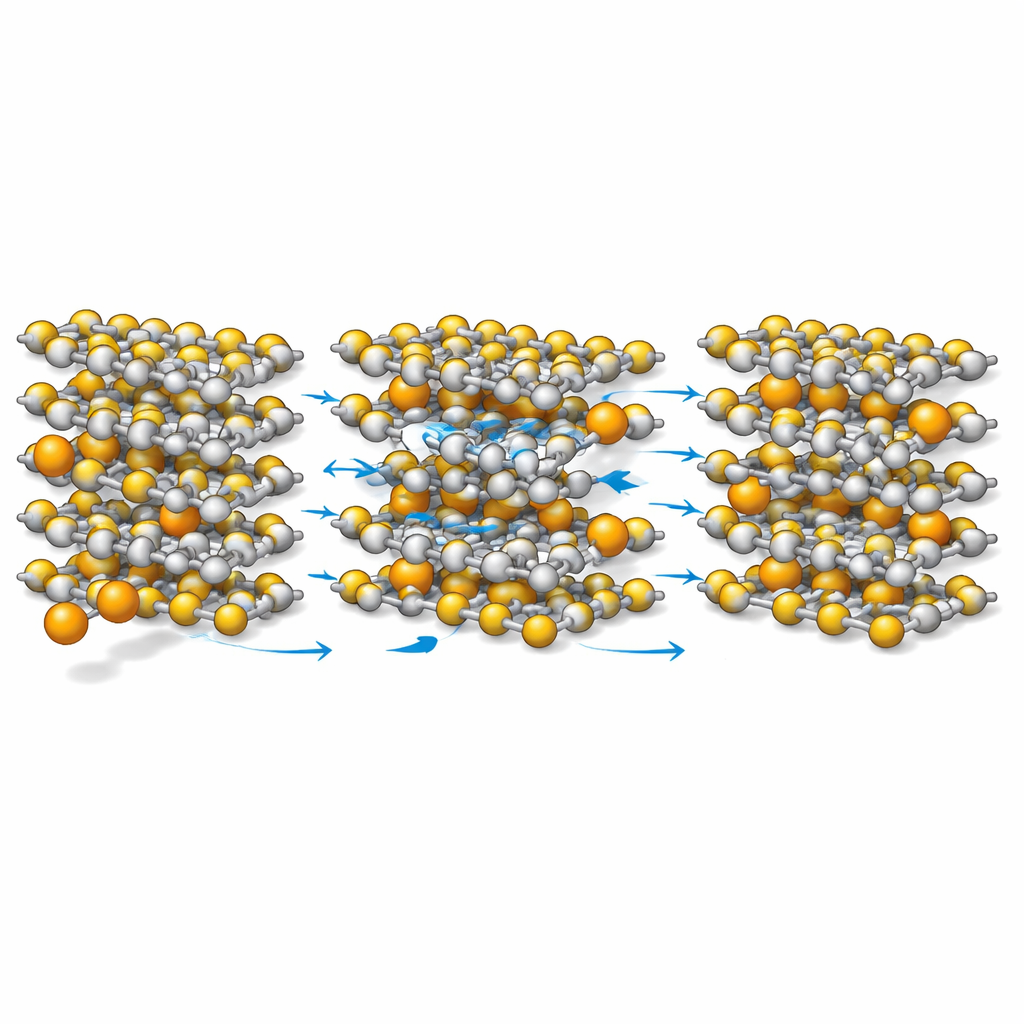
Energie, Stabilität und Praktikabilität ausbalancieren
Die Studie findet einen Kompromiss: Die mittlere Spannung von Kalzium in TiS2 ist niedriger als die von Lithium im selben Wirt, was bedeutet, dass jede Ladungseinheit etwas weniger Energie liefert. Da jedoch jedes Kalziumion zwei Elektronen statt einem verschiebt und weil die Struktur stabil bleibt und die Ionen sich schnell bewegen, bleibt die Gesamtenergiespeicherung wettbewerbsfähig. Wichtiger für künftige Technologien ist, dass Kalzium reichlich vorhanden, kostengünstig und umweltverträglich ist. Indem die Arbeit mikroskopisch darlegt, wie Kalzium sich leicht durch TiS2 bewegen kann, während das Wirtgitter intakt bleibt, liefert sie Gestaltungsprinzipien für die nächste Generation multivalenter Batterien: Das Wirtgerüst stark halten, die Bindung der Ionen gerade so schwach wählen, dass sie schnell bewegen können, und die elektronische Struktur so abstimmen, dass der Ladungstransport reibungslos verläuft. Diese Prinzipien können nun auf andere geschichtete Materialien angewendet werden, um praktikable Calcium‑Ionen‑Batterien zu finden.
Zitation: Yang, S., Lee, S., Nogales, P.M. et al. Atomistic and electronic insights into Ca2+ and Li+ intercalation in TiS2: a first-principles approach supported by electrochemical validation. Sci Rep 16, 14605 (2026). https://doi.org/10.1038/s41598-026-42087-w
Schlüsselwörter: Calcium-Ionen-Batterien, Titandisulfid, multivalente Ionen, Batteriematerialien, Ionen-Diffusion