Clear Sky Science · ru
Экстремедуллярные нишы кроветворения поддерживают появление и прогрессирование миелоидного злокачественного заболевания в селезёнке мыши
Почему селезёнка важна при заболеваниях крови
Когда мы думаем о том, где образуются клетки крови, обычно представляется костный мозг. Тем не менее у многих пациентов с онкологией крови, например лейкозом, наблюдается увеличение селезёнки, и врачи давно заметили, что это может свидетельствовать о более тяжёлом течении болезни. В этом исследовании на мышах задаётся на вид простой, но важный вопрос: может ли сама селезёнка превратиться в своего рода «теплицу», которая способствует росту и распространению опасных кровяных клеток? Раскрывая, как конкретная группа клеток селезёнки формирует такое скрытое окружение, работа предлагает новые пути замедлить или перенаправить развитие миелоидных заболеваний крови.
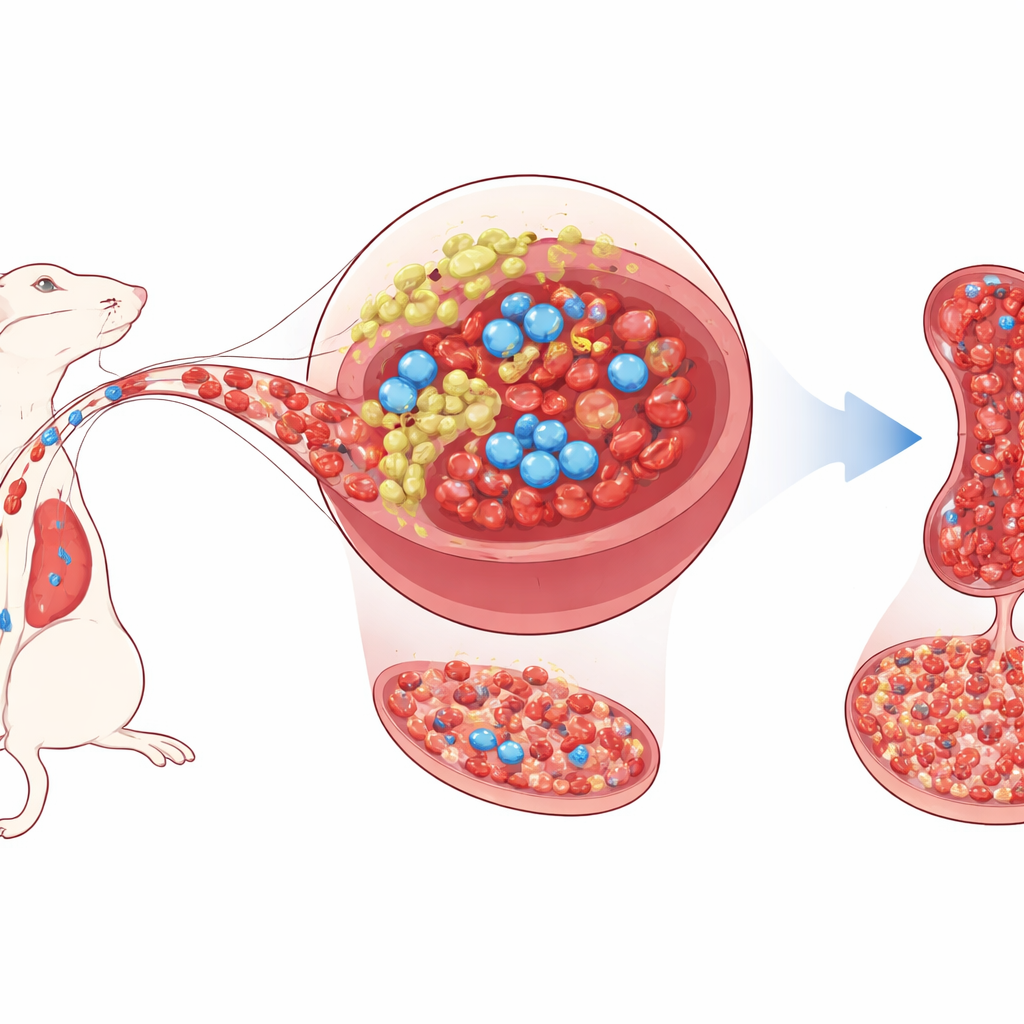
Второй дом для кроветворных клеток
Здоровые гемопоэтические стволовые клетки обычно обитают глубоко в костном мозге, где окружающие поддерживающие клетки снабжают их сигнальными факторами роста и контролируют их поведение. Селезёнка, наиболее известная как фильтр крови и орган иммунной защиты, также может включать резервное кроветворение в условиях стресса — процесс, называемый экстрамедуллярным кроветворением. Авторы сосредоточились на небольшой популяции поддерживающих клеток селезёнки у мышей — мезенхимальных стромальных/предшественниковых клетках — которые несут ген Tlx1. У взрослых мышей Tlx1 обнаруживается почти исключительно в этих клетках селезёнки. Ранее показали, что усиление активности Tlx1 мобилизует стволовые клетки из костного мозга в селезёнку и запускает там дополнительное кроветворение.
Как один переключатель перенастраивает селезёнку
Чтобы понять, как клетки с Tlx1 влияют на кроветворение, исследователи сначала воссоздали поддерживающую нишу селезёнки в культуре. Они модифицировали стромальные клетки селезёнки так, чтобы добавление препарата усиливало экспрессию Tlx1. Когда нормальные гемопоэтические стволовые и предшественниковые клетки выращивали на этих «включённых» клетках селезёнки, кровяные клетки размножались больше и умирали реже по сравнению с культурами на немодифицированных клетках селезёнки или на несвязанных фибробластах. Стромальные клетки с повышенным Tlx1 также вырабатывали больше нескольких ключевых факторов роста, известных как питательные для стволовых клеток. Иными словами, повышение Tlx1 превращало поддерживающие клетки селезёнки в мощную среду, расширяющую недифференцированные кровяные клетки.
Когда селезёнка становится убежищем для лейкемии
Далее команда изучила, что происходит при остром миелоидном лейкозе — быстро прогрессирующем раке миелоидных клеток крови. Используя хорошо изучённую линию лейкемических клеток у мышей, они трансплантировали раковые клетки животным и наблюдали за изменениями в органах со временем. По мере прогрессирования лейкемии селезёнка увеличивалась, а Tlx1-положительные стромальные клетки усиливали экспрессию Tlx1 и молекул, поддерживающих стволовые клетки. Микроскопия показала, что лейкемические клетки оседают в тесном контакте с Tlx1-богатыми нишами в красной пульпе селезёнки. Удаление селезёнки задерживало появление лейкемических клеток в кровотоке и умеренно продлевало выживаемость, что указывает на то, что этот орган активно подпитывает болезнь.
Включение или выключение ниши
Чтобы проверить причинно-следственную связь более напрямую, авторы создали два типа генетически изменённых мышей. В одной модели они могли искусственно сверхактивировать Tlx1 в стромальных клетках селезёнки, усиливая экстрамедуллярную кроветворную нишу. У этих мышей пересаженные лейкемические клетки охотнее мигрировали в селезёнку и накапливались в ней, раньше появлялись в крови и сокращали выживаемость по сравнению с нормальными сиблингами. Во второй модели они могли удалить Tlx1 специфически из стромальных клеток селезёнки. Здесь лейкемическим клеткам едва удавалось закрепиться в селезёнке, хотя костный мозг всё ещё сильно инфильтрировался, и общая выживаемость существенно не улучшалась. Эти эксперименты показывают, что ниши селезёнки, управляемые Tlx1, являются важными «пристыковочными станциями» для лейкемии, но не единственными участками, поддерживающими болезнь.
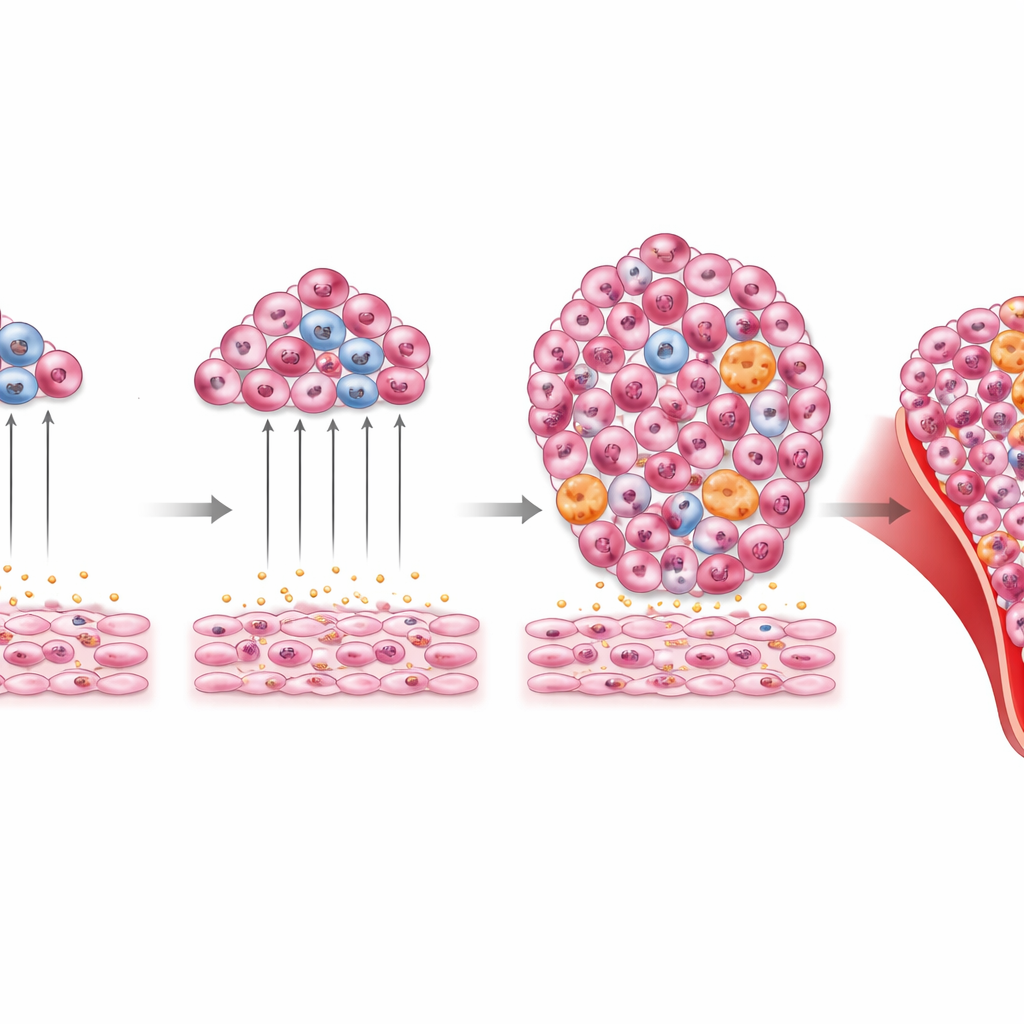
Когда резервное кроветворение заходит слишком далеко
История не ограничивается кратковременным ростом лейкемии. Исследователи также изучали, что происходит, когда Tlx1 остаётся повышенным в стромальных клетках селезёнки в течение многих месяцев, даже без введения лейкемических клеток. У мышей с хронической сверхэкспрессией Tlx1 развивались большие селезёнки, анемия, избыток лейкоцитов и деформированный костный мозг, заполненный миелоидными клетками и их предшественниками. Их печень оказалась инфильтрирована этими клетками, а мазки крови показали аномальные, незрелые формы. Важно, что при трансплантации клеток костного мозга или селезёнки от этих животных реципиенты развивали сходные миелоидные нарушения. Это указывает на то, что длительно действующая ниша селезёнки, управляемая Tlx1, может способствовать возникновению или поддержанию нездоровых популяций миелоидных клеток, которые ведут себя как миелоидная злокачественность.
Что это значит для пациентов
В целом работа изображает селезёнку не как пассивного наблюдателя, а как активного партнёра при отдельных заболеваниях крови. Включив переключатель Tlx1 в специализированной группе поддерживающих клеток, селезёнка может привлекать нормальные и злокачественные предшественники, усиливать их рост и, со временем, способствовать появлению аномальных миелоидных клеток. Для пациентов это означает, что терапии, направленные на изменение или ослабление благоприятной для лейкемии ниши селезёнки — а не удаление органа — в будущем могут дополнить существующие методы лечения. Хотя у людей ситуация сложнее, чем у мышей, и остаётся много вопросов, исследование подчёркивает, что места, где живут раковые клетки, могут быть столь же важной мишенью, как и сами раковые клетки.
Цитирование: Oda, A., Tezuka, T., Nakamura, T. et al. Extramedullary hematopoietic niches support the initiation and progression of myeloid malignancy in the murine spleen. Sci Rep 16, 11211 (2026). https://doi.org/10.1038/s41598-026-41461-y
Ключевые слова: острый миелоидный лейкоз, ниша селезёнки, экстрамедуллярное кроветворение, гемопоэтические стволовые клетки, миелоидная злокачественность