Clear Sky Science · es
Las nichos hematopoyéticos extramedulares sostienen la iniciación y progresión de la malignidad mieloide en el bazo murino
Por qué el bazo importa en el cáncer de la sangre
Cuando pensamos en dónde se produce la sangre, normalmente viene a la mente la médula ósea. Sin embargo, muchos pacientes con cánceres sanguíneos como la leucemia desarrollan también esplenomegalia, y los médicos llevan tiempo observando que eso puede indicar una enfermedad más grave. Este estudio en ratones plantea una pregunta aparentemente sencilla con grandes implicaciones: ¿puede el propio bazo convertirse en una especie de “invernadero” que facilita el crecimiento y la diseminación de células sanguíneas peligrosas? Al desvelar cómo un grupo específico de células esplénicas configura ese entorno oculto, el trabajo sugiere nuevas maneras de frenar o desviar la evolución de los cánceres mieloides de la sangre.
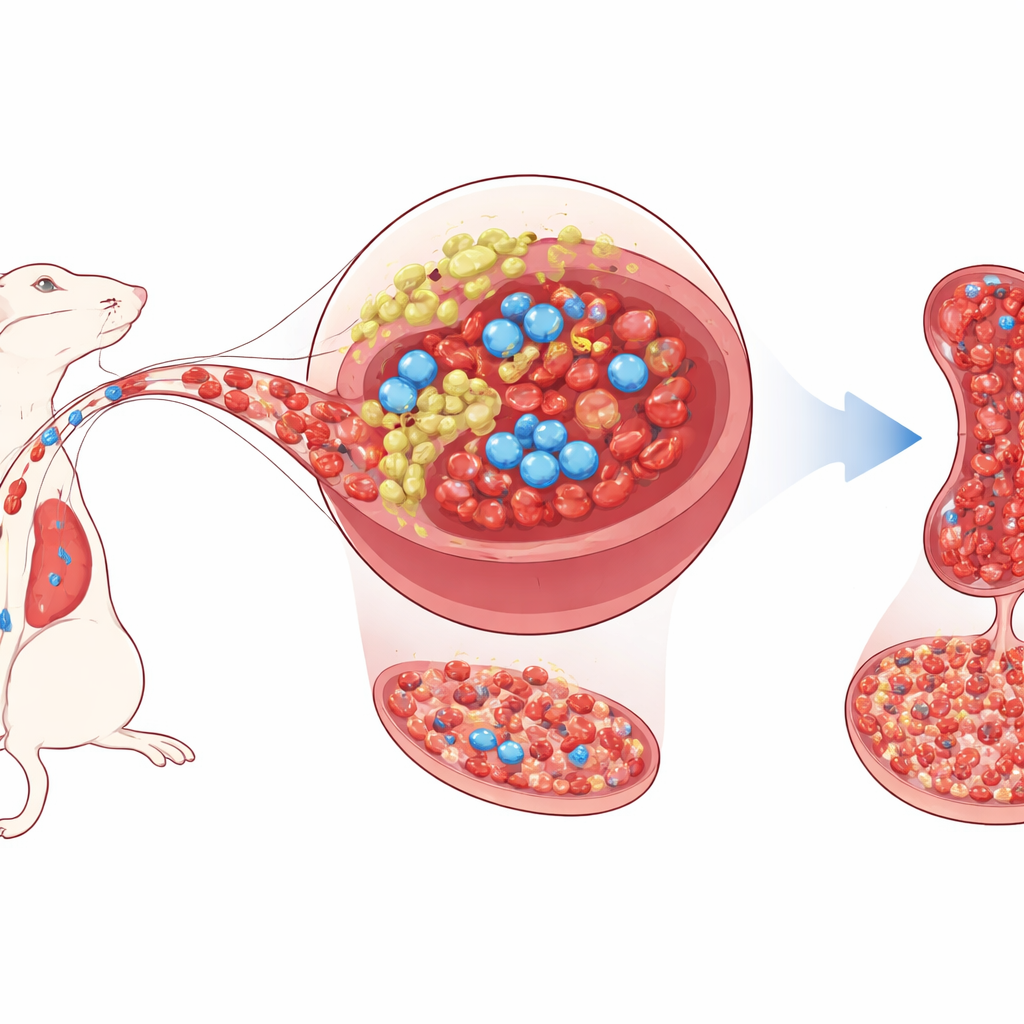
Un segundo hogar para las células formadoras de sangre
Las células madre formadoras de sangre sanas suelen vivir en lo profundo de la médula ósea, donde las células vecinas de apoyo les suministran señales de crecimiento y regulan su comportamiento. El bazo, conocido sobre todo por filtrar la sangre y combatir infecciones, también puede activar una producción sanguínea de respaldo bajo estrés, un proceso llamado hematopoyesis extramedular. Los autores se centran en una pequeña población de células de apoyo en el bazo de ratón: células estromales/progenitoras mesenquimales que expresan un gen llamado Tlx1. En ratones adultos, Tlx1 se encuentra casi exclusivamente en estas células esplénicas. Trabajos previos mostraron que aumentar la actividad de Tlx1 moviliza células madre desde la médula ósea hacia el bazo e inicia la producción extra de sangre allí.
Cómo un único interruptor reorganiza el bazo
Para entender cómo estas células portadoras de Tlx1 influyen en la formación sanguínea, los investigadores recrearon primero el nicho de apoyo esplénico en placa. Diseñaron células estromales esplénicas de modo que la adición de un fármaco incrementara Tlx1. Cuando células madre y progenitoras sanguíneas normales se cultivaron sobre estas células esplénicas “activadas”, las células sanguíneas proliferaron más y murieron menos, en comparación con cultivos sobre células esplénicas sin alterar o sobre fibroblastos no relacionados. Las células estromales con alta expresión de Tlx1 también producían más varios factores de crecimiento clave conocidos por nutrir a las células madre. En otras palabras, elevar Tlx1 convirtió a las células de apoyo esplénico en una cuna potente que expande células sanguíneas inmaduras.
Cuando el bazo se convierte en refugio para la leucemia
El equipo preguntó luego qué sucede durante la leucemia mieloide aguda, un cáncer de rápido crecimiento de células mieloides. Usando una línea celular leucémica de ratón bien establecida, trasplantaron células cancerosas en animales y observaron cómo cambiaban los órganos con el tiempo. A medida que la leucemia progresaba, el bazo se agrandaba y sus células estromales positivas para Tlx1 aumentaban Tlx1 y las moléculas que sostienen a las células madre. La microscopía mostró células leucémicas asentándose en contacto cercano con nichos ricos en Tlx1 en las zonas de pulpa roja del bazo. La extirpación del bazo retrasó la aparición de células leucémicas en la sangre y prolongó modestamente la supervivencia, lo que sugiere que este órgano ayuda activamente a alimentar la enfermedad.
Subir o bajar el nicho
Para probar la relación de causalidad de forma más directa, los autores crearon dos tipos de ratones genéticamente alterados. En uno, podían sobreactivar artificialmente Tlx1 en las células estromales esplénicas, exagerando el nicho de hematopoyesis extramedular. En estos ratones, las células leucémicas trasplantadas se dirigieron y acumularon en el bazo con mucha más facilidad, se vertieron antes en la sangre y acortaron la supervivencia en comparación con los hermanos normales. En el segundo modelo, podían eliminar Tlx1 específicamente de las células estromales esplénicas. Aquí, las células leucémicas apenas lograron establecerse en el bazo, aunque la médula ósea siguió estando fuertemente infiltrada y la supervivencia global no mejoró de forma drástica. Estos experimentos revelan que los nichos esplénicos impulsados por Tlx1 son estaciones de acoplamiento cruciales para la leucemia, pero no son los únicos sitios que sostienen la enfermedad.
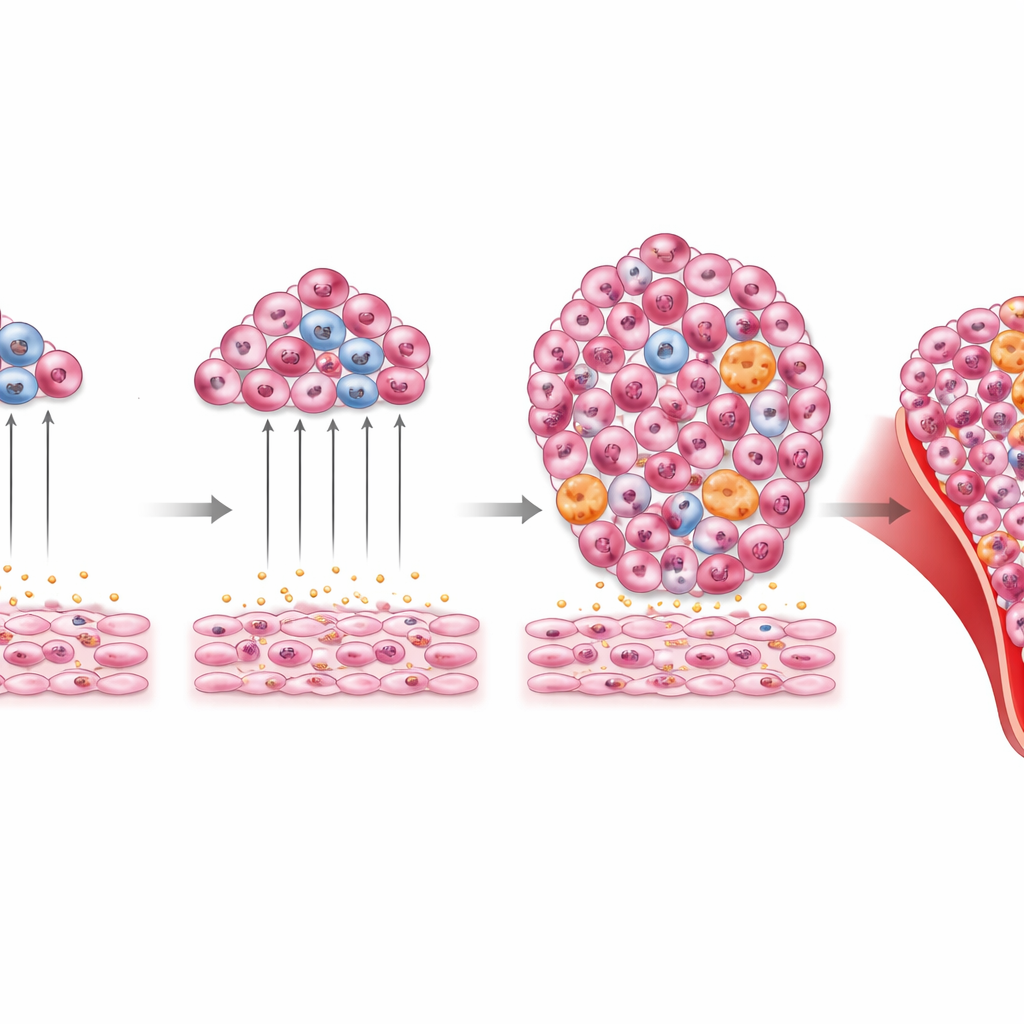
Cuando la producción de sangre de respaldo se desboca
La historia no termina con el crecimiento leucémico a corto plazo. Los investigadores también examinaron qué sucede cuando Tlx1 se mantiene alto en las células estromales esplénicas durante muchos meses, incluso sin inyectar células leucémicas. Los ratones con sobreexpresión crónica de Tlx1 desarrollaron bazo grande, anemia, exceso de glóbulos blancos y médula ósea deformada, repleta de células mieloides y sus precursores. Sus hígados quedaron infiltrados por estas células, y los frotis sanguíneos mostraron formas anormales e inmaduras. Es importante, que cuando las células de médula ósea o del bazo de estos animales se trasplantaron a nuevos receptores, los receptores desarrollaron anomalías mieloides similares. Esto indica que el nicho esplénico sostenido por Tlx1 puede ayudar a generar o mantener poblaciones mieloides perjudiciales que se comportan como una malignidad mieloide.
Qué significa esto para los pacientes
En conjunto, el trabajo presenta al bazo no como un espectador pasivo sino como un socio activo en ciertos cánceres de la sangre. Al accionar el interruptor Tlx1 en un grupo especializado de células de apoyo, el bazo puede reclutar precursores normales y malignos, potenciar su crecimiento y, con el tiempo, promover el surgimiento de células mieloides anómalas. Para los pacientes, esto sugiere que las terapias dirigidas a remodelar o atenuar el nicho esplénico favorable a la leucemia —en lugar de extirpar el órgano por completo— podrían algún día complementar los tratamientos existentes. Aunque los humanos son más complejos que los ratones y quedan muchas preguntas, el estudio subraya cómo los lugares donde viven las células cancerosas pueden ser un objetivo tan importante como las propias células cancerosas.
Cita: Oda, A., Tezuka, T., Nakamura, T. et al. Extramedullary hematopoietic niches support the initiation and progression of myeloid malignancy in the murine spleen. Sci Rep 16, 11211 (2026). https://doi.org/10.1038/s41598-026-41461-y
Palabras clave: leucemia mieloide aguda, nicho esplénico, hematopoyesis extramedular, células madre hematopoyéticas, malignidad mieloide