Clear Sky Science · de
Extramedulläre hämatopoetische Nischen unterstützen die Initiierung und Progression myeloischer Malignität in der murinen Milz
Warum die Milz bei Blutkrebs wichtig ist
Wenn wir an den Ort denken, an dem Blut gebildet wird, fällt den meisten zuerst das Knochenmark ein. Viele Patientinnen und Patienten mit Blutkrebs wie Leukämie entwickeln jedoch auch vergrößerte Milzen, und Kliniker beobachten seit langem, dass dies ein Zeichen für eine schwerere Erkrankung sein kann. Diese Studie an Mäusen stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Kann die Milz selbst zu einer Art „Gewächshaus“ werden, das gefährliche Blutzellen fördert und verbreiten hilft? Indem sie zeigen, wie eine bestimmte Gruppe von Milzzellen dieses verborgene Umfeld formt, deutet die Arbeit auf neue Wege hin, den Verlauf myeloischer Blutkrebserkrankungen zu verlangsamen oder umzulenken.
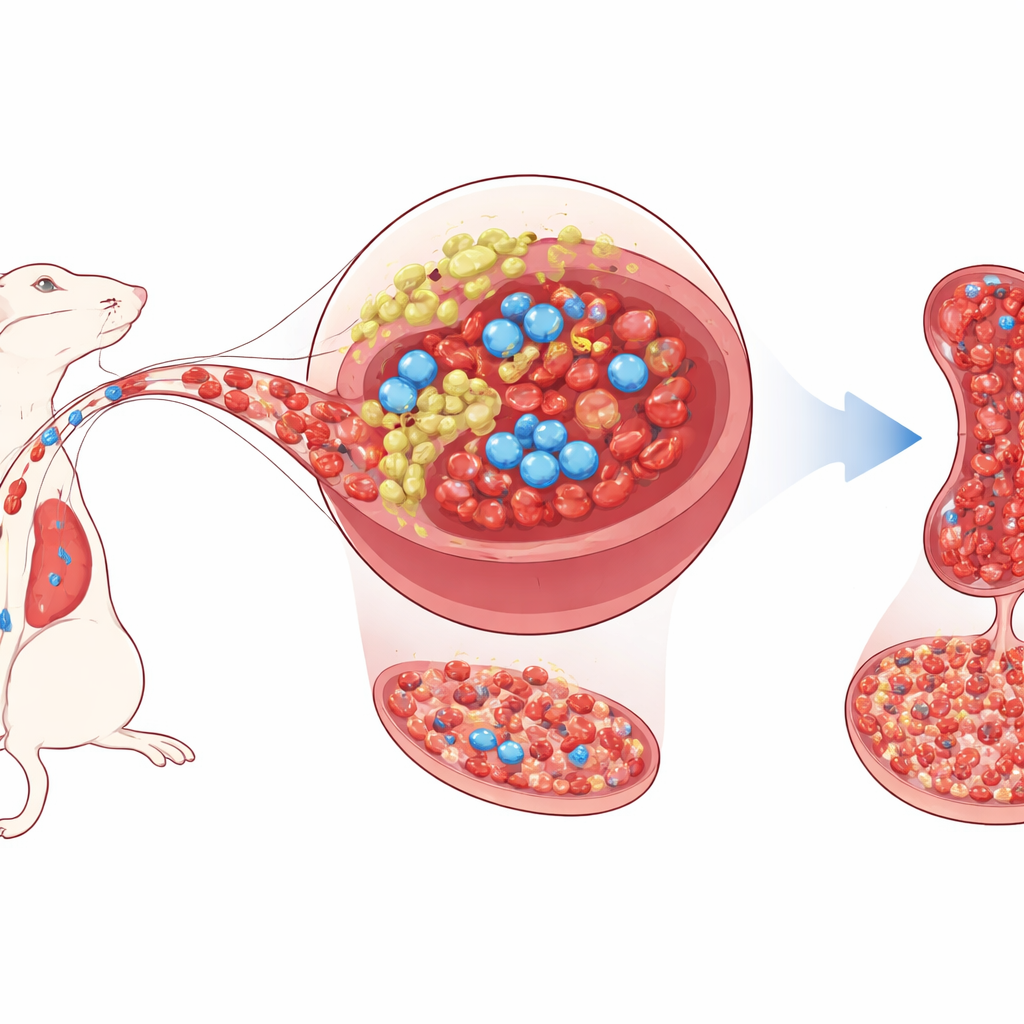
Ein zweites Zuhause für blutbildende Zellen
Gesunde blutbildende Stammzellen wohnen normalerweise tief im Knochenmark, wo benachbarte Stütz- und Nährzellen sie mit Wachstumsfaktoren versorgen und ihr Verhalten regulieren. Die Milz, am besten bekannt für Blutfilterung und Abwehr von Infektionen, kann unter Stress auch die Blutbildung als Reserve aktivieren – ein Prozess, der als extramedulläre Hämatopoese bezeichnet wird. Die Autorinnen und Autoren konzentrieren sich auf eine kleine Population von Stütz- und Vorläuferzellen in der Mäusemilz – mesenchymale stromale/progenitorische Zellen –, die das Gen Tlx1 tragen. Bei erwachsenen Mäusen findet sich Tlx1 nahezu ausschließlich in diesen milzspezifischen Zellen. Frühere Arbeiten zeigten, dass eine verstärkte Aktivierung von Tlx1 Stammzellen aus dem Knochenmark in die Milz mobilisiert und dort die zusätzliche Blutbildung anstößt.
Wie ein einziger Schalter die Milz umbaut
Um zu verstehen, wie diese Tlx1-exprimierenden Zellen die Blutbildung beeinflussen, rekonstruierten die Forschenden zunächst die Milznische in vitro. Sie veränderten milzstaminale Stromazellen so, dass ein zugesetztes Medikament Tlx1 verstärkt einschalten konnte. Wurden normale blutbildende Stamm- und Vorläuferzellen auf diesen „eingeschalteten“ Milzzellen kultiviert, teilten sich die Blutzellen stärker und zeigten weniger Zelltod, verglichen mit Kulturen auf unveränderten Milzzellen oder auf nicht verwandten Fibroblasten. Die Tlx1-hohen Stromazellen produzierten zudem mehrerer wichtiger Wachstumsfaktoren, die Stammzellen nähren. Anders ausgedrückt verwandelte die Hochregulierung von Tlx1 die milzspezifischen Stützellen in eine potente Wiege, die unreife Blutzellen expandiert.
Wenn die Milz zur Leukämie-Zuflucht wird
Das Team untersuchte anschließend, was bei akuter myeloischer Leukämie geschieht, einer schnell wachsenden Krebserkrankung der myeloischen Blutzellen. Mithilfe einer etablierten murinen Leukämiezelllinie transplantierten sie Krebszellen in Tiere und verfolgten, wie sich Organe im Zeitverlauf veränderten. Mit dem Fortschreiten der Leukämie vergrößerte sich die Milz, und ihre Tlx1-positiven Stromazellen steigerten Tlx1 sowie stammezellunterstützende Moleküle. Mikroskopische Aufnahmen zeigten Leukämiezellen, die engen Kontakt zu Tlx1-reichen Nischen in den roten Pulpa-Regionen der Milz aufnahmen. Die Entfernung der Milz verzögerte das Auftreten von Leukämiezellen im Blut und verlängerte das Überleben moderat, was darauf hindeutet, dass dieses Organ aktiv zur Förderung der Erkrankung beiträgt.
Die Nische hoch- oder herunterregeln
Um Ursache und Wirkung direkter zu testen, erzeugten die Autorinnen und Autoren zwei Typen genetisch veränderter Mäuse. In einem Modell konnten sie Tlx1 in milzstamminalen Stromazellen künstlich überaktivieren und so die extramedulläre Blutsbildungsnische verstärken. In diesen Tieren homten sich transplantierte Leukämiezellen deutlich stärker in die Milz, sammeltenz sich dort an, traten früher ins Blut über und verkürzten das Überleben im Vergleich zu normalen Wurfgeschwistern. Im zweiten Modell konnten sie Tlx1 spezifisch in milzstamminalen Stromazellen löschen. Hier schafften es Leukämiezellen kaum, in der Milz Fuß zu fassen, obwohl das Knochenmark weiterhin stark infiltriert wurde und das Gesamtüberleben sich nicht dramatisch verbesserte. Diese Experimente zeigen, dass Tlx1-getriebene Milz-Nischen wichtige Andockstellen für Leukämie sind, aber nicht die einzigen Orte, die die Erkrankung stützen.
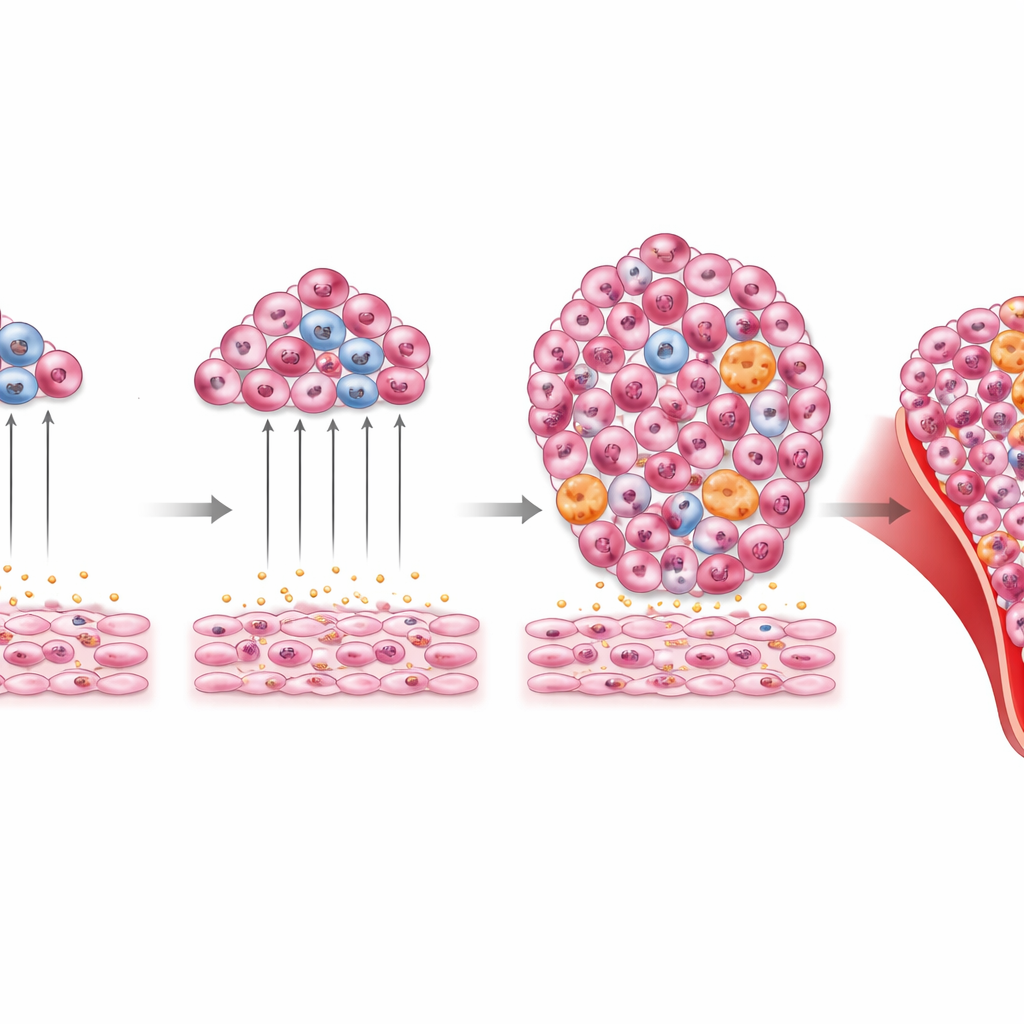
Wenn die Reserveblutbildung außer Kontrolle gerät
Die Geschichte endet nicht bei kurzfristigem Leukämiewachstum. Die Forschenden betrachteten auch, was passiert, wenn Tlx1 in milzstamminalen Stromazellen über viele Monate hoch bleibt, selbst ohne Transplantation von Leukämiezellen. Mäuse mit chronischer Tlx1-Überexpression entwickelten große Milzen, Anämie, eine Überzahl weißer Blutkörperchen und verzerrtes Knochenmark, das mit myeloischen Zellen und ihren Vorläufern gefüllt war. Auch die Leber wurde von diesen Zellen infiltriert, und Blutabstriche zeigten abnorme, unreife Erscheinungsformen. Wichtig ist: Wurden Knochenmark- oder Milzzellen dieser Tiere in neue Empfänger transplantiert, entwickelten die Empfänger ähnliche myeloische Auffälligkeiten. Das deutet darauf hin, dass die lang anhaltende, Tlx1-getriebene Milz-Nische zur Entstehung oder Aufrechterhaltung ungesunder myeloischer Zellpopulationen beitragen kann, die sich wie eine myeloische Malignität verhalten.
Was das für Patientinnen und Patienten bedeutet
Insgesamt zeichnet die Arbeit das Bild der Milz nicht als passiven Zuschauer, sondern als aktiven Partner bei bestimmten Blutkrebserkrankungen. Durch das Umschalten des Tlx1-Schalters in einer spezialisierten Gruppe von Stützellen kann die Milz normale und maligne Vorläufer anziehen, ihr Wachstum fördern und langfristig die Entstehung abnormer myeloischer Zellen begünstigen. Für Patientinnen und Patienten legt dies nahe, dass Therapien, die darauf abzielen, die leukämiefreundliche Nische der Milz umzugestalten oder zu dämpfen – statt das Organ routinemäßig zu entfernen – eines Tages die bestehenden Behandlungen ergänzen könnten. Obwohl der Mensch komplexer ist als die Maus und viele Fragen offen bleiben, hebt die Studie hervor, dass die Orte, an denen Krebszellen leben, genauso wichtige Angriffspunkte sein können wie die Krebszellen selbst.
Zitation: Oda, A., Tezuka, T., Nakamura, T. et al. Extramedullary hematopoietic niches support the initiation and progression of myeloid malignancy in the murine spleen. Sci Rep 16, 11211 (2026). https://doi.org/10.1038/s41598-026-41461-y
Schlüsselwörter: akute myeloische Leukämie, Milz-Nische, extramedulläre Hämatopoese, hämatopoetische Stammzellen, myeloische Malignität