Clear Sky Science · nl
Extramedullaire hematopoëtische niches ondersteunen het ontstaan en de progressie van myeloïde maligniteit in de muriene milt
Waarom de milt ertoe doet bij bloedkanker
Als we nadenken over waar bloed wordt aangemaakt, denken we meestal aan het beenmerg. Toch ontwikkelen veel patiënten met bloedkankers zoals leukemie ook vergrote milten, en artsen hebben lang opgemerkt dat dit kan duiden op ernstiger ziekte. Deze studie bij muizen stelt een bedrieglijk eenvoudige vraag met grote implicaties: kan de milt zelf een soort „broeikas” worden die gevaarlijke bloedcellen helpt groeien en zich verspreiden? Door te achterhalen hoe een specifieke groep miltcellen deze verborgen omgeving vormt, suggereert het werk nieuwe manieren om de ontwikkeling van myeloïde bloedkankers te vertragen of om te buigen.
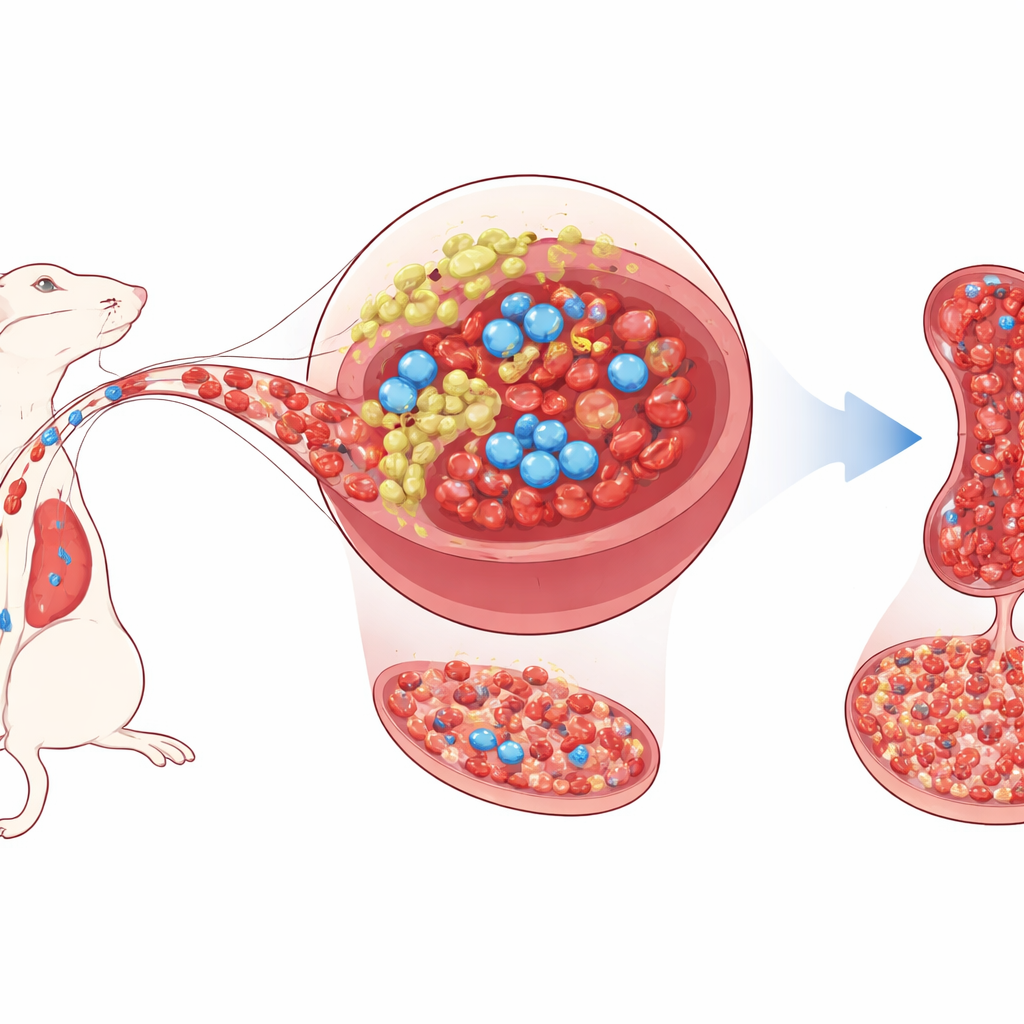
Een tweede thuis voor bloedvormende cellen
Gezonde bloedvormende stamcellen leven gewoonlijk diep in het beenmerg, waar naburige steuncellen hen van groeisignalen voorzien en hun gedrag reguleren. De milt, vooral bekend om het filteren van bloed en het bestrijden van infecties, kan onder stress ook als reserve voor bloedproductie inspringen — een proces dat extramedullaire hematopoëse heet. De auteurs richten zich op een kleine populatie steuncellen in de milt van muizen — mesenchymale stromale/progenitorcellen — die het gen Tlx1 dragen. Bij volwassen muizen komt Tlx1 bijna uitsluitend in deze miltcellen voor. Eerder werk toonde aan dat sterkere activering van Tlx1 stamcellen uit het beenmerg naar de milt mobiliseert en daar extra bloedproductie op gang brengt.
Hoe één schakelaar de milt herbedraad
Om te begrijpen hoe deze Tlx1-dragende cellen de bloedvorming beïnvloeden, hebben de onderzoekers eerst het steun-niche van de milt in een schaaltje nagebouwd. Ze waren de miltstromale cellen zodanig genetisch gewijzigd dat het toevoegen van een geneesmiddel Tlx1 zou verhogen. Toen normale bloedstam- en progenitorcellen bovenop deze „aangeschakelde” miltcellen werden gekweekt, vermenigvuldigden de bloedcellen zich sterker en gingen er minder dood, vergeleken met kweek op ongewijzigde miltcellen of op niet-verwante fibroblasten. De Tlx1-rijke stromale cellen produceerden ook meer van verschillende sleutelfactoren die bekendstaan om stamcellen te voeden. Met andere woorden: het verhogen van Tlx1 zette miltsteuncellen om in een krachtige kraamkamer die onrijpe bloedcellen uitbreidt.
Wanneer de milt een toevluchtsoord voor leukemie wordt
Het team vroeg zich vervolgens af wat er gebeurt tijdens acute myeloïde leukemie, een snelgroeiende kanker van myeloïde bloedcellen. Met behulp van een goed gevestigde muizenleukemielijn transplanteerden ze kankercellen in dieren en volgden hoe organen in de loop van de tijd veranderden. Naarmate de leukemie vorderde, vergrootte de milt en verhoogden de Tlx1-positieve stromale cellen daarin Tlx1 en de moleculen die stamcellen ondersteunen. Microscopen toonden dat leukemiecellen zich vestigden in nauwe aanhechting bij Tlx1-rijke niches in de rode pulparegio’s van de milt. Het verwijderen van de milt vertraagde het verschijnen van leukemiecellen in de bloedbaan en verlengde de overleving licht, wat suggereert dat dit orgaan actief bijdraagt aan het voeden van de ziekte.
De niche harder of zachter zetten
Om oorzaak en gevolg directer te testen, creëerden de auteurs twee typen genetisch gewijzigde muizen. In het ene model konden ze Tlx1 in miltstromale cellen kunstmatig overactiveren, waarmee ze de extramedullaire bloedvormende niche overdrijven. In deze muizen homden getransplanteerde leukemiecellen veel gemakkelijker naar de milt en stapelden zich daar op, kwamen eerder in het bloed terecht en verkortten de overleving vergeleken met normale nestgenoten. In het tweede model konden ze Tlx1 specifiek uit miltstromale cellen verwijderen. Hier slaagden leukemiecellen er nauwelijks in om zich in de milt te vestigen, hoewel het beenmerg nog steeds sterk geïnfiltreerd raakte en de totale overleving niet dramatisch verbeterde. Deze experimenten tonen aan dat Tlx1-gedreven miltniches cruciale aanlegplaatsen voor leukemie zijn, maar niet de enige locaties die de ziekte in stand houden.
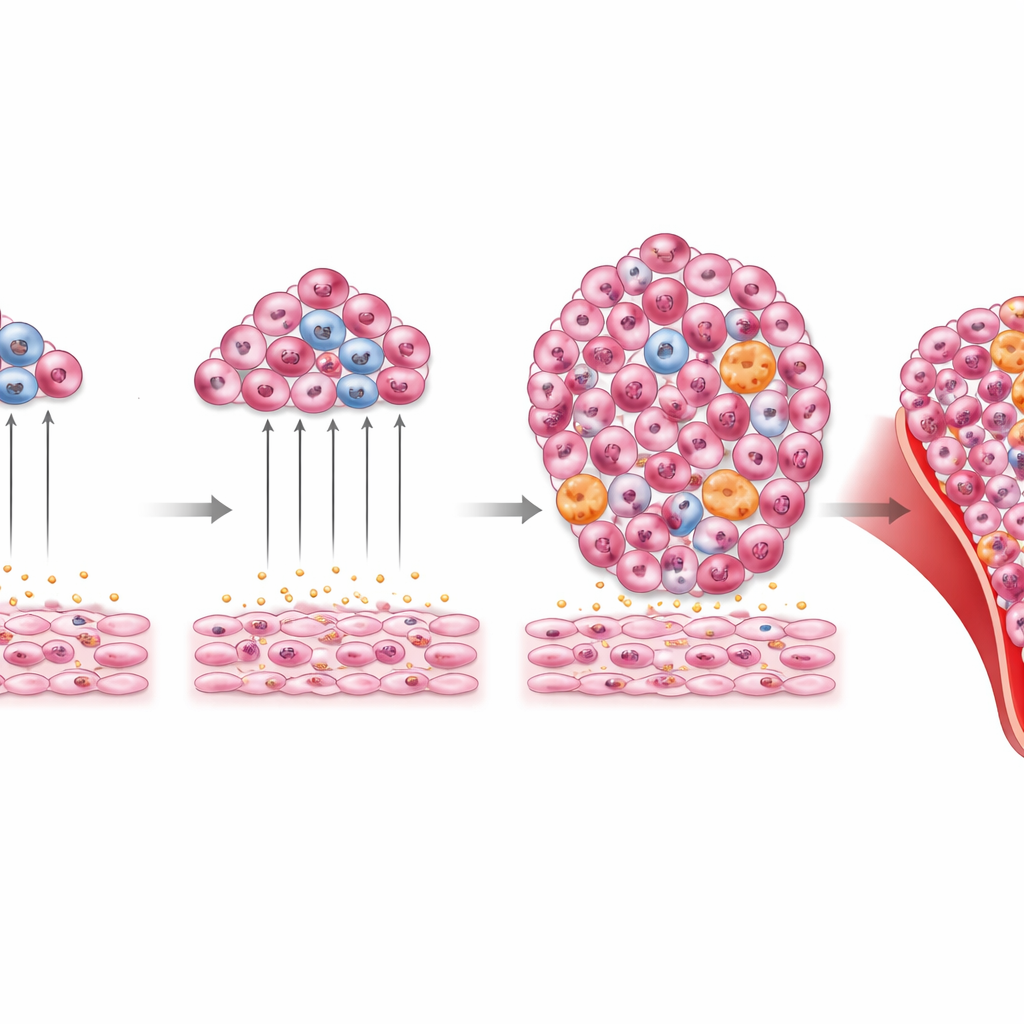
Wanneer reservebloedproductie doorschiet
Het verhaal eindigt niet bij kortdurende leukemiegroei. De onderzoekers bekeken ook wat er gebeurt wanneer Tlx1 langdurig hoog blijft in miltstromale cellen, zelfs zonder injectie van leukemiecellen. Muizen met chronische Tlx1-overexpressie ontwikkelden grote milten, bloedarmoede, teveel witte bloedcellen en vervormd beenmerg vol met myeloïde cellen en hun voorlopers. Hun lever raakte geïnfiltreerd door deze cellen en bloeduitstrijken toonden abnormale, onrijpe vormen. Belangrijk is dat, wanneer beenmerg- of miltcellen van deze dieren werden getransplanteerd naar nieuwe ontvangers, die ontvangers soortgelijke myeloïde afwijkingen ontwikkelden. Dit wijst erop dat de langdurige, Tlx1-gedreven miltniche kan helpen bij het genereren of in stand houden van ongezonde myeloïde celpopulaties die zich gedragen als een myeloïde maligniteit.
Wat dit betekent voor patiënten
Alles bij elkaar schildert het werk de milt niet als een passieve toeschouwer, maar als een actieve partner bij bepaalde bloedkankers. Door de Tlx1-schakelaar om te zetten in een gespecialiseerde groep steuncellen kan de milt zowel normale als kwaadaardige voorlopers rekruteren, hun groei stimuleren en na verloop van tijd de opkomst van afwijkende myeloïde cellen bevorderen. Voor patiënten suggereert dit dat therapieën gericht op het hervormen of dempen van de miltelijke, leukemievriendelijke niche — in plaats van het orgaan simpelweg te verwijderen — op termijn bestaande behandelingen zouden kunnen aanvullen. Hoewel mensen ingewikkelder zijn dan muizen en er nog veel vragen onbeantwoord blijven, benadrukt de studie hoe de plekken waar kankercellen verblijven even belangrijke doelwitten kunnen zijn als de kankercellen zelf.
Bronvermelding: Oda, A., Tezuka, T., Nakamura, T. et al. Extramedullary hematopoietic niches support the initiation and progression of myeloid malignancy in the murine spleen. Sci Rep 16, 11211 (2026). https://doi.org/10.1038/s41598-026-41461-y
Trefwoorden: acute myeloïde leukemie, milt-niche, extramedullaire hematopoëse, hematopoëtische stamcellen, myeloïde maligniteit