Clear Sky Science · pt
Nichos hematopoiéticos extramedulares sustentam a iniciação e progressão de malignidade mieloide no baço de camundongos
Por que o Baço Importa no Câncer de Sangue
Quando pensamos em onde o sangue é produzido, a medula óssea geralmente vem à mente. Ainda assim, muitos pacientes com cânceres do sangue, como a leucemia, desenvolvem esplenomegalia, e os médicos há muito observam que isso pode sinalizar doença mais grave. Este estudo em camundongos faz uma pergunta aparentemente simples, com grandes implicações: o próprio baço pode se tornar uma espécie de “estufa” que ajuda células sanguíneas perigosas a crescer e se espalhar? Ao revelar como um grupo específico de células esplênicas molda esse ambiente oculto, o trabalho sugere novas maneiras de desacelerar ou redirecionar o curso dos cânceres mieloides.
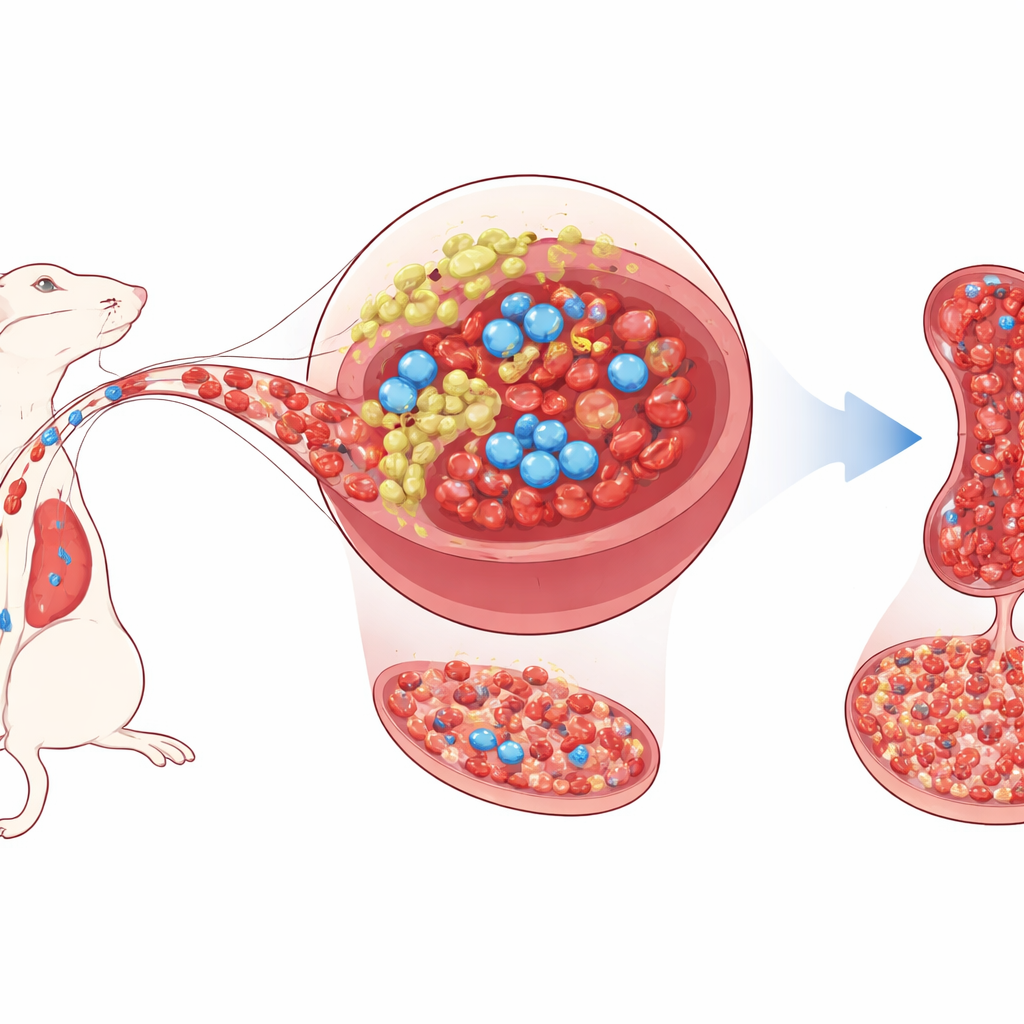
Um Segundo Lar para Células Formadoras de Sangue
Células-tronco hematopoéticas saudáveis normalmente vivem no interior da medula óssea, onde células de suporte vizinhas as nutrem com sinais de crescimento e regulam seu comportamento. O baço, mais conhecido por filtrar o sangue e combater infecções, também pode ativar a produção de sangue de reserva sob estresse, um processo chamado hematopoiese extramedular. Os autores focam em uma pequena população de células de suporte no baço de camundongo — células estromais/progenitoras mesenquimais — que expressam um gene chamado Tlx1. Em camundongos adultos, Tlx1 é encontrado quase exclusivamente nessas células esplênicas. Trabalhos anteriores mostraram que ativar Tlx1 de forma mais intensa mobiliza células-tronco da medula óssea para o baço e inicia a produção extra de sangue lá.
Como um Único Interruptor Reconfigura o Baço
Para entender como essas células portadoras de Tlx1 influenciam a formação do sangue, os pesquisadores primeiro recriaram o nicho de suporte esplênico em cultura. Eles modificaram geneticamente células estromais esplênicas para que a adição de um fármaco aumentasse Tlx1. Quando células-tronco e progenitoras sanguíneas normais foram cultivadas sobre essas células esplênicas “ativadas”, as células sanguíneas se multiplicaram mais e morreram menos, em comparação com culturas sobre células esplênicas não alteradas ou fibroblastos não relacionados. As células estromais com alto Tlx1 também produziram mais de vários fatores de crescimento-chave conhecidos por nutrir células-tronco. Em outras palavras, elevar Tlx1 converteu células de suporte esplênicas em um berço poderoso que expande células sanguíneas imaturas.
Quando o Baço se Torna um Refúgio para a Leucemia
Em seguida, a equipe perguntou o que acontece durante a leucemia mieloide aguda, um câncer de crescimento rápido das células mieloides do sangue. Usando uma linhagem de células leucêmicas de camundongo bem estabelecida, transplantaram células cancerosas em animais e observaram como os órgãos mudavam ao longo do tempo. À medida que a leucemia progredia, o baço aumentou de tamanho e suas células estromais Tlx1-positivas aumentaram a expressão de Tlx1 e de moléculas que sustentam células-tronco. A microscopia mostrou células leucêmicas se alojando em contato próximo com nichos ricos em Tlx1 nas regiões do polpa vermelha do baço. A remoção do baço retardou o aparecimento de células leucêmicas na corrente sanguínea e estendeu modestamente a sobrevida, sugerindo que esse órgão ajuda ativamente a alimentar a doença.
Aumentando ou Diminuindo o Nicho
Para testar causa e efeito mais diretamente, os autores criaram dois tipos de camundongos geneticamente alterados. Em um modelo, podiam hiperativar artificialmente Tlx1 nas células estromais esplênicas, exagerando o nicho de hematopoiese extramedular. Nesses camundongos, células leucêmicas transplantadas migraram e se acumularam no baço com muito mais facilidade, dominaram o sangue mais cedo e reduziram a sobrevida em comparação com animais normais. No segundo modelo, puderam deletar Tlx1 especificamente nas células estromais esplênicas. Aqui, as células leucêmicas mal conseguiram se estabelecer no baço, embora a medula óssea ainda ficasse fortemente infiltrada e a sobrevida geral não tenha melhorado dramaticamente. Esses experimentos revelam que nichos esplênicos dirigidos por Tlx1 são estações de ancoragem cruciais para a leucemia, mas não são os únicos locais que sustentam a doença.
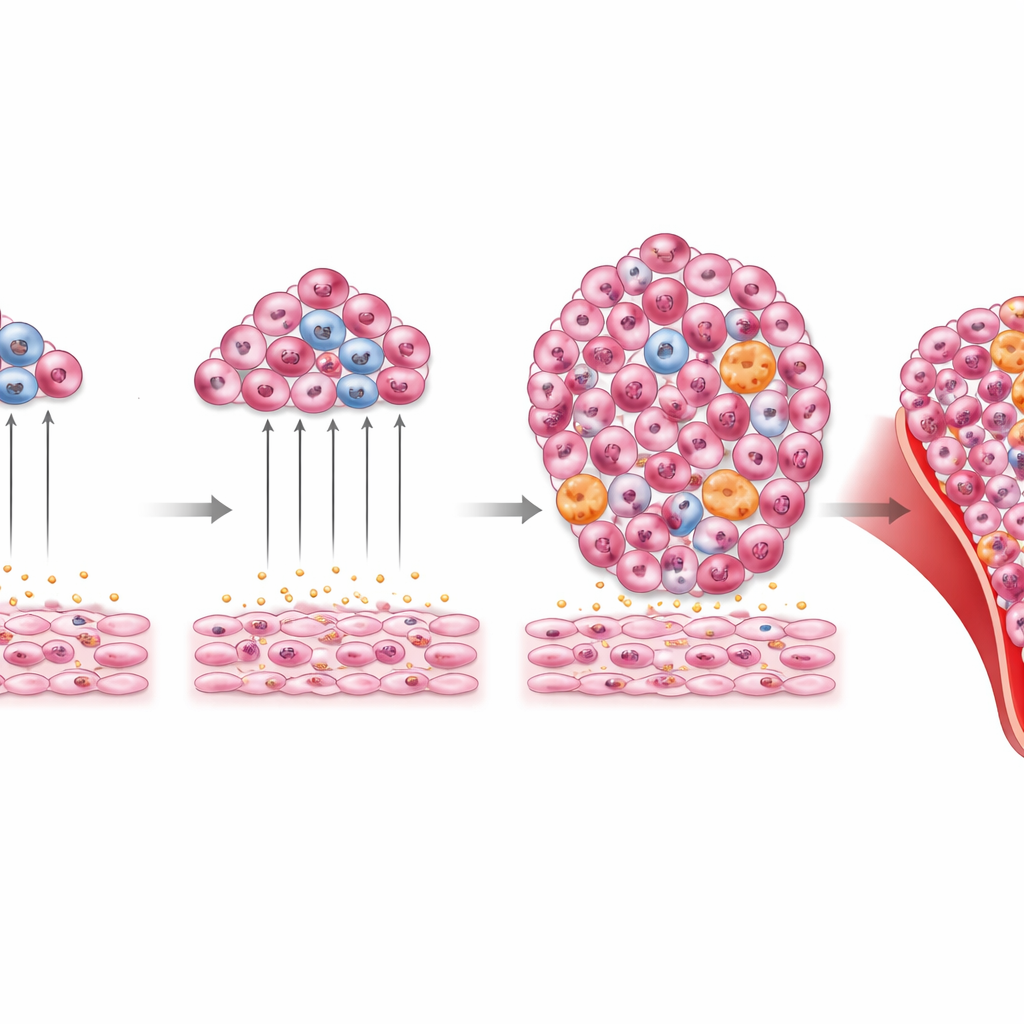
Quando a Produção de Sangue de Reserva Vai Longe Demais
A história não termina com o crescimento leucêmico de curto prazo. Os pesquisadores também examinaram o que acontece quando Tlx1 permanece elevado nas células estromais esplênicas por muitos meses, mesmo sem injeção de células leucêmicas. Camundongos com superexpressão crônica de Tlx1 desenvolveram baços grandes, anemia, excesso de leucócitos e medulas ósseas distorcidas, repletas de células mieloides e seus precursores. Seus fígados ficaram infiltrados por essas células, e esfregaços sanguíneos mostraram formas anormais e imaturas. Importante, quando células da medula óssea ou do baço desses animais foram transplantadas em novos recipientes, os receptores desenvolveram anomalias mieloides semelhantes. Isso indica que o nicho esplênico duradouro, dirigido por Tlx1, pode ajudar a gerar ou manter populações mieloides doentes que se comportam como uma malignidade mieloide.
O que Isso Significa para Pacientes
No conjunto, o trabalho pinta o baço não como um espectador passivo, mas como um parceiro ativo em certos cânceres do sangue. Ao virar o interruptor Tlx1 em um grupo especializado de células de suporte, o baço pode recrutar precursores normais e malignos, impulsionar seu crescimento e, com o tempo, favorecer a emergência de células mieloides anormais. Para pacientes, isso sugere que terapias destinadas a remodelar ou atenuar o nicho esplênico favorável à leucemia — em vez de remover o órgão por completo — poderiam um dia complementar os tratamentos existentes. Embora humanos sejam mais complexos que camundongos e muitas perguntas permaneçam, o estudo destaca como os locais onde as células cancerosas vivem podem ser um alvo tão importante quanto as próprias células cancerosas.
Citação: Oda, A., Tezuka, T., Nakamura, T. et al. Extramedullary hematopoietic niches support the initiation and progression of myeloid malignancy in the murine spleen. Sci Rep 16, 11211 (2026). https://doi.org/10.1038/s41598-026-41461-y
Palavras-chave: leucemia mieloide aguda, nicho esplênico, hematopoiese extramedular, células-tronco hematopoéticas, malignidade mieloide