Clear Sky Science · fr
Les niches hématopoïétiques extramédullaires favorisent l’initiation et la progression des maladies myéloïdes dans la rate murine
Pourquoi la rate compte dans les cancers du sang
Quand on pense à la fabrication du sang, la moelle osseuse vient généralement à l’esprit. Pourtant, de nombreux patients atteints de cancers du sang tels que la leucémie développent aussi une splénomégalie, et les cliniciens observent depuis longtemps que cela peut indiquer une maladie plus sévère. Cette étude chez la souris pose une question apparemment simple mais lourde de conséquences : la rate peut‑elle elle‑même devenir une sorte de « serre » qui aide des cellules sanguines dangereuses à croître et à se disséminer ? En révélant comment un groupe précis de cellules spléniques façonne cet environnement caché, le travail suggère de nouvelles façons de ralentir ou de détourner l’évolution des cancers myéloïdes.
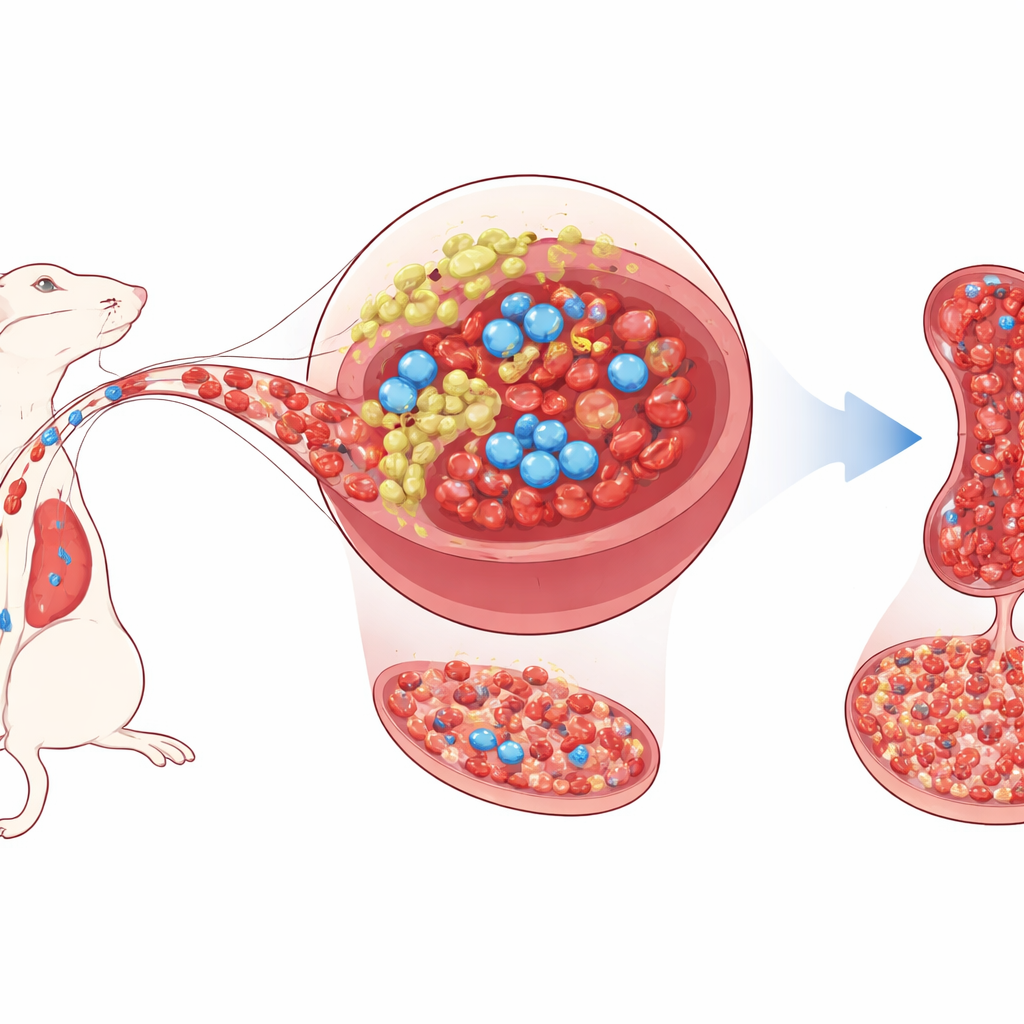
Une seconde demeure pour les cellules hématopoïétiques
Les cellules souches hématopoïétiques saines vivent habituellement profondément dans la moelle osseuse, où des cellules de soutien voisines leur fournissent des signaux de croissance et régulent leur comportement. La rate, surtout connue pour filtrer le sang et lutter contre les infections, peut aussi activer une production de sang de secours en cas de stress, un processus appelé hématopoïèse extramédullaire. Les auteurs se concentrent sur une petite population de cellules stromales/progéitrices mésenchymateuses dans la rate de souris qui portent un gène nommé Tlx1. Chez l’adulte, Tlx1 se trouve presque exclusivement dans ces cellules spléniques. Des travaux antérieurs montraient que l’activation accrue de Tlx1 mobilise les cellules souches hors de la moelle vers la rate et déclenche une production sanguine supplémentaire sur place.
Comment un seul commutateur reprogramme la rate
Pour comprendre comment ces cellules porteuses de Tlx1 influencent la formation du sang, les chercheurs ont d’abord recréé la niche de soutien splénique en culture. Ils ont modifié génétiquement des cellules stromales spléniques pour que l’ajout d’un médicament augmente l’expression de Tlx1. Lorsque des cellules souches et progénitrices sanguines normales ont été cultivées au contact de ces cellules spléniques « activées », les cellules sanguines ont proliféré davantage et sont mortes moins souvent, comparé à des cultures sur des cellules spléniques non modifiées ou sur des fibroblastes non apparentés. Les cellules stromales à forte expression de Tlx1 produisaient aussi davantage de plusieurs facteurs de croissance connus pour nourrir les cellules souches. En d’autres termes, l’augmentation de Tlx1 convertissait les cellules de soutien splénique en un puissant berceau qui amplifie les cellules sanguines immatures.
Quand la rate devient un refuge pour la leucémie
L’équipe a ensuite examiné ce qui se passe lors d’une leucémie myéloïde aiguë, un cancer à croissance rapide des lignées myéloïdes. En utilisant une lignée cellulaire leucémique murine bien établie, ils ont transplanté des cellules cancéreuses chez des animaux et observé l’évolution des organes au fil du temps. À mesure que la leucémie progressait, la rate s’agrandissait et ses cellules stromales Tlx1‑positives augmentaient leur expression de Tlx1 et de molécules soutenant les cellules souches. La microscopie a montré des cellules leucémiques s’installant en contact étroit avec des niches riches en Tlx1 dans les régions de la pulpe rouge de la rate. L’ablation de la rate retardait l’apparition de cellules leucémiques dans la circulation et prolongeait modestement la survie, ce qui suggère que cet organe contribue activement à alimenter la maladie.
Augmenter ou réduire la niche
Pour tester la relation de cause à effet de façon plus directe, les auteurs ont créé deux types de souris génétiquement modifiées. Dans l’une, ils pouvaient suractiver artificiellement Tlx1 dans les cellules stromales spléniques, exagérant ainsi la niche d’hématopoïèse extramédullaire. Chez ces animaux, les cellules leucémiques transplantées se dirigeaient vers la rate et s’y accumulaient beaucoup plus facilement, se déversaient plus tôt dans le sang et réduisaient la survie comparé aux congénères normaux. Dans le second modèle, ils pouvaient supprimer spécifiquement Tlx1 dans les cellules stromales spléniques. Là, les cellules leucémiques peinaient à s’implanter dans la rate, bien que la moelle osseuse devienne toujours fortement infiltrée et que la survie globale ne s’améliore pas de façon spectaculaire. Ces expériences montrent que les niches spléniques contrôlées par Tlx1 sont des stations d’amarrage cruciales pour la leucémie, mais qu’elles ne sont pas les seuls sites qui soutiennent la maladie.
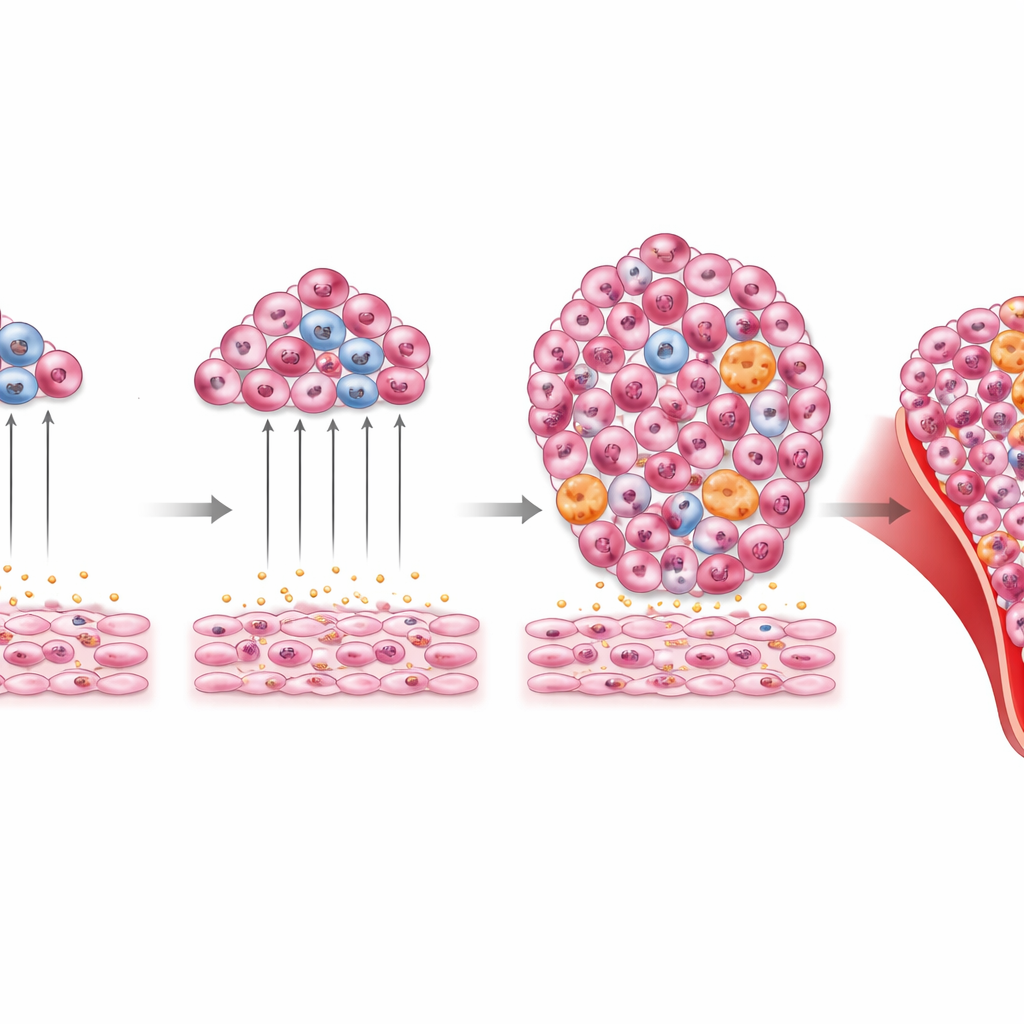
Quand la production de secours dépasse les bornes
L’histoire ne s’arrête pas à la croissance leucémique à court terme. Les chercheurs ont aussi examiné ce qui arrive lorsque Tlx1 reste élevé dans les cellules stromales spléniques pendant de longs mois, même sans injection de cellules leucémiques. Les souris avec une surexpression chronique de Tlx1 développaient de grosses rates, une anémie, un excès de globules blancs et une moelle osseuse déformée, remplie de cellules myéloïdes et de leurs précurseurs. Leurs foies étaient infiltrés par ces cellules, et les frottis sanguins révélaient des formes immatures et anormales. Fait important, lorsque des cellules de moelle osseuse ou de rate de ces animaux étaient transplantées chez de nouveaux receveurs, ces derniers développaient des anomalies myéloïdes similaires. Cela indique que la niche splénique durable et dirigée par Tlx1 peut contribuer à générer ou à maintenir des populations cellulaires myéloïdes pathologiques qui se comportent comme une malignité myéloïde.
Ce que cela signifie pour les patients
Dans l’ensemble, ce travail dépeint la rate non pas comme un simple spectateur, mais comme une partenaire active dans certains cancers du sang. En activant le commutateur Tlx1 dans un groupe spécialisé de cellules de soutien, la rate peut recruter des précurseurs normaux et malins, stimuler leur croissance et, avec le temps, favoriser l’émergence de cellules myéloïdes anormales. Pour les patients, cela suggère que des thérapies visant à remodeler ou atténuer la niche splénique favorable à la leucémie — plutôt que d’ôter l’organe purement et simplement — pourraient un jour compléter les traitements existants. Si les humains sont plus complexes que les souris et que de nombreuses questions demeurent, l’étude met en lumière que les lieux où vivent les cellules cancéreuses peuvent être des cibles aussi importantes que les cellules elles‑mêmes.
Citation: Oda, A., Tezuka, T., Nakamura, T. et al. Extramedullary hematopoietic niches support the initiation and progression of myeloid malignancy in the murine spleen. Sci Rep 16, 11211 (2026). https://doi.org/10.1038/s41598-026-41461-y
Mots-clés: leucémie myéloïde aiguë, niche splénique, hématopoïèse extramédullaire, cellules souches hématopoïétiques, malignité myéloïde