Clear Sky Science · ru
Хроническая адаптивная глубинная стимуляция головного мозга при болезни Паркинсона: выводы ADAPT-START и принципы программирования
Почему важны «умные» импульсы для мозга
Для многих людей с болезнью Паркинсона крошечные электрические импульсы, подаваемые глубоко в мозг, значительно облегчают скованность и тремор. Тем не менее эта терапия, называемая глубинной стимуляцией мозга, по-прежнему в определённой степени грубый инструмент: ток обычно остаётся постоянным в течение всего дня, хотя симптомы и активность мозга меняются от часа к часу. В этом исследовании описывается более гибкая, «адаптивная» форма стимуляции, которая в реальном времени отслеживает сигналы мозга и автоматически регулирует интенсивность импульсов. Авторы рассказывают, как они внедрили эту технологию в повседневную клиническую практику и что она уже означала для двигательной функции пациентов, особенно для ходьбы.
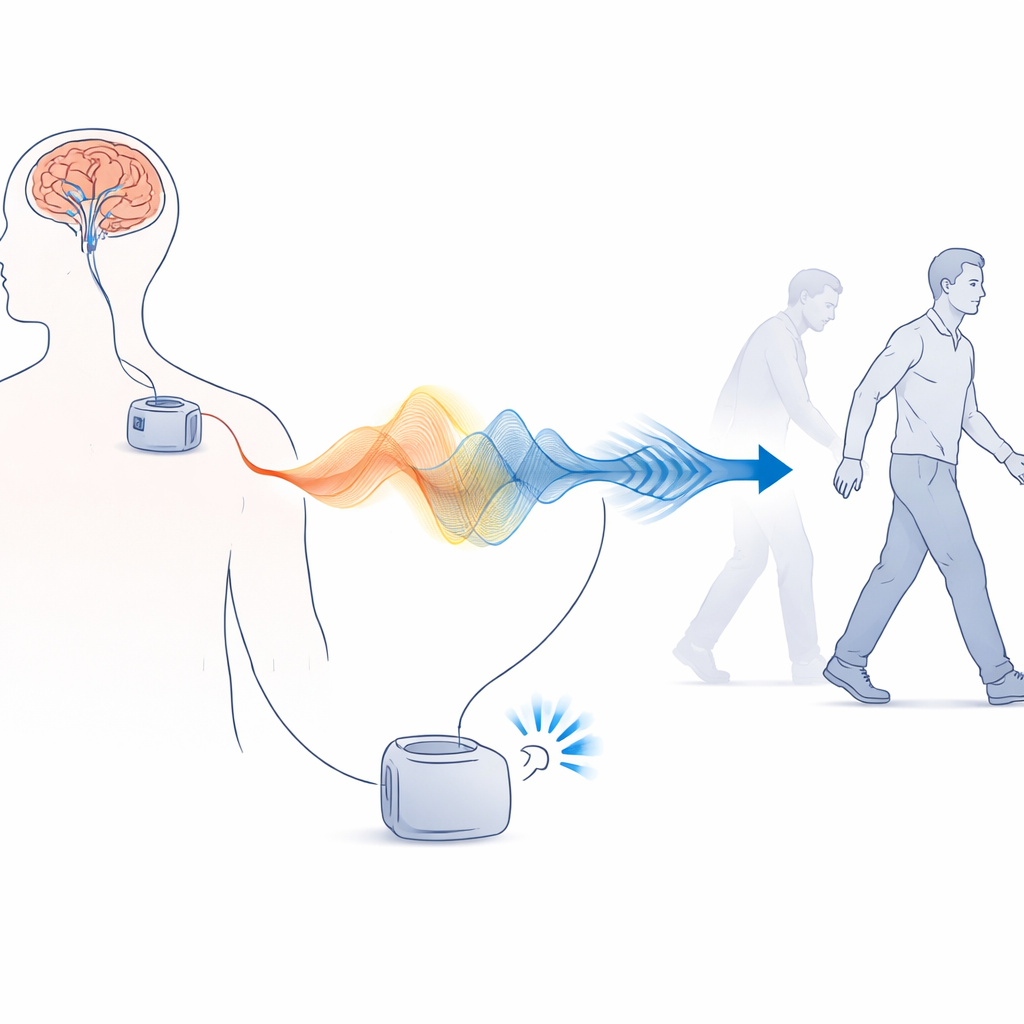
От постоянного включения к «как раз» стимулю
Традиционная глубинная стимуляция работает как оставленный включённым свет на фиксированной яркости. Электроды, размещённые в небольшой области — субталамическом ядре, подключены к импланту, похожему на кардиостимулятор в области грудной клетки, который непрерывно отправляет электрические импульсы по заранее заданным параметрам. Этот метод может значительно улучшать тремор и скованность, но некоторые симптомы, особенно нарушения равновесия и ходьбы, часто остаются. Движения пациентов также меняются в зависимости от приёма лекарств, сна и повседневной активности, в то время как стимуляция этого не учитывает. В результате подход «всегда включено» иногда может недолечивать симптомы или вызывать побочные эффекты, такие как непроизвольные движения.
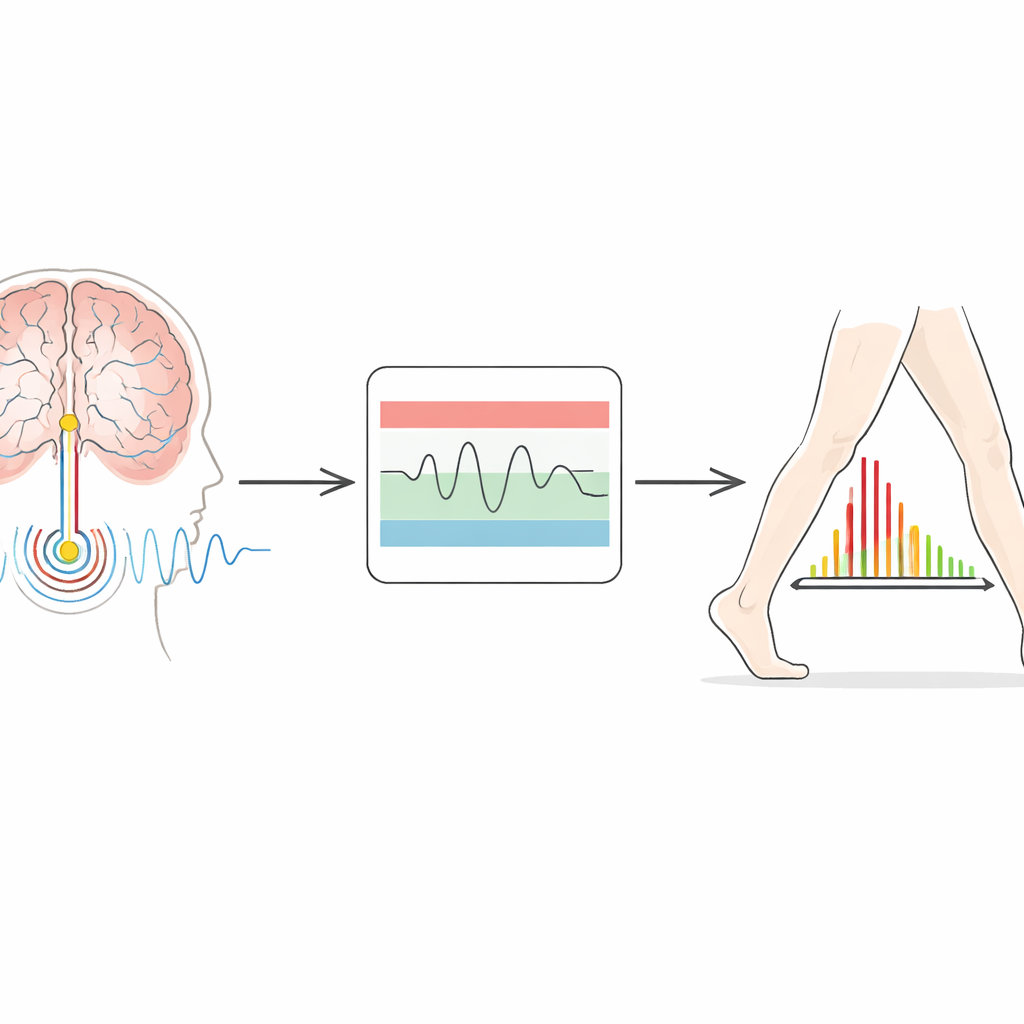
Слушая ритмы мозга
Новые импланты делают не только подачу тока — они также могут записывать местную активность мозга. При болезни Паркинсона определённый ритм, известный как бета-активность, становится сильнее, когда пациенты медленны и скованы, и обычно ослабевает, когда они двигаются свободнее или принимают лекарства. Идея адаптивной стимуляции состоит в использовании этого ритма в качестве ориентира: когда бета-активность растёт, устройство увеличивает ток; когда она падает, стимуляция снижается. Система, испытанная здесь, использует конструкцию с «двойным порогом». Клиницисты задают нижнюю и верхнюю границы допустимой мощности бета-ритма. Если сигнал мозга поднимается выше или опускается ниже этих границ достаточно долго, устройство постепенно увеличивает или снижает стимуляцию в пределах безопасных лимитов, установленных для каждого пациента.
Применение адаптивной стимуляции в реальной жизни
С января по апрель 2025 года команда предложила этот подход с двойным порогом 20 людям с болезнью Паркинсона, у которых уже была традиционная стимуляция с устройством, способным к записи сигналов. Не все могли перейти на новый режим: у нескольких пациентов записи были зашумлены, отсутствовал явный бета-ритм или требовались параметры, несовместимые с режимом записи. В итоге девяти пациентам переключили режим на адаптивный, и пятеро прошли по крайней мере один месяц стабильного лечения. Настройка требовала трёх структурированных посещений клиники. Сначала врачи картировали сигналы мозга и текущие параметры стимуляции, затем отправляли пациента домой на несколько дней, пока имплант пассивно записывал бета-активность в обычной жизни. На следующем визите определяли безопасные минимальные и максимальные уровни тока и выбирали пороги бета-активности на основе этих записей. Последующий визит через две недели использовали для тонкой настройки системы, опираясь как на проверку симптомов, так и на данные с нательного датчика движения, который отслеживал ходьбу и периоды хорошего или плохого движения в течение дня.
Что изменилось для пациентов
Через месяц на адаптивной стимуляции пятеро пациентов в среднем показали примерно на 35 процентов большее улучшение по стандартной моторной шкале по сравнению с их ранее оптимизированными конвенциональными настройками, несмотря на то что эти исходные настройки уже хорошо работали. Наиболее явные улучшения касались показателей, связанных с походкой, и опросника, ориентированного на застывание при ходьбе. Нательные датчики показали, что пациенты в среднем проводили более 40 дополнительных минут в день в состоянии хорошего движения без тревожных непроизвольных движений и до 160 минут меньше в плохие «OFF»-периоды. Большинство показателей немоторных симптомов также улучшились умеренно. Интересно, что общий опросник качества жизни иногда ухудшался, хотя пациенты и ухаживающие за ними однозначно предпочитали адаптивный режим. Авторы предполагают, что это может отражать то, что люди стали более активными — и, следовательно, более осведомлёнными о сохраняющихся ограничениях — а не истинное ухудшение.
Проблемы и следующие шаги
Несмотря на обнадёживающие результаты, авторы подчёркивают, что адаптивная стимуляция не является решением «включил и забыл». Только около половины отобранных пациентов могли использовать режим с двойным порогом из‑за технических ограничений, таких как загрязнение сигнала сердечными импульсами или требование определённой конфигурации электродов. Даже для подходящих пациентов часто требовались повторные визиты, чтобы найти стабильный ритм для отслеживания и настроить пороги так, чтобы стимуляция действительно адаптировалась, а не работала как простой двухуровневый переключатель. В среднем адаптивная терапия потребляла немного больше электрической энергии, чем конвенциональная, но не постоянно; ток повышался главным образом в периоды, когда симптомы, вероятно, были хуже. Будущие улучшения, такие как продвинутые методы обработки сигналов, более точные биомаркеры для разных симптомов и возможность удалённой тонкой настройки, могут сделать этот подход более широкодоступным и менее обременительным.
Что это значит для людей с болезнью Паркинсона
Этот ранний опыт показывает, что имплант, который «слушает и отвечает», может давать дополнительные преимущества по сравнению с сегодняшними стимуляторами с постоянным выходом, особенно для ходьбы и суточных колебаний движения. Практически адаптивная стимуляция позволила многим пациентам проводить большую часть дня в хорошем состоянии движения без заметных побочных эффектов и в целом рекомендовалась чаще, чем старый подход. В то же время метод в текущем виде требует тщательного отбора пациентов, детальной настройки и постоянной корректировки специалистами. По мере развития технологий и алгоритмов адаптивная глубинная стимуляция может стать более персонализированной, отзывчивой терапией, которая следует потребностям мозга в реальном времени, а не заставляет пациентов подстраиваться под фиксированный режим стимуляции.
Цитирование: Cascino, S., Luiso, F., Caffi, L. et al. Chronic adaptive deep brain stimulation in Parkinson’s disease: ADAPT-START findings and programming principles. npj Parkinsons Dis. 12, 85 (2026). https://doi.org/10.1038/s41531-026-01269-z
Ключевые слова: Болезнь Паркинсона, глубокая стимуляция мозга, адаптивная нейромодуляция, снятие сигналов мозга, ходьба и движение