Clear Sky Science · pl
Przewlekła adaptacyjna stymulacja głęboka w chorobie Parkinsona: wyniki ADAPT-START i zasady programowania
Dlaczego ważne są mądrzejsze impulsy mózgowe
Dla wielu osób z chorobą Parkinsona drobne impulsy elektryczne dostarczane głęboko do mózgu mogą znacząco złagodzić sztywność i drżenie. Jednak to leczenie, zwane głęboką stymulacją mózgu, wciąż bywa narzędziem dość nieprecyzyjnym: natężenie prądu zwykle pozostaje stałe przez cały dzień, mimo że objawy i aktywność mózgu zmieniają się z godziny na godzinę. Badanie opisuje bardziej elastyczną, „adaptacyjną” formę stymulacji, która nasłuchuje sygnałów mózgowych w czasie rzeczywistym i automatycznie dostosowuje intensywność impulsów. Autorzy opisują, jak wdrożyli tę technologię w codziennej praktyce klinicznej i co do tej pory oznaczała ona dla ruchów pacjentów, zwłaszcza chodzenia.
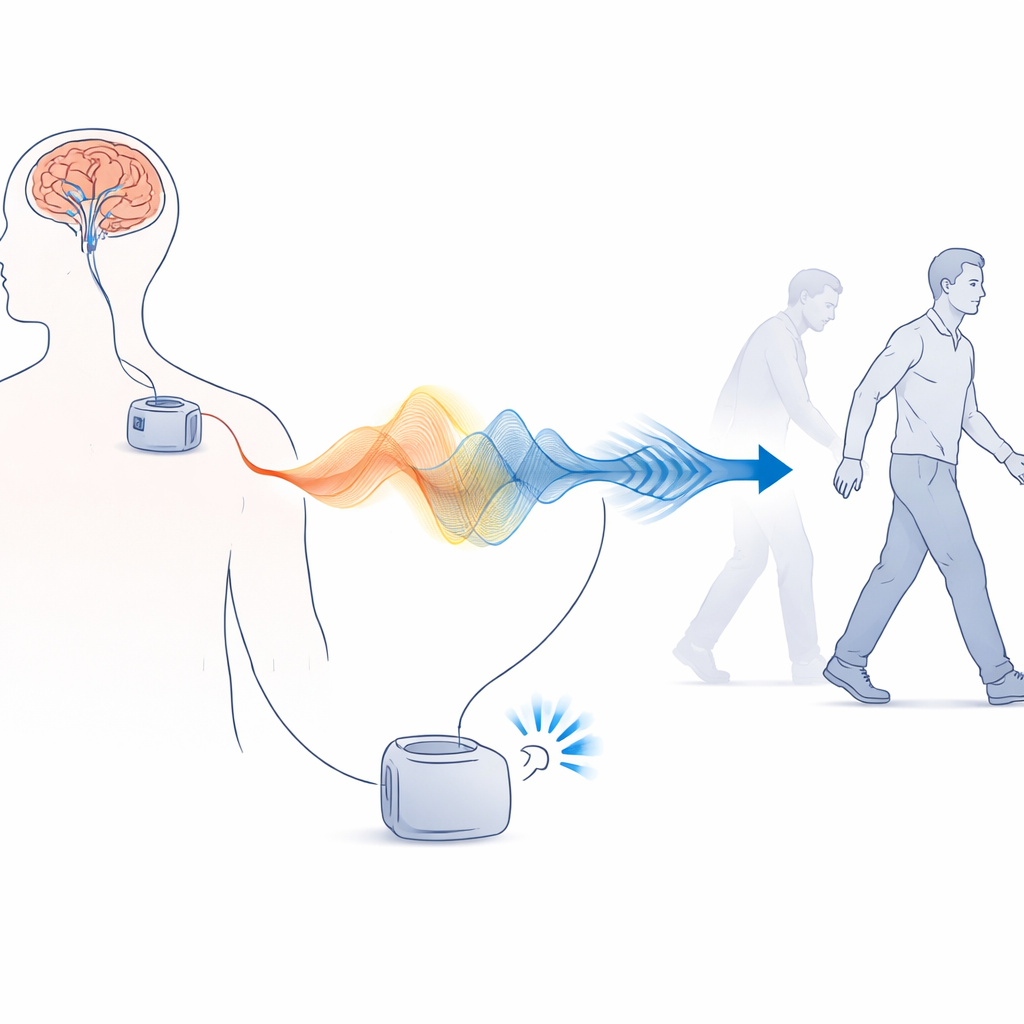
Od stałego włączenia do stymulacji „w sam raz”
Tradycyjna głęboka stymulacja mózgu działa jak światło pozostawione na stałej jasności. Elektrody umieszczone w małym obszarze zwanym jądrem niskowzgórzowym (subthalamic nucleus) są połączone z urządzeniem podobnym do rozrusznika w klatce piersiowej, które nieustannie wysyła impulsy elektryczne według ustawień. Metoda ta może znacznie poprawić drżenie i sztywność, ale niektóre objawy, szczególnie problemy z równowagą i chodzeniem, często utrzymują się. Ruchy pacjentów zmieniają się też w zależności od leków, snu i codziennych aktywności, podczas gdy stymulacja tego nie uwzględnia. W efekcie podejście „zawsze włączone” może czasem niedostatecznie leczyć objawy lub powodować skutki uboczne, takie jak mimowolne ruchy.
Nasłuchiwanie rytmów mózgu
Nowsze implanty robią więcej niż tylko wysyłają prąd — potrafią też rejestrować lokalną aktywność mózgu. W chorobie Parkinsona pewien rytm znany jako aktywność beta wzmacnia się, gdy pacjenci są spowolniali i sztywni, i zwykle słabnie, gdy poruszają się swobodniej lub przyjmują leki. Idea adaptacyjnej stymulacji polega na użyciu tego rytmu jako wskazówki: gdy aktywność beta rośnie, urządzenie zwiększa natężenie; gdy maleje, urządzenie je obniża. Testowany system wykorzystuje konstrukcję z „podwójnym progiem”. Klinicyści definiują dolny i górny zakres dopuszczalnej mocy beta. Jeśli sygnał mózgowy przekroczy lub spadnie poniżej tych zakresów przez wystarczająco długi czas, urządzenie stopniowo zwiększa lub zmniejsza stymulację w bezpiecznych granicach ustalonych dla każdego pacjenta.
Wypróbowanie adaptacyjnej stymulacji w życiu codziennym
Między styczniem a kwietniem 2025 roku zespół zaproponował podejście z podwójnym progiem 20 osobom z chorobą Parkinsona, które już miały konwencjonalną stymulację za pomocą urządzenia z funkcją rejestracji sygnału. Nie wszyscy mogli skorzystać z nowego trybu: u kilku pacjentów nagrania były zaszumione, brakowało wyraźnego rytmu beta albo wymagane ustawienia były niezgodne z rejestracją. Ostatecznie dziewięciu pacjentów przeszło na stymulację adaptacyjną, a pięciu zakończyło co najmniej miesiąc stabilnego leczenia. Konfiguracja obejmowała trzy zaplanowane wizyty w klinice. Najpierw lekarze zmapowali sygnały mózgowe i bieżące ustawienia każdego pacjenta, potem wysyłali ich do domu na kilka dni, podczas których implant pasywnie rejestrował aktywność beta w normalnym życiu. Podczas kolejnej wizyty określono bezpieczne minimalne i maksymalne poziomy prądu oraz wybrano progi beta na podstawie tych nagrań. Wizytę kontrolną po dwóch tygodniach wykorzystano do dopracowania systemu, opierając się zarówno na ocenie objawów, jak i danych z nośnego na pasku sensora ruchu, który śledził chód i okresy dobrego lub złego ruchu w ciągu dnia.
Co się zmieniło dla pacjentów
Po miesiącu stosowania adaptacyjnej stymulacji pięciu pacjentów wykazało średnio około 35 procent większą poprawę w standardowym wyniku motorycznym w porównaniu z ich wcześniejszymi, już zoptymalizowanymi ustawieniami konwencjonalnymi, mimo że te oryginalne ustawienia działały dobrze. Najbardziej widoczne korzyści dotyczyły pozycji związanych z chodem oraz kwestionariusza dotyczącego zatrzemywania chodu (freezing of gait). Czujniki noszone sugerowały, że pacjenci spędzali ponad dodatkowe 40 minut dziennie w stanie dobrego ruchu bez uciążliwych mimowolnych ruchów, a do 160 minut mniej dziennie w złych okresach „OFF”. Większość miar objawów niemotorycznych również poprawiła się umiarkowanie. Co ciekawe, ogólny kwestionariusz jakości życia miejscami ulegał pogorszeniu, mimo że pacjenci i opiekunowie wyraźnie preferowali tryb adaptacyjny. Autorzy przypuszczają, że może to odzwierciedlać wzrost aktywności — a więc większą świadomość pozostałych ograniczeń — a nie rzeczywiste pogorszenie.
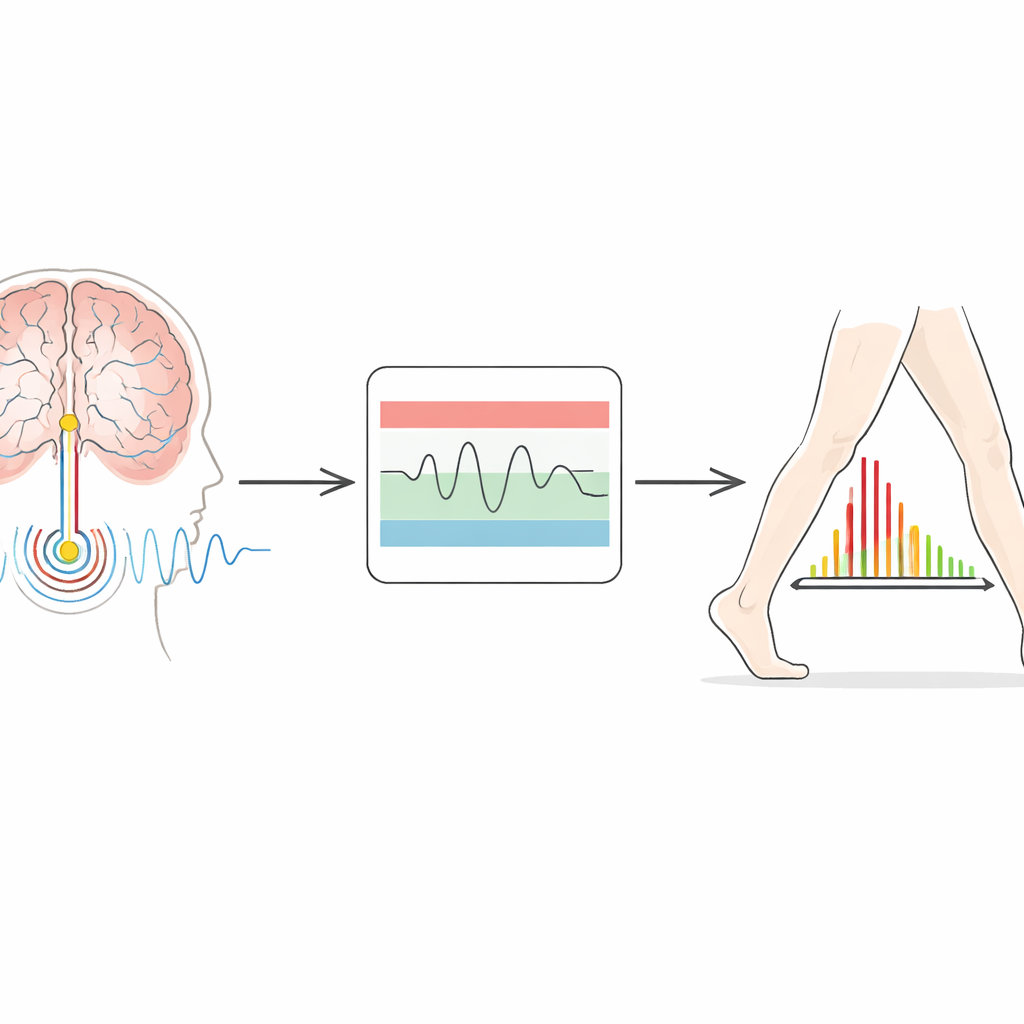
Wyzwania i kolejne kroki
Mimo obiecujących wyników autorzy podkreślają, że adaptacyjna stymulacja nie jest rozwiązaniem typu „podłącz i działaj”. Tylko około połowa badanych pacjentów mogła korzystać z trybu z podwójnym progiem z powodu ograniczeń technicznych, takich jak zanieczyszczenie sygnału od impulsów serca lub potrzeba określonych konfiguracji elektrod. Nawet u kwalifikujących się pacjentów często konieczne były powtarzane wizyty, aby znaleźć stabilny rytm mózgowy do śledzenia i dostosować progi tak, by stymulacja rzeczywiście adaptowała się, zamiast zachowywać się jak prosty dwupoziomowy przełącznik. Średnio terapia adaptacyjna dostarczała nieco więcej energii elektrycznej niż terapia konwencjonalna, ale nie ciągle; natężenie wzrastało przeważnie wtedy, gdy objawy prawdopodobnie się nasilały. Przyszłe ulepszenia, takie jak lepsze przetwarzanie sygnałów, bardziej precyzyjne biomarkery mózgowe dla różnych objawów oraz zdalne dopracowywanie ustawień, mogłyby uczynić to podejście bardziej powszechnym i mniej uciążliwym.
Co to oznacza dla osób z Parkinsonem
To wczesne doświadczenie sugeruje, że implant mózgowy, który „nasłuchuje i reaguje”, może oferować dodatkowe korzyści w porównaniu z dzisiejszymi stymulatorami o stałym wyjściu, szczególnie jeśli chodzi o chodzenie i dobowe wahania ruchu. W praktyce adaptacyjna stymulacja pozwoliła wielu pacjentom spędzać więcej czasu w ciągu dnia poruszając się dobrze, bez zauważalnych dodatkowych skutków ubocznych, i była konsekwentnie preferowana od starszego podejścia. Jednocześnie metoda ta wymaga obecnie starannej selekcji pacjentów, szczegółowej konfiguracji i ciągłego dopasowywania przez specjalistów. W miarę jak technologia i algorytmy dojrzeją, adaptacyjna głęboka stymulacja mózgu może stać się bardziej spersonalizowaną, responsywną terapią, która podąża za potrzebami mózgu w czasie rzeczywistym, zamiast zmuszać pacjentów do dopasowania się do stałego schematu stymulacji.
Cytowanie: Cascino, S., Luiso, F., Caffi, L. et al. Chronic adaptive deep brain stimulation in Parkinson’s disease: ADAPT-START findings and programming principles. npj Parkinsons Dis. 12, 85 (2026). https://doi.org/10.1038/s41531-026-01269-z
Słowa kluczowe: Choroba Parkinsona, głęboka stymulacja mózgu, adaptacyjna neuromodulacja, monitorowanie mózgu, chód i ruch