Clear Sky Science · ru
Реконструкция Sn-катализатора и модуляция микроокружения для эффективного электро-синтеза аминокислот через C–N-спаривание
Превращение отходов в полезные строительные блоки
Аминокислоты — крошечные молекулы, из которых состоят белки — являются необходимыми компонентами для лекарств, кормов для животных и пищевых добавок. Сегодня многие аминокислоты получают с использованием токсичных реагентов и энергоёмких процессов. В этом исследовании рассматривается другой путь: применение электричества и распространённых промышленных потоков отходов для чистого и более эффективного получения глицина — самой простой аминокислоты.
Почему стоит переосмыслить производство аминокислот
Традиционные методы производства аминокислот, такие как процесс Стреккера, зависят от цианида и аммиака, которые связаны с рисками безопасности и климатическими проблемами. Биологические подходы с использованием ферментов или микроорганизмов могут быть мягче, но часто они медленные, дорогостоящие в эксплуатации и ориентированы на узкий круг продуктов. В условиях глобального стремления к «зеленой» химии на возобновляемой электроэнергии растёт интерес к поиску новых способов связывать углеродно- и азотсодержащие строительные блоки в аминокислоты без опасных реагентов и экстремальных условий температуры и давления.
Использование электричества для создания глицина из простых кислот
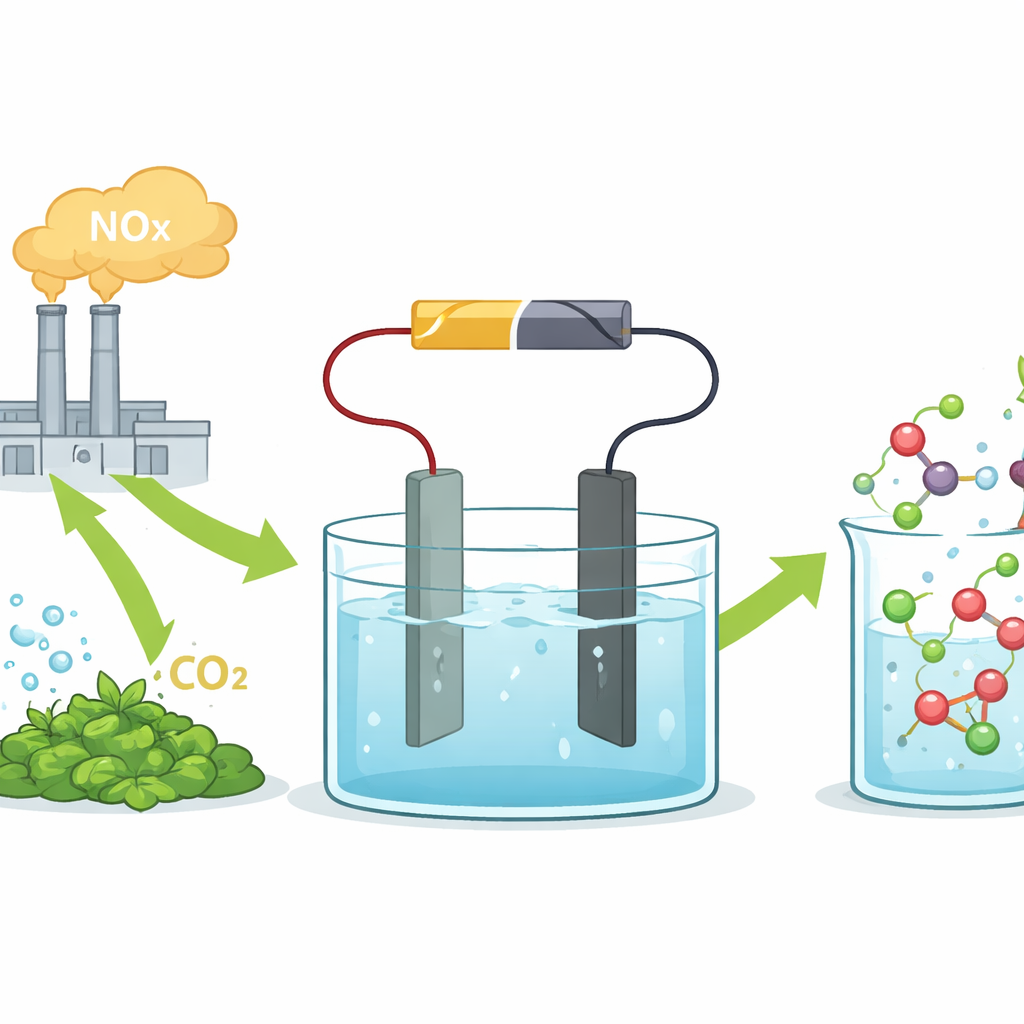
Авторы сосредоточились на электросинтезе, при котором приложенное напряжение приводит к химическим реакциям в жидкой среде. В систему подают азотную кислоту, которую можно получить из промышленных выбросов NOx, и щавелевую кислоту, которую можно синтезировать из углекислого газа или биомассы. В основе установки — электрод на основе олова, который селективно направляет реакцию в сторону глицина, а не побочных продуктов или выделения водорода. В простой лабораторной ячейке этот оловянный катализатор превращает две кислоты в глицин с высокой селективностью и при плотностях тока, близких к промышленным, демонстрируя, что подход не просто лабораторная курьёзность.
Как поверхность катализатора и локальные условия выполняют работу
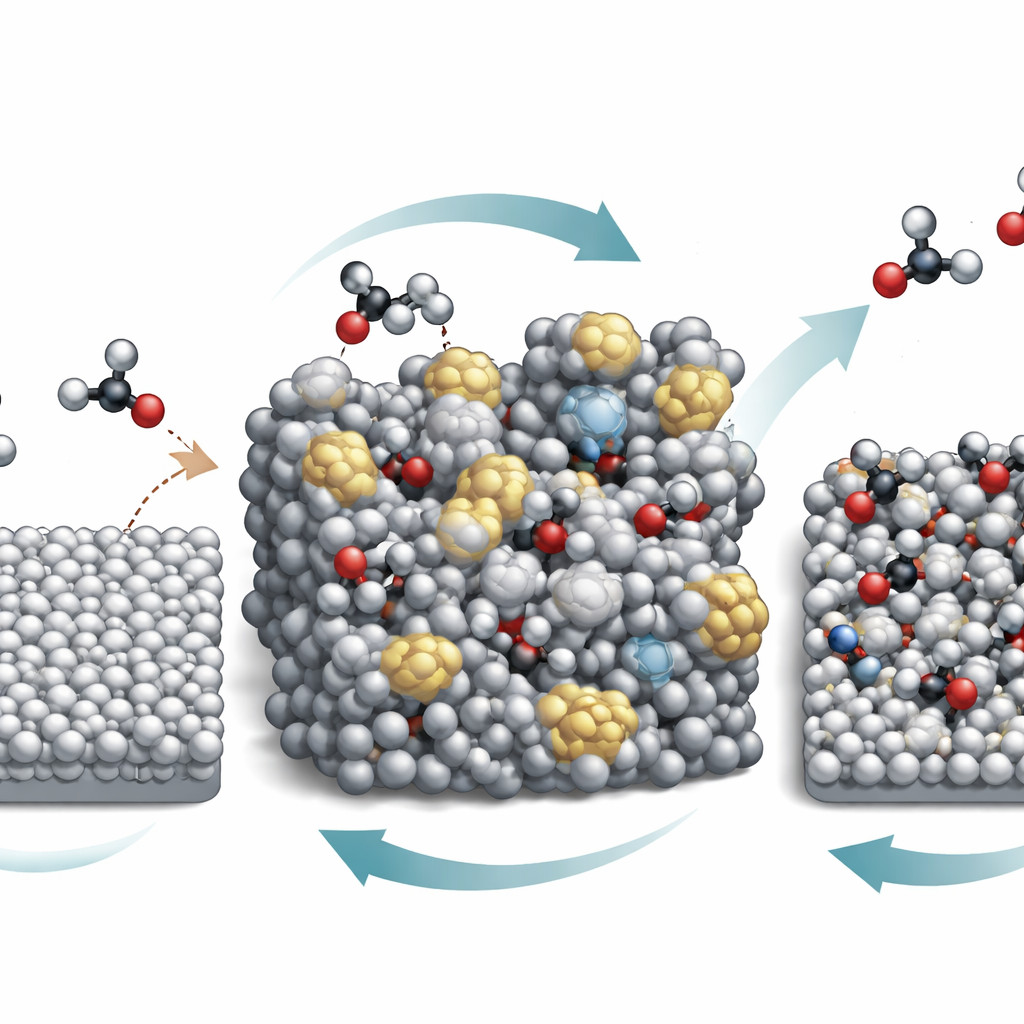
Ключевое наблюдение состоит в том, что поверхность олова не остаётся статичной в процессе работы. В сильно кислой среде олово и азотная кислота проходят некую «дыхательную» цикличность валентности: олово частично окисляется, а затем восстанавливается приложенным напряжением. Это непрерывное чередование постепенно разрушает упорядоченную кристаллическую структуру и формирует аморфную, неупорядоченную поверхность олова. Современные зондирующие методы, включая рентгеновские и колебательные техники, применённые in operando, показывают, что аморфная форма сильнее связывает ключевые углеродно-азотные интермедиаты по сравнению с исходно гладкой поверхностью. Одновременно интенсивная реакция повышает pH непосредственно у электрода, хотя окружающий раствор остаётся сильно кислым, так что слабые кислоты, такие как щавелевая кислота и их производные, возле поверхности существуют в основном в отрицательно заряженной форме.
От медленных цепных реакций к быстрой поверхностной химии
Эти изменения и в катализаторе, и в его микроокружении меняют путь реакции. Сначала интермедиаты, такие как глиоксильная кислота и её оксим, образуются в растворе и затем медленно превращаются в глицин через серию шагов, что даёт скромные выходы. По мере того как олово становится аморфным и локальный pH повышается, отрицательно заряженные интермедиаты сильнее прилипают к поверхности и гидрироватьются прямо на интерфейсе, а не растворяясь в объёме. Авторы показывают, что этот поверхностно-детерминированный путь быстрее и более селективен, доводя долю электрического тока, расходуемого на глицин, выше 90% при работе в специально спроектированном проточном реакторе. Они также демонстрируют, что родственные молекулы, например другие малые кетокислоты, можно превратить в соответствующие аминокислоты, что указывает на широкую применимость стратегии.
Масштабирование до практического производства
Руководствуясь механистическими выводами, команда создала проточный элемент, который непрерывно циркулирует смесь кислот мимо предварительно активированного аморфного оловянного электрода. Настраивая скорость потока и состав питания так, чтобы сохранять благоприятное локальное окружение, они достигают промышленных плотностей тока при высокой селективности по глицину. Поскольку процесс использует только реакционные кислоты и не требует дополнительных поддерживающих солей, конечный продукт можно выделить простым удалением воды, получая практически чистый глицин. Базовый экономический анализ показывает, что при использовании дешёвой электроэнергии этот метод потенциально может производить глицин примерно за половину текущей рыночной стоимости, особенно в сочетании с низкотемпературными плазменными системами, превращающими воздух и воду в азотную кислоту на месте.
Более чистый путь к повседневным молекулам
В целом исследование демонстрирует, что тщательное управление как динамическим состоянием катализатора, так и тонким слоем раствора вокруг него может преобразовать неэффективную реакцию в высокоселективную и масштабируемую. Используя отходы азота и углерода и приводя химию в действие электричеством, авторы наметили путь к более чистому производству аминокислот. Их работа предполагает, что аналогичный контроль реконструкции катализатора и локального pH может открыть возможности для более экологичных синтезов многих других азотсодержащих молекул, лежащих в основе современной жизни.
Цитирование: Han, S., Liu, H., Timoshenko, J. et al. Sn catalyst reconstruction and microenvironment modulation for efficient amino acid electrosynthesis via C–N coupling. Nat Commun 17, 3614 (2026). https://doi.org/10.1038/s41467-026-71694-4
Ключевые слова: электросинтез, зелёная химия, глицин, оловянный катализатор, аминокислоты