Clear Sky Science · es
Reconstrucción del catalizador de Sn y modificación del microambiente para una electrosíntesis eficiente de aminoácidos mediante acoplamiento C–N
Convertir residuos en bloques de construcción útiles
Los aminoácidos, las diminutas moléculas que forman las proteínas, son ingredientes esenciales para medicinas, piensos animales y complementos alimenticios. Hoy en día, muchos aminoácidos se producen mediante rutas que dependen de sustancias químicas tóxicas y procesos que consumen mucha energía. Este estudio explora un camino distinto: usar electricidad y corrientes de desecho industriales comunes para fabricar glicina, el aminoácido más simple, de una forma más limpia y eficiente.
Por qué importa replantear la producción de aminoácidos
Los métodos convencionales para fabricar aminoácidos, como el proceso de Strecker, dependen del cianuro y la amoníaco, ambos con problemas de seguridad y de impacto climático. Las rutas biológicas usando enzimas o microbios pueden ser más suaves, pero con frecuencia son lentas, costosas de operar y están diseñadas para una gama limitada de productos. Con el mundo buscando una química más verde impulsada por electricidad renovable, existe un gran interés en encontrar nuevas formas de unir bloques con carbono y nitrógeno para formar aminoácidos sin reactivos peligrosos ni altas temperaturas y presiones.
Usar electricidad para construir glicina a partir de ácidos sencillos
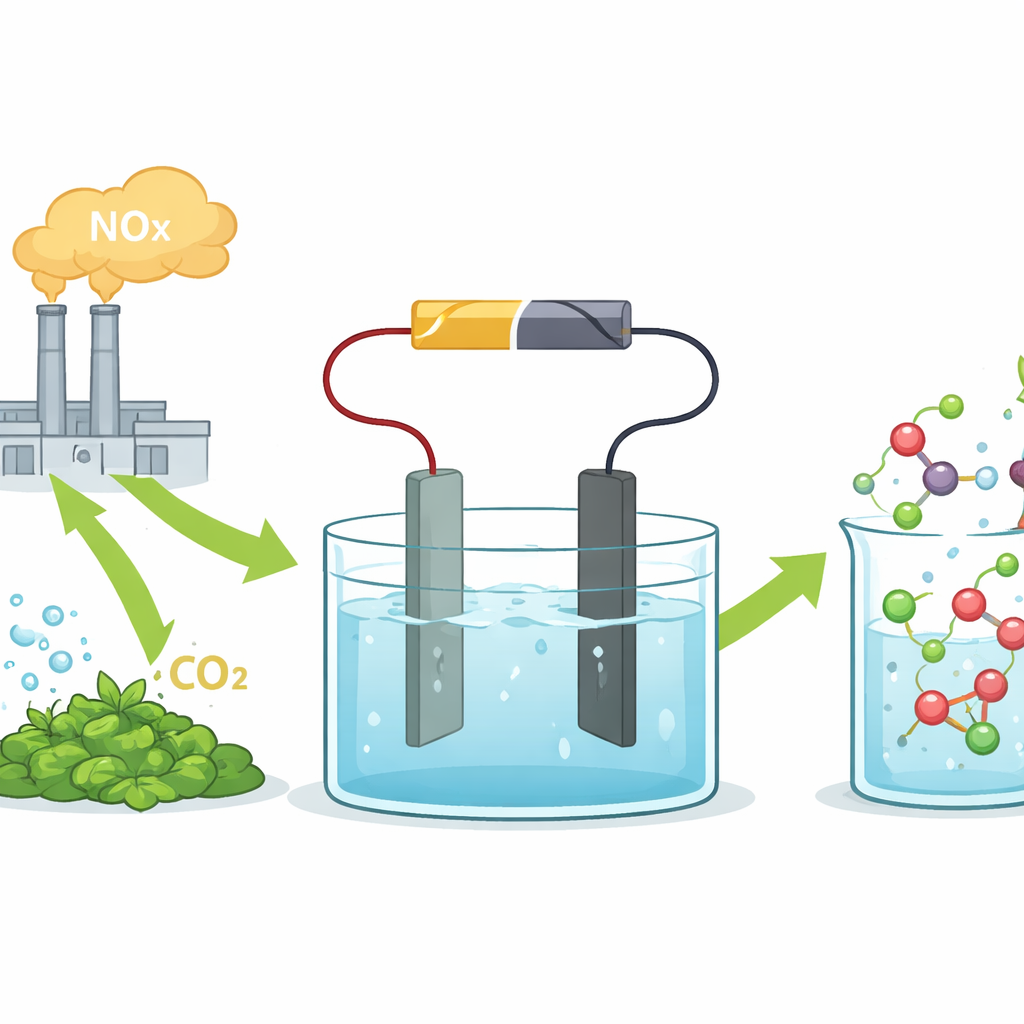
Los investigadores se centran en la electrosíntesis, en la que una tensión aplicada impulsa reacciones químicas en una solución líquida. Alimentan el sistema con ácido nítrico, que puede derivarse de los gases NOx industriales, y ácido oxálico, que puede producirse a partir de dióxido de carbono o biomasa. En el corazón de su montaje hay un electrodo a base de estaño que dirige selectivamente la reacción hacia la glicina en lugar de subproductos no deseados o hidrógeno. En una celda de laboratorio simple, este catalizador de estaño convierte los dos ácidos en glicina con alta selectividad y a densidades de corriente cercanas a las usadas en la industria, demostrando que el enfoque no es solo una curiosidad de laboratorio.
Cómo la superficie del catalizador y las condiciones locales hacen el trabajo
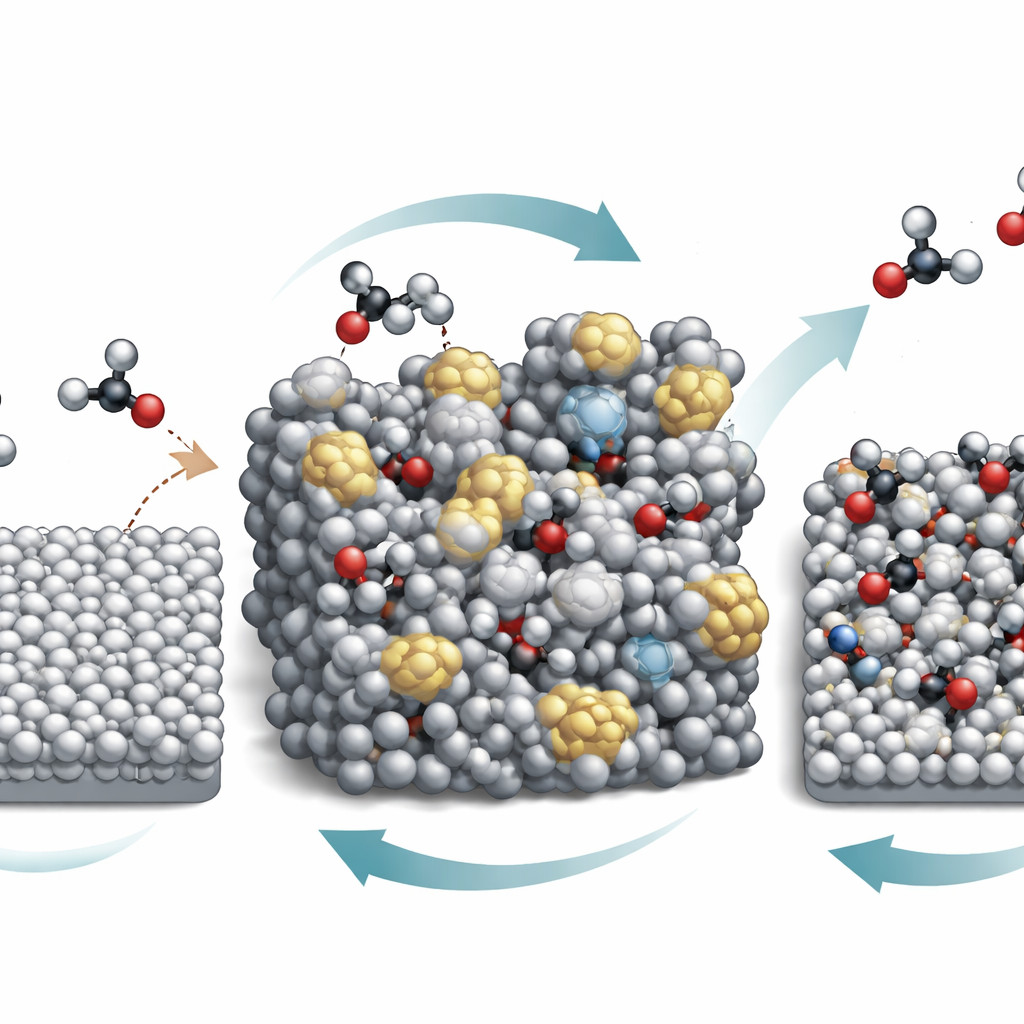
Un hallazgo clave es que la superficie de estaño no permanece estática mientras trabaja. Bajo condiciones fuertemente ácidas, el estaño y el ácido nítrico experimentan una especie de ciclo de “respiración” de valencia: el estaño se oxida parcialmente y luego se reduce de nuevo por la tensión aplicada. Este vaivén continuo rompe gradualmente la estructura cristalina ordenada y genera una superficie de estaño amorfa y desordenada. Sondeos avanzados, incluidas técnicas de rayos X y vibracionales utilizadas mientras la reacción está en curso, muestran que esta forma amorfa une intermedios cruciales C–N con más fuerza que la superficie lisa original. Al mismo tiempo, la reacción vigorosa eleva el pH justo en el electrodo, aunque la solución circundante siga siendo fuertemente ácida, de modo que ácidos débiles como el oxálico y sus derivados existen principalmente en forma cargada negativamente cerca de la superficie.
De reacciones en cadena lentas a química de superficie rápida
Estos cambios tanto en el catalizador como en su microambiente invierten la vía de reacción. Al principio, se forman en el líquido intermedios como el ácido glicóxico y su oxima, que luego se convierten lentamente en glicina a través de una cadena de pasos, lo que conduce a rendimientos modestos. A medida que el estaño se vuelve amorfo y el pH local aumenta, los intermedios cargados negativamente se adhieren con más fuerza a la superficie y se hidrogenan directamente en la interfaz en lugar de dispersarse en la solución. Los autores muestran que esta vía dominada por la superficie es más rápida y más selectiva, llevando la fracción de la corriente eléctrica que acaba en glicina por encima del 90% cuando se opera en un reactor de flujo diseñado especialmente. También demuestran que moléculas relacionadas, como otros pequeños ácidos ceto, pueden convertirse en sus correspondientes aminoácidos, lo que sugiere que la estrategia es ampliamente aplicable.
Escalar hasta una producción práctica
Guiado por sus conocimientos mecanísticos, el equipo construye una celda de flujo que hace circular continuamente la mezcla ácida frente a un electrodo de estaño amorfo preactivado. Ajustando la velocidad de flujo y la composición de alimentación para preservar el entorno local beneficioso, alcanzan densidades de corriente relevantes a escala industrial manteniendo alta la selectividad hacia la glicina. Debido a que el proceso usa solo los ácidos reactivos y no sales de apoyo adicionales, el producto final puede aislarse simplemente eliminando el agua, obteniendo glicina casi pura. Un análisis económico básico sugiere que, si se alimenta con electricidad barata, este método podría producir glicina a aproximadamente la mitad del coste actual del mercado, especialmente si se combina con sistemas de plasma de baja temperatura que convierten el aire y el agua en ácido nítrico in situ.
Un camino más limpio hacia moléculas cotidianas
En conjunto, el estudio muestra que gestionar con cuidado tanto el estado dinámico de un catalizador como la fina capa de solución a su alrededor puede transformar una reacción ineficiente en una altamente selectiva y escalable. Aprovechando fuentes de nitrógeno y carbono residuales y conduciendo la química con electricidad, los autores trazan un camino hacia una producción de aminoácidos más limpia. Su trabajo sugiere que un control similar de la reconstrucción del catalizador y del pH local podría desbloquear síntesis más verdes para muchos otros compuestos con nitrógeno que sustentan la vida moderna.
Cita: Han, S., Liu, H., Timoshenko, J. et al. Sn catalyst reconstruction and microenvironment modulation for efficient amino acid electrosynthesis via C–N coupling. Nat Commun 17, 3614 (2026). https://doi.org/10.1038/s41467-026-71694-4
Palabras clave: electrosíntesis, química verde, glicina, catalizador de estaño, aminoácidos