Clear Sky Science · fr
Reconstruction du catalyseur à base d’étain et modulation du microenvironnement pour une électrosynthèse efficace d’acides aminés via couplage C–N
Transformer les déchets en briques utiles
Les acides aminés, ces petites molécules qui composent les protéines, sont des ingrédients essentiels pour les médicaments, l’alimentation animale et les compléments alimentaires. Aujourd’hui, de nombreux acides aminés sont produits par des procédés qui reposent sur des produits chimiques toxiques et des processus énergivores. Cette étude explore une voie différente : utiliser l’électricité et des flux de déchets industriels courants pour fabriquer la glycine, l’acide aminé le plus simple, de manière plus propre et plus efficace.
Pourquoi repenser la production d’acides aminés importe
Les méthodes conventionnelles de production d’acides aminés, comme le procédé de Strecker, dépendent du cyanure et de l’ammoniac, qui soulèvent des problèmes de sécurité et d’impact climatique. Les voies biologiques faisant appel à des enzymes ou des micro-organismes peuvent être plus douces, mais elles sont souvent lentes, coûteuses à exploiter et adaptées à une gamme restreinte de produits. Dans un monde qui cherche une chimie plus verte alimentée par de l’électricité renouvelable, il y a un fort intérêt à trouver de nouvelles façons d’assembler des blocs carbonés et azotés en acides aminés sans réactifs dangereux ni hautes températures et pressions.
Utiliser l’électricité pour construire la glycine à partir d’acides simples
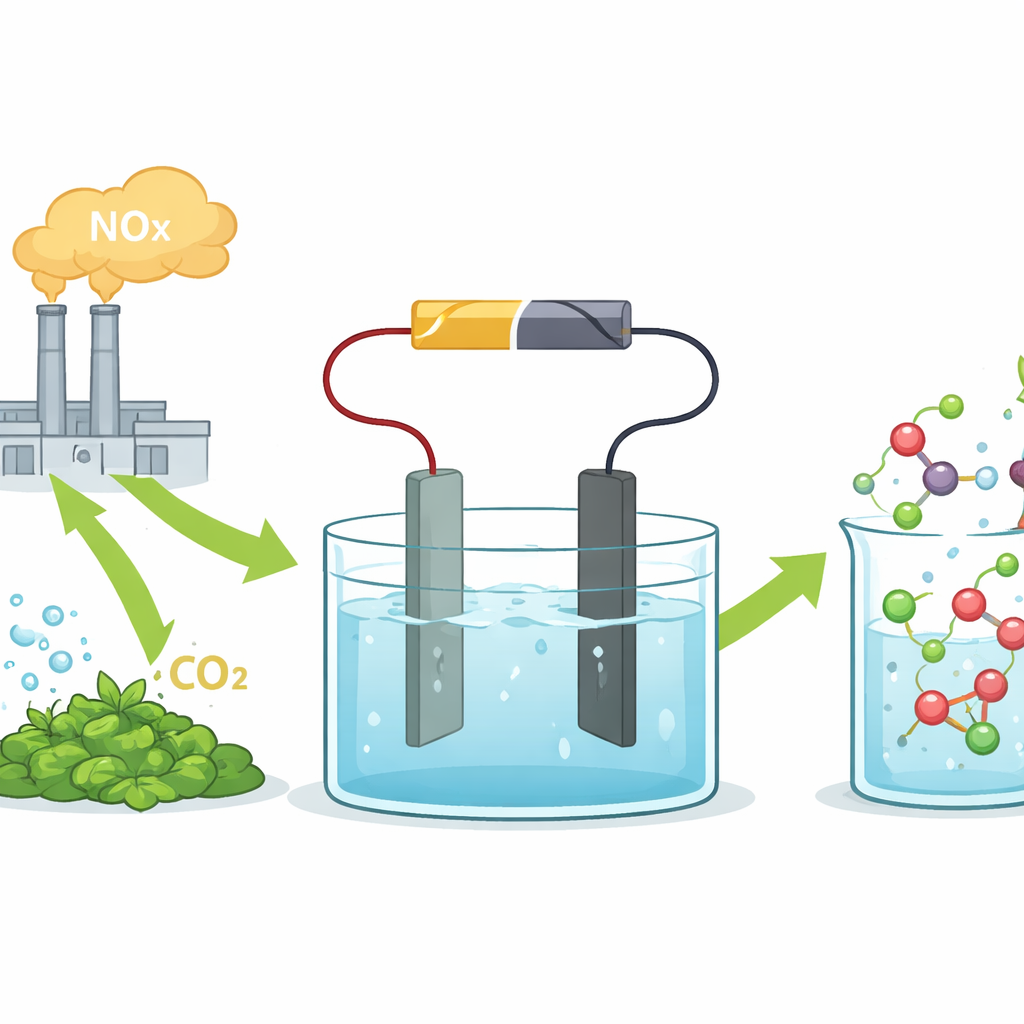
Les chercheurs se concentrent sur l’électrosynthèse, où une tension appliquée conduit des réactions chimiques dans une solution liquide. Ils alimentent le système en acide nitrique, qui peut être dérivé des émissions industrielles de NOx, et en acide oxalique, qui peut être produit à partir du dioxyde de carbone ou de la biomasse. Au cœur de leur dispositif se trouve une électrode à base d’étain qui oriente sélectivement la réaction vers la glycine plutôt que vers des sous-produits indésirables ou le dégagement d’hydrogène. Dans une cellule de laboratoire simple, ce catalyseur à l’étain convertit les deux acides en glycine avec une forte sélectivité et à des densités de courant approchant celles utilisées industriellement, démontrant que l’approche n’est pas qu’une curiosité de laboratoire.
Comment la surface du catalyseur et les conditions locales font le travail
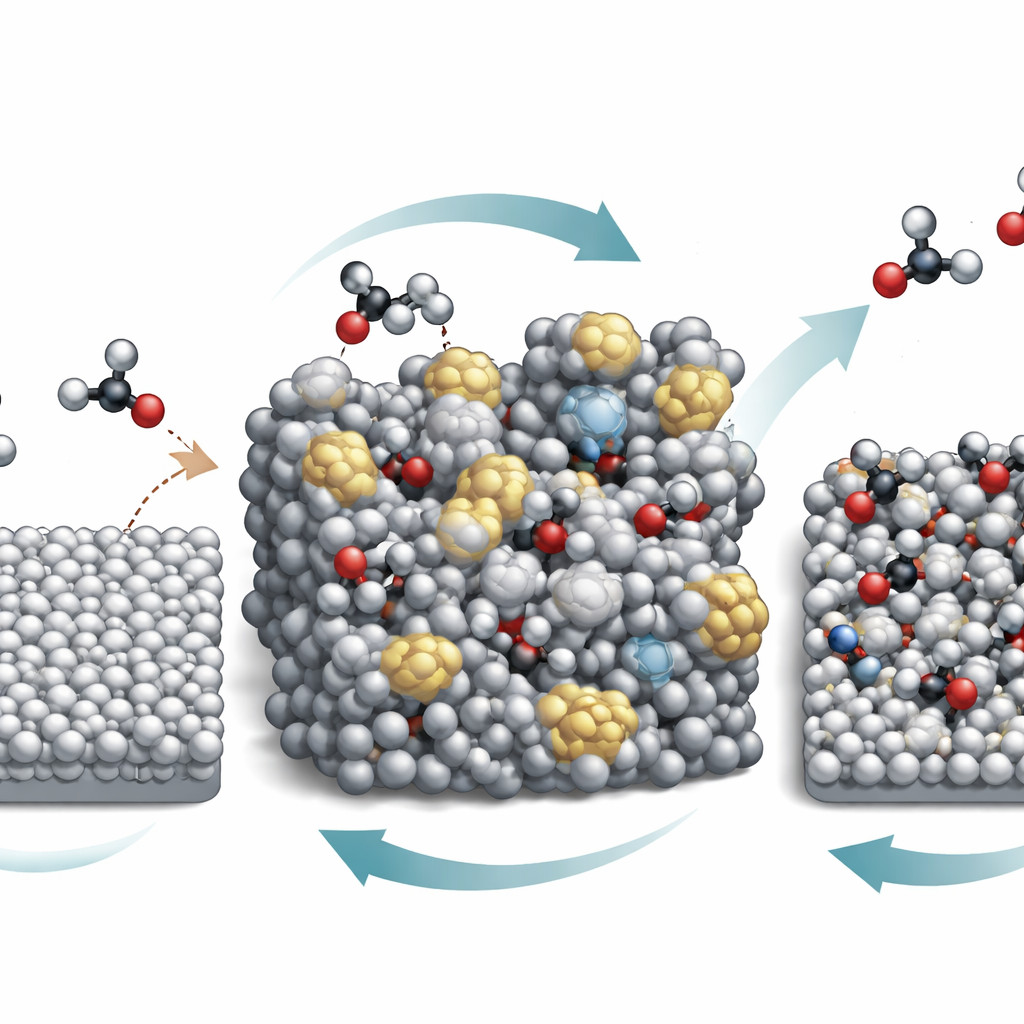
Une découverte clé est que la surface d’étain ne reste pas statique pendant son fonctionnement. En conditions fortement acides, l’étain et l’acide nitrique subissent une sorte de cycle d’« respiration » de valence : l’étain s’oxyde partiellement puis est réduit de nouveau par la tension appliquée. Cet aller-retour continu fragmente progressivement la structure cristalline ordonnée et produit une surface d’étain amorphe et désordonnée. Des sondes avancées, y compris des techniques aux rayons X et vibratoires utilisées en opérando, montrent que cette forme amorphe lie les intermédiaires carbone–azote cruciaux plus fortement que la surface lisse d’origine. Parallèlement, la réaction vigoureuse élève le pH juste à la surface de l’électrode, même si la solution environnante reste fortement acide, de sorte que des acides faibles comme l’acide oxalique et ses dérivés existent principalement sous forme chargée négativement près de la surface.
De réactions en chaîne lentes à une chimie de surface rapide
Ces changements, tant au niveau du catalyseur que du microenvironnement, inversent le parcours réactionnel. Au départ, des intermédiaires tels que l’acide glyoxylique et son oxime se forment en phase liquide puis sont lentement convertis en glycine par une chaîne d’étapes, conduisant à des rendements modestes. À mesure que l’étain devient amorphe et que le pH local augmente, les intermédiaires chargés négativement adhèrent plus fermement à la surface et sont hydrogénés directement à l’interface au lieu de dériver dans la solution. Les auteurs montrent que cette voie pilotée par la surface est plus rapide et plus sélective, poussant la fraction du courant électrique dirigée vers la glycine au‑dessus de 90 % lorsqu’elle est exploitée dans un réacteur à flux spécialement conçu. Ils démontrent également que des molécules apparentées, comme d’autres petits acides cétos, peuvent être converties en leurs acides aminés correspondants, suggérant que la stratégie a une application plus large.
Passer à une production pratique à grande échelle
Guidée par leurs insights mécanistiques, l’équipe construit une cellule à flux qui fait circuler en continu le mélange d’acides devant une électrode d’étain amorphe pré‑activée. En réglant le débit et la composition de l’alimentation pour préserver l’environnement local favorable, ils atteignent des densités de courant pertinentes industriellement tout en maintenant une forte sélectivité pour la glycine. Comme le procédé n’utilise que les acides réactifs et aucun sel de support supplémentaire, le produit final peut être isolé simplement par élimination de l’eau, donnant une glycine presque pure. Une analyse économique de base suggère que, si elle est alimentée par une électricité peu coûteuse, cette méthode pourrait produire de la glycine à environ la moitié du coût du marché actuel, surtout si elle est couplée à des systèmes plasma basse température qui transforment l’air et l’eau en acide nitrique sur site.
Une voie plus propre vers des molécules du quotidien
Dans l’ensemble, l’étude montre que la gestion soignée à la fois de l’état dynamique d’un catalyseur et de la mince couche de solution qui l’entoure peut transformer une réaction inefficace en une réaction hautement sélective et évolutive. En exploitant des sources azotées et carbonées de déchets et en pilotant la chimie par l’électricité, les auteurs dessinent une voie vers une production d’acides aminés plus propre. Leur travail suggère que le contrôle similaire de la reconstruction du catalyseur et du pH local pourrait débloquer des synthèses plus vertes pour de nombreuses autres molécules contenant de l’azote qui soutiennent la vie moderne.
Citation: Han, S., Liu, H., Timoshenko, J. et al. Sn catalyst reconstruction and microenvironment modulation for efficient amino acid electrosynthesis via C–N coupling. Nat Commun 17, 3614 (2026). https://doi.org/10.1038/s41467-026-71694-4
Mots-clés: électrosynthèse, chimie verte, glycine, catalyseur à l’étain, acides aminés