Clear Sky Science · pt
Reconstrução do catalisador de Sn e modulação do microambiente para eletrossíntese eficiente de aminoácidos via acoplamento C–N
Transformando Resíduos em Blocos de Construção Úteis
Aminoácidos, as pequenas moléculas que formam proteínas, são ingredientes essenciais para medicamentos, ração animal e suplementos alimentares. Hoje, muitos aminoácidos são produzidos por rotas que dependem de produtos químicos tóxicos e processos intensivos em energia. Este estudo explora um caminho diferente: usar eletricidade e correntes de resíduos industriais comuns para fabricar glicina, o aminoácido mais simples, de maneira mais limpa e eficiente.
Por que Repensar a Produção de Aminoácidos é Importante
Métodos convencionais para fabricar aminoácidos, como o processo Strecker, dependem de cianeto e amônia, ambos associados a riscos de segurança e impactos climáticos. Rotas biológicas que usam enzimas ou microrganismos podem ser mais suaves, mas costumam ser lentas, caras de operar e direcionadas a uma faixa restrita de produtos. Com o mundo buscando química mais verde alimentada por eletricidade renovável, há grande interesse em encontrar novas maneiras de unir blocos carbonados e nitrogenados em aminoácidos sem reagentes perigosos ou altas temperaturas e pressões.
Usando Eletricidade para Construir Glicina a partir de Ácidos Simples
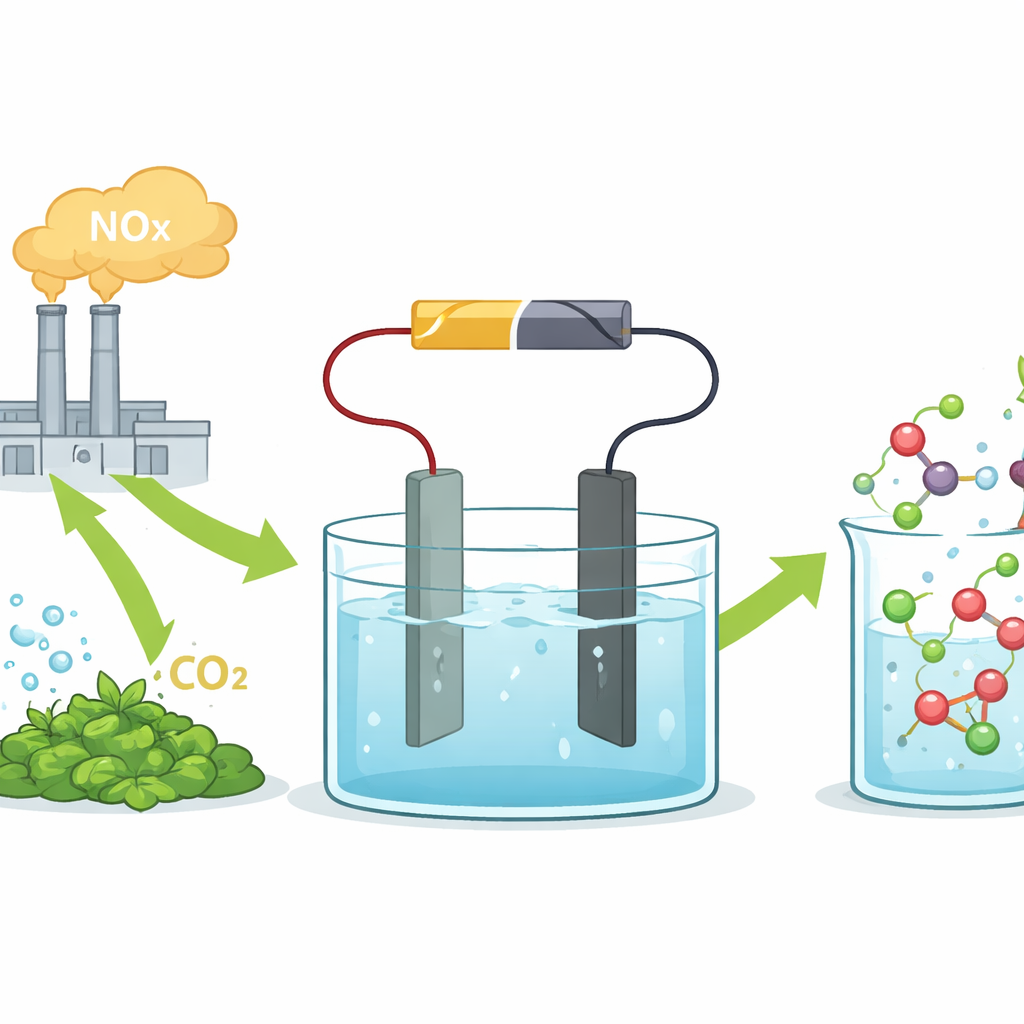
Os pesquisadores concentram-se em eletrossíntese, na qual uma voltagem aplicada impulsiona reações químicas em solução líquida. Eles alimentam o sistema com ácido nítrico, que pode ser derivado de emissões industriais de NOx, e ácido oxálico, que pode ser produzido a partir de dióxido de carbono ou biomassa. No centro do arranjo está um eletrodo à base de estanho que direciona seletivamente a reação para a glicina em vez de subprodutos indesejáveis ou gás hidrogênio. Em uma célula de laboratório simples, esse catalisador de estanho converte os dois ácidos em glicina com alta seletividade e em densidades de corrente próximas às usadas na indústria, demonstrando que a abordagem não é apenas uma curiosidade de laboratório.
Como a Superfície do Catalisador e as Condições Locais Fazem o Trabalho
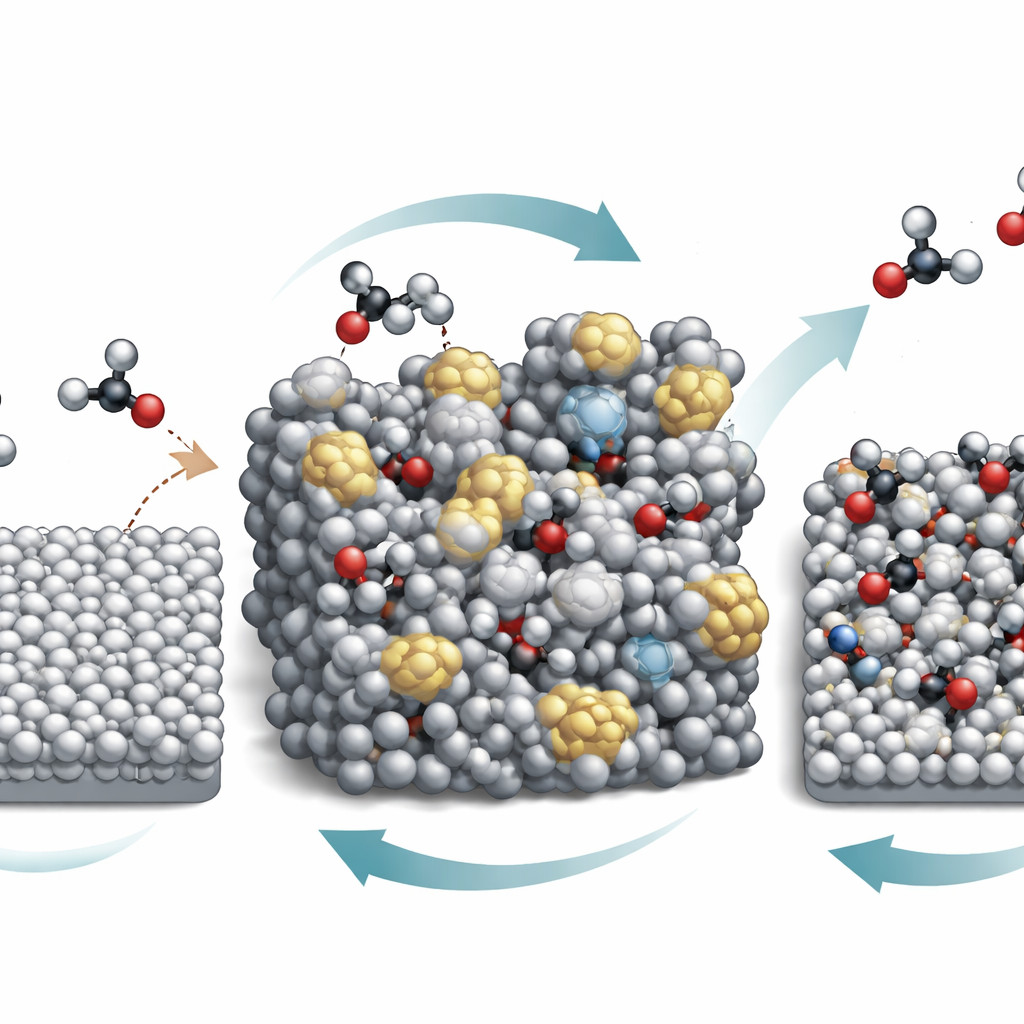
Uma descoberta chave é que a superfície de estanho não permanece estática enquanto funciona. Em condições fortemente ácidas, o estanho e o ácido nítrico passam por uma espécie de ciclo de "respiração" de valência: o estanho se oxida parcialmente e então é reduzido de volta pela voltagem aplicada. Esse vai-e-vem contínuo gradualmente quebra a estrutura cristalina ordenada e produz uma superfície de estanho amorfa e desordenada. Sondas avançadas, incluindo técnicas de raios X e vibracionais usadas durante a reação, mostram que essa forma amorfa liga intermediários cruciais de carbono–nitrogênio mais fortemente do que a superfície lisa original. Ao mesmo tempo, a reação vigorosa eleva o pH exatamente na eletrodo, embora a solução circundante permaneça fortemente ácida, de modo que ácidos fracos como o ácido oxálico e seus derivados existam principalmente em forma carregada negativamente perto da superfície.
De Reações em Cadeia Lentas para Química de Superfície Rápida
Essas mudanças tanto no catalisador quanto em seu microambiente invertem a via reacional. A princípio, intermediários como ácido glicóxico e seu oxima são formados no líquido e depois convertidos lentamente em glicina por uma cadeia de etapas, levando a rendimentos modestos. Conforme o estanho se torna amorfo e o pH local aumenta, os intermediários carregados negativamente aderem mais firmemente à superfície e são hidrogenados diretamente na interface em vez de se dispersarem na solução. Os autores mostram que essa rota dirigida pela superfície é mais rápida e mais seletiva, elevando a fração da corrente elétrica que se converte em glicina para acima de 90% quando operada em um reator de fluxo especialmente projetado. Eles também demonstram que moléculas relacionadas, como outros pequenos ácidos ceto, podem ser convertidas em seus correspondentes aminoácidos, sugerindo que a estratégia é amplamente aplicável.
Escalando para uma Produção Prática
Guiada por seus insights mecanísticos, a equipe constrói uma célula de fluxo que circula continuamente a mistura de ácidos por um eletrodo de estanho amorfo pré-ativado. Ao ajustar a taxa de fluxo e a composição de alimentação para preservar o ambiente local benéfico, eles alcançam densidades de corrente relevantes para a indústria mantendo alta seletividade para glicina. Como o processo usa apenas os ácidos reagentes e não requer sais de suporte extras, o produto final pode ser isolado simplesmente pela remoção da água, produzindo glicina quase pura. Uma análise econômica básica sugere que, se alimentado por eletricidade barata, esse método poderia produzir glicina a aproximadamente metade do custo de mercado atual, especialmente se acoplado a sistemas de plasma a baixa temperatura que convertem ar e água em ácido nítrico no local.
Um Caminho Mais Limpo para Moléculas do Dia a Dia
No geral, o estudo mostra que gerir cuidadosamente tanto o estado dinâmico de um catalisador quanto a fina camada de solução ao seu redor pode transformar uma reação ineficiente em uma rota altamente seletiva e escalável. Aproveitando fontes de nitrogênio e carbono derivadas de resíduos e conduzindo a química com eletricidade, os autores delineiam um caminho para uma produção de aminoácidos mais limpa. O trabalho sugere que controle semelhante da reconstrução do catalisador e do pH local poderia desbloquear sínteses mais verdes para muitas outras moléculas contendo nitrogênio que sustentam a vida moderna.
Citação: Han, S., Liu, H., Timoshenko, J. et al. Sn catalyst reconstruction and microenvironment modulation for efficient amino acid electrosynthesis via C–N coupling. Nat Commun 17, 3614 (2026). https://doi.org/10.1038/s41467-026-71694-4
Palavras-chave: eletrossíntese, química verde, glicina, catalisador de estanho, aminoácidos