Clear Sky Science · de
Rekonstruktion von Sn-Katalysatoren und Modulation des Mikro‑Umfelds für effiziente Aminosäure‑Elektrosynthese via C–N‑Kopplung
Abfall in nützliche Bausteine verwandeln
Aminosäuren, die winzigen Moleküle, aus denen Proteine bestehen, sind unverzichtbare Zutaten für Medikamente, Tierfutter und Nahrungsergänzungsmittel. Heute werden viele Aminosäuren über Verfahren hergestellt, die auf giftigen Chemikalien und energieintensiven Prozessen beruhen. Diese Studie untersucht einen anderen Weg: Strom und gängige industrielle Abfallströme zu nutzen, um Glycin, die einfachste Aminosäure, auf sauberere und effizientere Weise herzustellen.
Warum ein Umdenken in der Aminosäurenproduktion wichtig ist
Konventionelle Verfahren zur Herstellung von Aminosäuren, wie der Strecker‑Prozess, arbeiten mit Cyaniden und Ammoniak, die beide Sicherheits‑ und Klimaprobleme mit sich bringen. Biologische Wege mit Enzymen oder Mikroben können schonender sein, sind aber oft langsam, teuer im Betrieb und auf einen engen Produktbereich zugeschnitten. Während die Welt nach grünerer Chemie sucht, die mit erneuerbarem Strom betrieben wird, besteht großes Interesse daran, neue Wege zu finden, Kohlenstoff‑ und Stickstoffbausteine zu Aminosäuren zu verbinden, ohne gefährliche Reagenzien oder hohe Temperaturen und Drücke.
Elektrizität nutzen, um Glycin aus einfachen Säuren aufzubauen
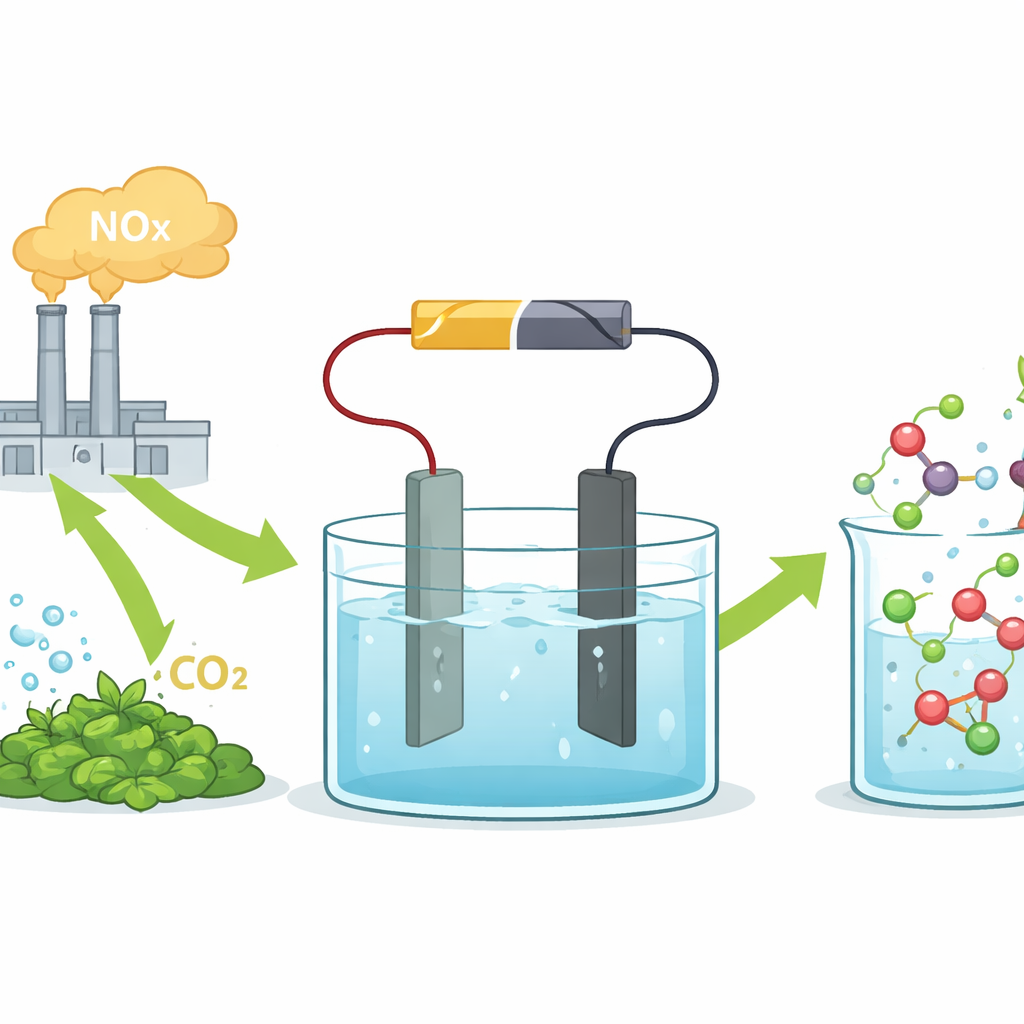
Die Forschenden konzentrieren sich auf Elektrosynthese, bei der eine angelegte Spannung chemische Reaktionen in einer Lösung antreibt. Sie speisen das System mit Salpetersäure, die aus industriellen NOx‑Abgasen gewonnen werden kann, und Oxalsäure, die aus Kohlendioxid oder Biomasse hergestellt werden kann. Im Zentrum ihres Aufbaus steht eine zinnbasierte Elektrode, die die Reaktion selektiv in Richtung Glycin statt in Richtung unerwünschter Nebenprodukte oder Wasserstoffgas lenkt. In einer einfachen Laborzelle wandelt dieser Zinnkatalysator die beiden Säuren mit hoher Selektivität und bei Stromdichten um, die an industrielle Bedingungen heranreichen, in Glycin um und zeigt damit, dass der Ansatz nicht nur eine Laborneugier ist.
Wie Katalysatoroberfläche und lokale Bedingungen die Arbeit übernehmen
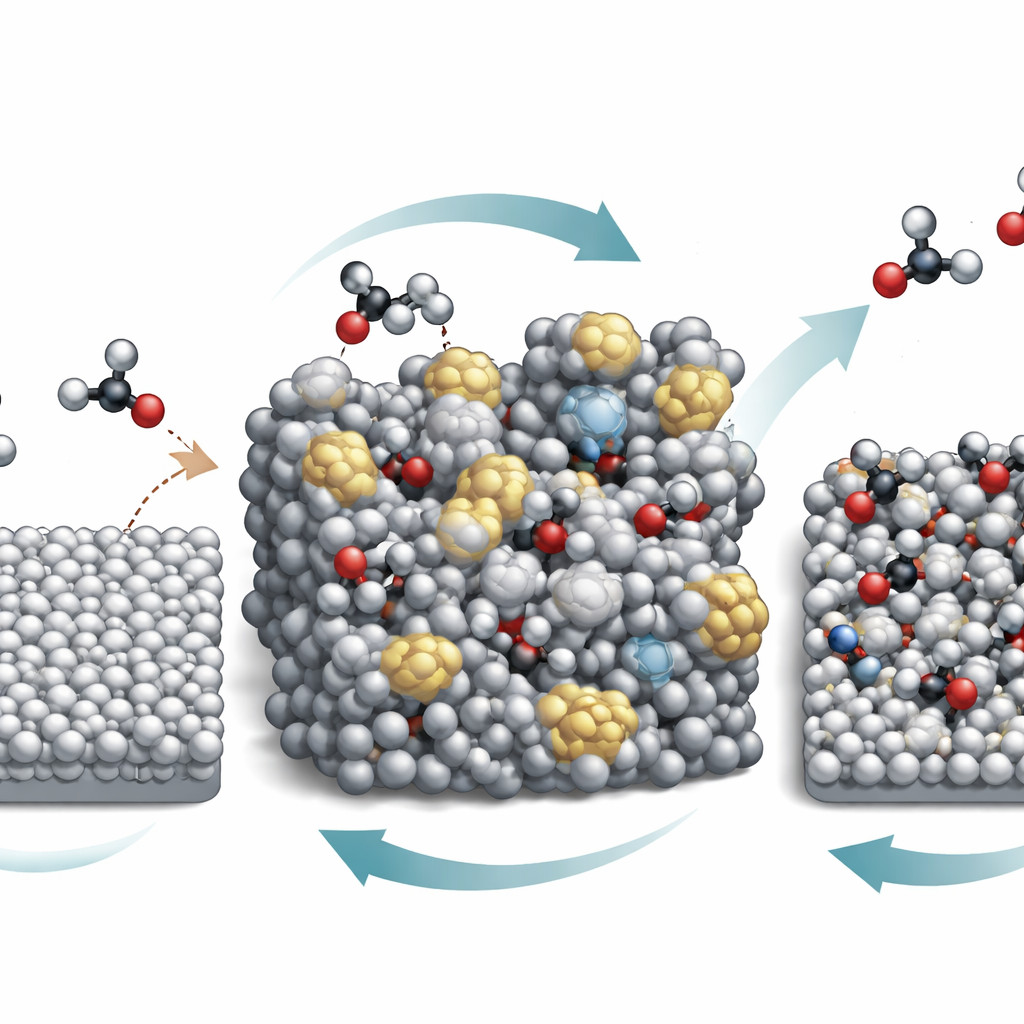
Eine zentrale Erkenntnis ist, dass die Zinnoberfläche während des Betriebs nicht statisch bleibt. Unter stark sauren Bedingungen durchläuft Zinn zusammen mit der Salpetersäure eine Art Valenz‑„Atmungszyklus“: Zinn wird partiell oxidiert und dann durch die angelegte Spannung wieder reduziert. Dieses ständige Hin und Her baut allmählich die geordnete Kristallstruktur auf und erzeugt eine amorphe, ungeordnete Zinnoberfläche. Fortgeschrittene Sonden, darunter in situ‑Röntgen‑ und Schwingungsspektroskopie, zeigen, dass diese amorphe Form entscheidende C–N‑Zwischenprodukte stärker bindet als die ursprüngliche glatte Oberfläche. Gleichzeitig erhöht die intensive Reaktion den pH‑Wert unmittelbar an der Elektrode, obwohl die umgebende Lösung stark sauer bleibt, sodass schwache Säuren wie Oxalsäure und deren Derivate in der Nähe der Oberfläche überwiegend in negativer, deprotonierter Form vorliegen.
Von langsamen Kettenreaktionen zu schneller Oberflächenchemie
Diese Veränderungen sowohl im Katalysator als auch in seinem Mikro‑Umfeld drehen den Reaktionspfad um. Zunächst bilden sich Zwischenprodukte wie Glyoxylsäure und deren Oxime in der Flüssigkeit und werden dann langsam in einer Kette von Schritten zu Glycin konvertiert, was nur mäßige Ausbeuten liefert. Wenn das Zinn amorph wird und der lokale pH‑Wert ansteigt, haften die negativ geladenen Zwischenprodukte stärker an der Oberfläche und werden direkt an der Grenzfläche hydriert, statt ins Lösungsmittel zu diffundieren. Die Autor*innen zeigen, dass dieser oberflächengetriebene Weg schneller und selektiver ist und den Anteil des elektrischen Stroms, der in Glycin einfließt, in einem speziell gestalteten Durchflussreaktor über 90 % hebt. Sie demonstrieren außerdem, dass verwandte Moleküle, etwa andere kleine Ketosäuren, in die entsprechenden Aminosäuren überführt werden können, was darauf hindeutet, dass die Strategie breit anwendbar ist.
Hochskalierung zur praktischen Produktion
Anhand ihrer mechanistischen Einsichten bauen die Forschenden eine Durchflusszelle, die das Säuregemisch kontinuierlich an einer voraktivierten amorphen Zinnelektrode vorbeiführt. Durch Einstellung von Durchflussrate und Einspeisezusammensetzung, um das günstige lokale Umfeld zu erhalten, erreichen sie industriell relevante Stromdichten bei hoher Glycin‑Selektivität. Da der Prozess nur die Reaktantsäuren und keine zusätzlichen Trägersalze verwendet, kann das Endprodukt einfach durch Wasserentzug isoliert werden und liefert nahezu reines Glycin. Eine einfache Wirtschaftlichkeitsanalyse legt nahe, dass dieses Verfahren bei billiger Elektrizität Glycin zu ungefähr halb so hohen Kosten wie der aktuelle Marktpreis produzieren könnte, insbesondere wenn es mit Niedertemperatur‑Plasmasystemen kombiniert wird, die vor Ort aus Luft und Wasser Salpetersäure erzeugen.
Ein saubererer Weg zu Alltagsmolekülen
Insgesamt zeigt die Studie, dass durch sorgfältige Steuerung sowohl des dynamischen Zustands eines Katalysators als auch der dünnen Lösungsschicht um ihn herum eine ineffiziente Reaktion in eine hochselektive, skalierbare verwandelt werden kann. Indem Abfall‑Stickstoff‑ und Kohlenstoffquellen genutzt und die Chemie mit Strom angetrieben wird, skizzieren die Autor*innen einen Weg zu sauberer hergestellten Aminosäuren. Ihre Arbeit legt nahe, dass ähnliche Kontrolle über Katalysatorrekonstruktion und lokalen pH‑Wert grünere Synthesen vieler anderer stickstoffhaltiger Moleküle ermöglichen könnte, die die moderne Welt tragen.
Zitation: Han, S., Liu, H., Timoshenko, J. et al. Sn catalyst reconstruction and microenvironment modulation for efficient amino acid electrosynthesis via C–N coupling. Nat Commun 17, 3614 (2026). https://doi.org/10.1038/s41467-026-71694-4
Schlüsselwörter: Elektrosynthese, grüne Chemie, Glycin, Zinnkatalysator, Aminosäuren