Clear Sky Science · pl
Przebudowa katalizatora Sn i modulacja mikrośrodowiska dla wydajnej elektrosyntezy aminokwasów przez sprzęganie C–N
Przekształcanie odpadów w użyteczne cegiełki
Aminokwasy, niewielkie cząsteczki tworzące białka, są kluczowymi składnikami leków, pasz dla zwierząt i suplementów diety. Obecnie wiele aminokwasów produkuje się metodami opartymi na toksycznych związkach i procesach energochłonnych. W tym badaniu zbadano alternatywną drogę: wykorzystanie elektryczności i powszechnych strumieni odpadów przemysłowych do wytwarzania glicyny, najprostszego aminokwasu, w sposób czystszy i bardziej wydajny.
Dlaczego warto przemyśleć produkcję aminokwasów
Konwencjonalne metody syntezy aminokwasów, takie jak proces Streckera, opierają się na cyjanku i amoniaku, które stwarzają zagrożenia dla bezpieczeństwa i środowiska klimatycznego. Drogą biologiczną, z użyciem enzymów lub mikroorganizmów, można osiągnąć łagodniejsze warunki, lecz często są one powolne, kosztowne i ograniczone do wąskiego zakresu produktów. W świecie dążącym do zielonej chemii napędzanej odnawialną energią rośnie zainteresowanie nowymi sposobami łączenia fragmentów węglowych i azotowych w aminokwasy bez niebezpiecznych reagentów czy wysokich temperatur i ciśnień.
Wykorzystanie elektryczności do budowy glicyny z prostych kwasów
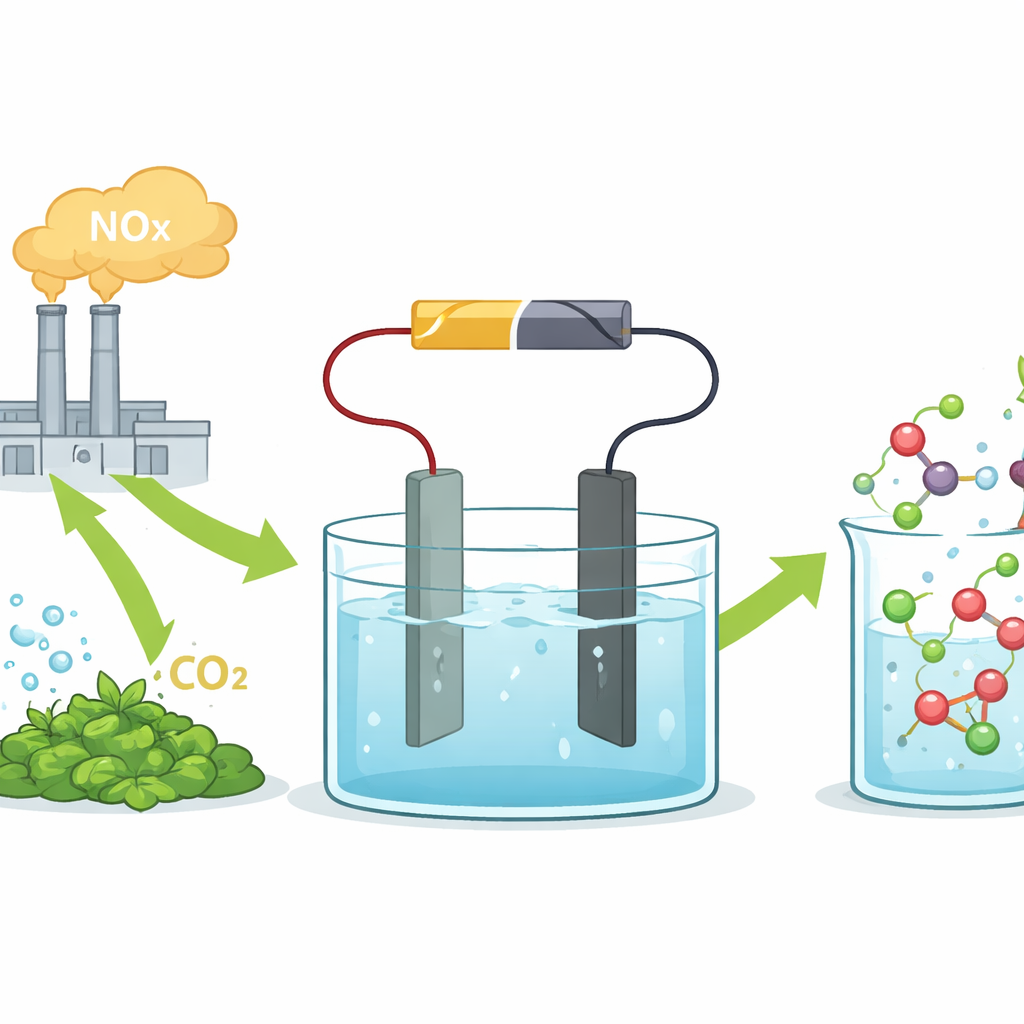
Naukowcy skupili się na elektrosyntezie, w której przyłożone napięcie napędza reakcje chemiczne w roztworze. Do układu podawano kwas azotowy, możliwy do pozyskania z emisji NOx w przemyśle, oraz kwas szczawiowy, który można otrzymać z dwutlenku węgla lub biomasy. W centrum ich układu znajduje się elektroda na bazie cyny, która selektywnie kieruje reakcję w stronę glicyny zamiast tworzenia niepożądanych produktów ubocznych czy wodoru. W prostym ogniwie laboratoryjnym ten katalizator cynowy przekształca oba kwasy w glicynę z wysoką selektywnością i przy gęstościach prądu zbliżonych do stosowanych w przemyśle, co dowodzi, że podejście to nie jest jedynie ciekawostką laboratoryjną.
Jak powierzchnia katalizatora i lokalne warunki wykonują pracę
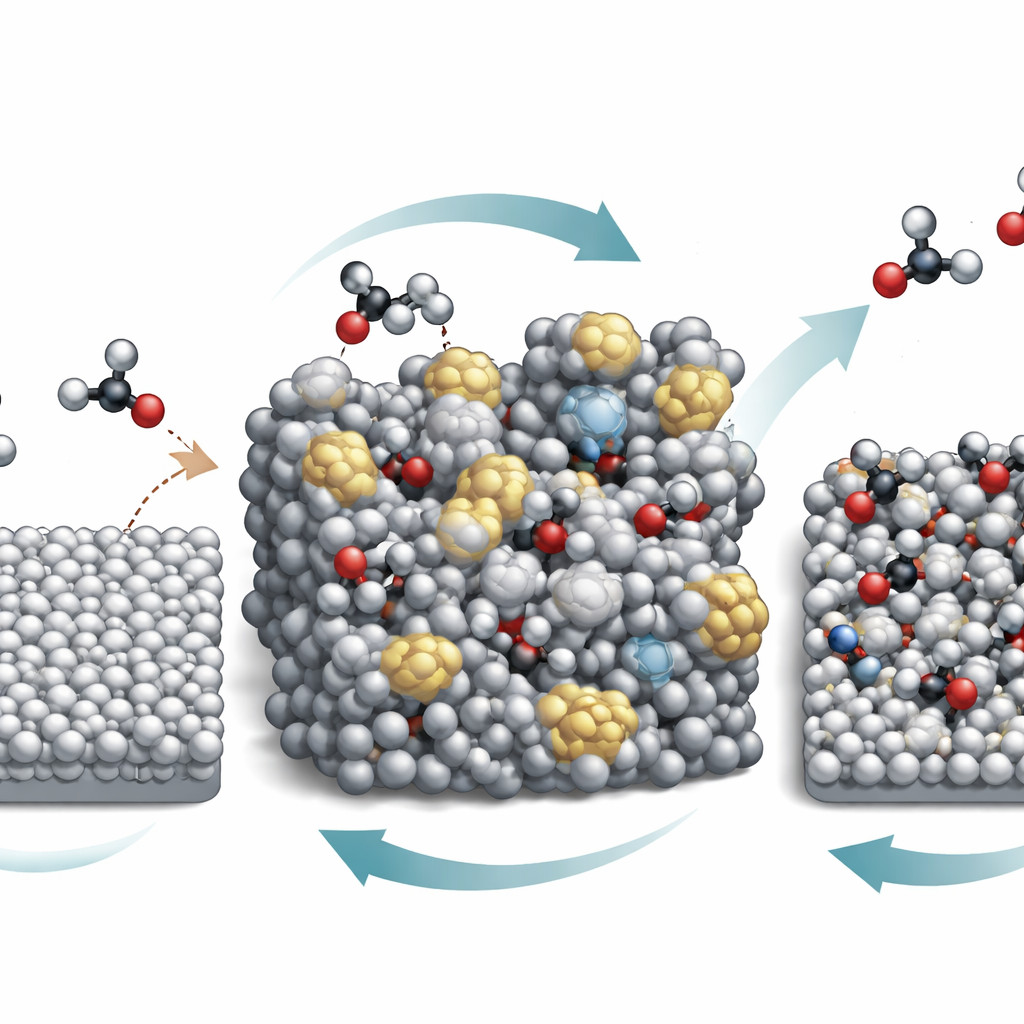
Kluczowym odkryciem jest to, że powierzchnia cyny nie pozostaje statyczna podczas pracy. W silnie kwaśnym środowisku cyna i kwas azotowy przechodzą rodzaj cyklu „oddechowego” zmiany wartościowości: cyna częściowo utlenia się, a następnie jest redukowana przez przyłożone napięcie. To ciągłe naprzemienne działanie stopniowo rozbija uporządkowaną strukturę krystaliczną i tworzy amorficzną, nieuporządkowaną powierzchnię cyny. Zaawansowane techniki pomiarowe, w tym badania rentgenowskie i wibracyjne prowadzone w trakcie reakcji, pokazują, że ta amorficzna forma silniej wiąże kluczowe pośrednie związki C–N niż pierwotna gładka powierzchnia. Równocześnie intensywna reakcja podnosi pH tuż przy elektrodzie, mimo że otaczający roztwór pozostaje silnie kwaśny, dzięki czemu słabe kwasy, takie jak kwas szczawiowy i jego pochodne, występują w pobliżu powierzchni głównie w postaci naładowanej ujemnie.
Od powolnych łańcuchów reakcji do szybkiej chemii powierzchniowej
Zmiany zarówno katalizatora, jak i jego mikrośrodowiska odwracają szlak reakcyjny. Początkowo pośrednie produkty, takie jak kwas glicoksylowy i jego oxim, tworzą się w cieczy i następnie powoli przekształcają w glicynę poprzez łańcuch kroków, co daje umiarkowane wydajności. W miarę jak cyna staje się amorficzna i lokalne pH wzrasta, naładowane ujemnie pośredniki silniej przylegają do powierzchni i ulegają bezpośredniej hydrogenacji na styku zamiast dyfundować do roztworu. Autorzy wykazują, że ta droga sterowana powierzchniowo jest szybsza i bardziej selektywna, podnosząc udział prądu elektrycznego kończącego w glicynie powyżej 90% przy pracy w specjalnie zaprojektowanym reaktorze przepływowym. Pokazują też, że pokrewne cząsteczki, takie jak inne małe kwasy keto, można przekształcić w odpowiadające im aminokwasy, co sugeruje szeroką zastosowalność strategii.
Skalowanie do produkcji praktycznej
Na podstawie wniosków mechanistycznych zespół skonstruował ogniwo przepływowe, które ciągle cyrkuluje mieszankę kwasów obok wstępnie aktywowanej amorficznej elektrody cyny. Poprzez dostrojenie prędkości przepływu i składu zasilania tak, by zachować korzystne lokalne warunki, osiągnęli przemysłowo istotne gęstości prądu przy jednoczesnym utrzymaniu wysokiej selektywności glicyny. Ponieważ proces używa jedynie reagentów — kwasów — i nie wymaga dodatkowych soli wspomagających, produkt końcowy można wyizolować przez prostą eliminację wody, uzyskując niemal czystą glicynę. Podstawowa analiza ekonomiczna sugeruje, że przy zasilaniu tanim prądem ta metoda mogłaby wytwarzać glicynę w przybliżeniu za połowę obecnych kosztów rynkowych, szczególnie jeśli połączyć ją z niskotemperaturowymi systemami plazmowymi wytwarzającymi kwas azotowy z powietrza i wody na miejscu.
Czystsza ścieżka do powszechnych cząsteczek
Podsumowując, praca pokazuje, że uważne zarządzanie zarówno dynamicznym stanem katalizatora, jak i cienką warstwą roztworu wokół niego może przekształcić nieefektywną reakcję w wysoce selektywną i skalowalną. Wykorzystując odpadowe źródła azotu i węgla oraz napędzając chemię elektrycznością, autorzy wytyczają drogę ku czyściejszej produkcji aminokwasów. Ich wyniki sugerują, że podobna kontrola przebudowy katalizatora i lokalnego pH może umożliwić bardziej zielone syntezy wielu innych związków azotowych, które są fundamentem współczesnego życia.
Cytowanie: Han, S., Liu, H., Timoshenko, J. et al. Sn catalyst reconstruction and microenvironment modulation for efficient amino acid electrosynthesis via C–N coupling. Nat Commun 17, 3614 (2026). https://doi.org/10.1038/s41467-026-71694-4
Słowa kluczowe: elektrosynteza, zielona chemia, glicyna, katalizator cyny, aminokwasy