Clear Sky Science · it
Ricostruzione del catalizzatore a base di Sn e modulazione del microambiente per un�efficiente elettrosintesi di amminoacidi tramite accoppiamento C�N
Trasformare i rifiuti in mattoni utili
Gli amminoacidi, le piccole molecole che costituiscono le proteine, sono ingredienti essenziali per farmaci, mangimi animali e integratori alimentari. Oggi molti amminoacidi vengono prodotti tramite percorsi che fanno ricorso a sostanze chimiche tossiche e processi ad alto consumo energetico. Questo studio esplora una via diversa: usare elettricità e flussi di scarto industriale comuni per produrre glicina, l�amminoacido pi� semplice, in modo pi� pulito ed efficiente.
Perch� ripensare la produzione di amminoacidi � importante
I metodi convenzionali per la produzione di amminoacidi, come il processo di Strecker, dipendono dal cianuro e dall�ammoniaca, entrambi associati a rischi per la sicurezza e per il clima. Le vie biologiche che impiegano enzimi o microrganismi possono essere pi� delicate, ma spesso sono lente, costose da gestire e mirate a una gamma ristretta di prodotti. Con il mondo alla ricerca di una chimica pi� sostenibile alimentata da elettricità rinnovabile, c����������������������������������������������������������� interessato a trovare nuovi modi per unire blocchi di carbonio e azoto in amminoacidi senza reagenti pericolosi o condizioni estreme di temperatura e pressione.
Usare l�elettricità per costruire glicina da acidi semplici
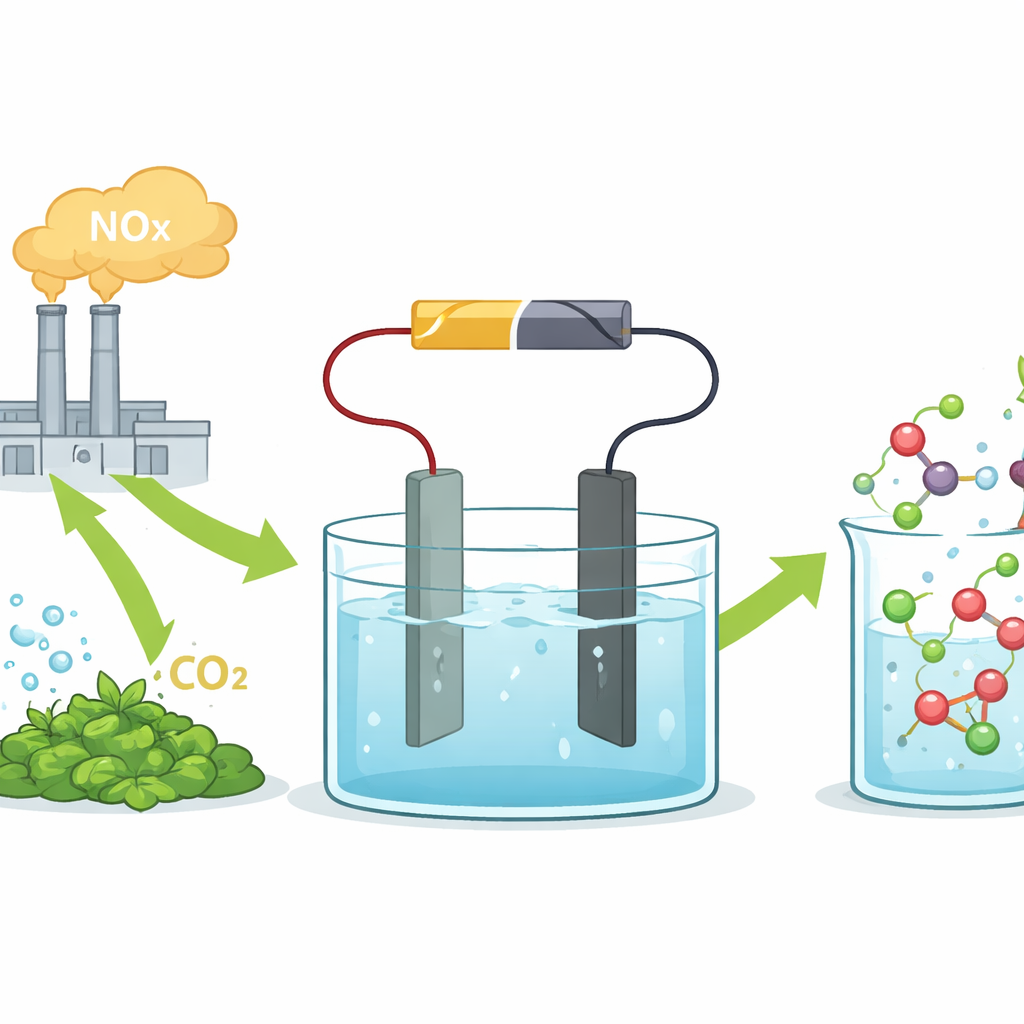
I ricercatori si concentrano sull�elettrosintesi, in cui una tensione applicata guida reazioni chimiche in soluzione liquida. Alimentano il sistema con acido nitrico, che pu� essere ricavato da gas di scarico NOx industriali, e acido ossalico, ottenibile da anidride carbonica o biomassa. Al centro del loro dispositivo c����������������������������������������������������������� un elettrodo a base di stagno che indirizza selettivamente la reazione verso la glicina invece di prodotti secondari indesiderati o idrogeno gassoso. In una cella di laboratorio semplice, questo catalizzatore a base di stagno converte i due acidi in glicina con alta selettivit� e a densit� di corrente prossime a quelle impiegate nell�industria, dimostrando che l�approccio non � soltanto una curiosit� di laboratorio.
Come la superficie del catalizzatore e le condizioni locali fanno il lavoro
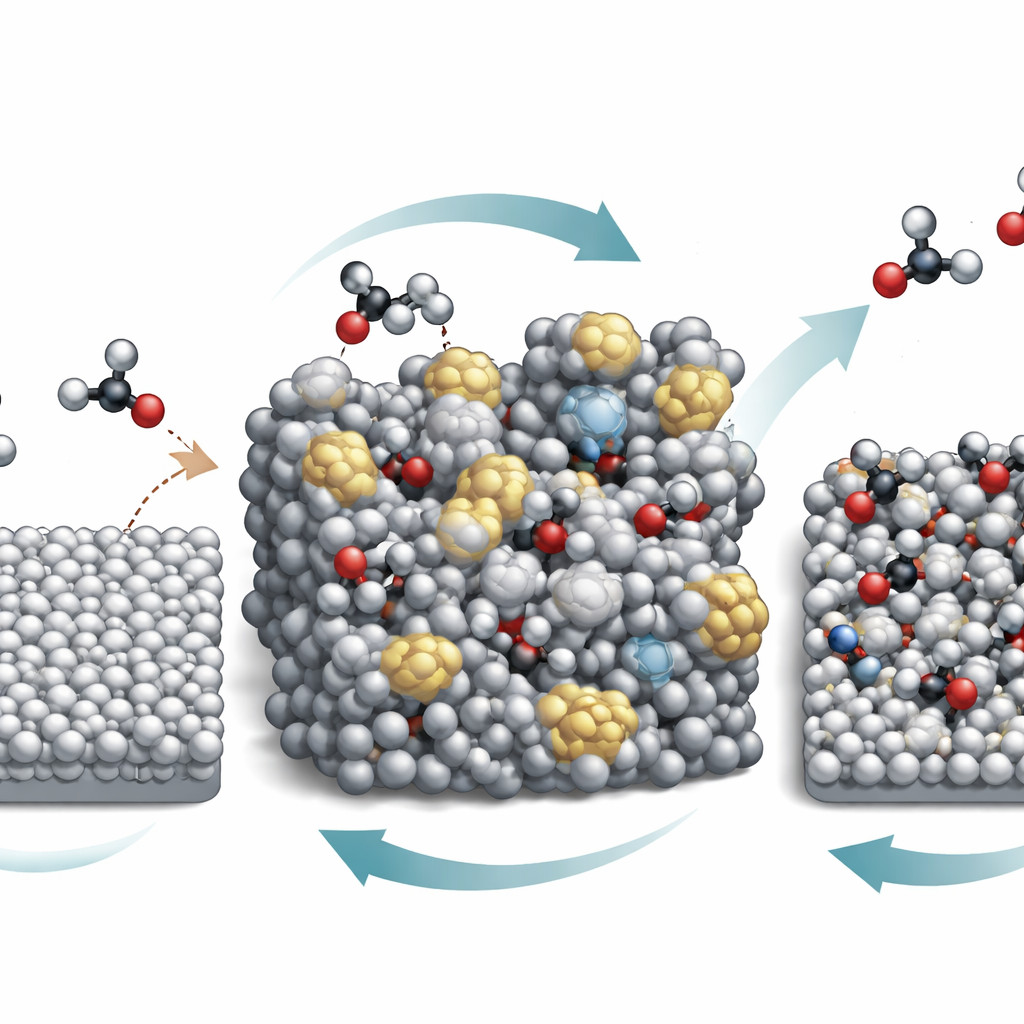
Una scoperta chiave � che la superficie dello stagno non resta statica mentre lavora. In condizioni fortemente acide, lo stagno e l�acido nitrico sperimentano una specie di ciclo di "respirazione" di valenza: lo stagno si ossida parzialmente e poi viene ridotto nuovamente dalla tensione applicata. Questo continuo andirivieni degrada gradualmente la struttura cristallina ordinata e produce una superficie di stagno amorfa e disordinata. Sonde avanzate, comprese tecniche a raggi X e di spettroscopia vibrazionale usate durante la reazione, mostrano che questa forma amorfa lega gli intermedi chiave C�N in modo pi� forte rispetto alla superficie liscia originale. Allo stesso tempo, la reazione vigorosa innalza il pH proprio all�interfaccia dell�elettrodo, nonostante la soluzione circostante rimanga fortemente acida, cos� che acidi deboli come l�ossalico e i suoi derivati esistono per lo pi� in forma negativamente caricata vicino alla superficie.
Da reazioni in catena lente a chimica superficiale rapida
Questi cambiamenti sia nel catalizzatore sia nel microambiente ribaltano il percorso di reazione. All�inizio, intermedi come l�acido glicossilico e il suo oxime si formano in fase liquida e vengono poi convertiti lentamente in glicina attraverso una catena di passaggi, portando a rese modeste. Quando lo stagno diventa amorfo e il pH locale aumenta, gli intermedi caricati negativamente aderiscono pi� saldamente alla superficie e vengono idrogenati direttamente all�interfaccia invece di disperdersi in soluzione. Gli autori mostrano che questa via guidata dalla superficie � pi� veloce e selettiva, portando la frazione di corrente elettrica che finisce in glicina oltre il 90% quando l�apparato � operato in un reattore a flusso appositamente progettato. Dimostrano inoltre che molecole correlate, come altri piccoli acidi chetonici, possono essere convertite nei corrispondenti amminoacidi, suggerendo che la strategia � ampiamente applicabile.
Scalare fino a una produzione pratica
Guidato dalle informazioni meccanicistiche, il team costruisce una cella a flusso che fa circolare continuamente la miscela acida oltre un elettrodo di stagno amorfo pre-attivato. Sintonizzando la velocit� di flusso e la composizione dell�alimentazione per preservare l�ambiente locale favorevole, raggiungono densit� di corrente rilevanti per l�industria mantenendo alta la selettivit� per la glicina. Poich� il processo utilizza solo gli acidi reagenti e nessun sale di supporto aggiuntivo, il prodotto finale pu� essere isolato semplicemente rimuovendo l�acqua, ottenendo glicina quasi pura. Una semplice analisi economica suggerisce che, se alimentato da elettricità a basso costo, questo metodo potrebbe produrre glicina a circa la metá del costo di mercato attuale, specialmente se accoppiato a sistemi a plasma a bassa temperatura che trasformano aria e acqua in acido nitrico direttamente in loco.
Una strada pi� pulita verso molecole di tutti i giorni
Nel complesso, lo studio mostra che gestire con cura sia lo stato dinamico di un catalizzatore sia il sottile strato di soluzione che lo circonda pu� trasformare una reazione inefficiente in una altamente selettiva e scalabile. Sfruttando fonti di azoto e carbonio derivanti da rifiuti e guidando la chimica con elettricità, gli autori delineano un percorso verso una produzione di amminoacidi pi� pulita. Il loro lavoro suggerisce che un controllo simile della ricostruzione del catalizzatore e del pH locale potrebbe sbloccare sintesi pi� verdi per molte altre molecole contenenti azoto che sono alla base della vita moderna.
Citazione: Han, S., Liu, H., Timoshenko, J. et al. Sn catalyst reconstruction and microenvironment modulation for efficient amino acid electrosynthesis via C–N coupling. Nat Commun 17, 3614 (2026). https://doi.org/10.1038/s41467-026-71694-4
Parole chiave: elettrosintesi, chimica verde, glicina, catalizzatore a base di stagno, amminoacidi