Clear Sky Science · ru
Терапия адоптивными γδ Т-клетками контролирует инфекцию цитомегаловируса в доклинических моделях трансплантации
Новая надежда против скрытого вируса
Цитомегаловирус (ЦМВ) — распространённый вирус, который у большинства здоровых людей проходит почти незаметно. Для пациентов, получивших трансплантат органа или костного мозга, ЦМВ однако может быть опасен для жизни и трудно поддаваться лечению одними препаратами. В этом исследовании изучают новый тип клеточной иммунотерапии, основанный на редком подтипе Т‑клеток — γδ Т‑клетках, призванный помочь организму контролировать ЦМВ, когда стандартные методы не работают. Работа указывает путь к универсальной готовой к применению клеточной терапии, способной защитить особенно уязвимых реципиентов трансплантатов.
Почему ЦМВ так опасен после трансплантации
После трансплантации пациенты принимают мощные препараты, чтобы предотвратить отторжение нового органа или донорских клеток. Те же лекарства ослабляют защиту от инфекций. ЦМВ вызывает особую тревогу: это самая частая оппортунистическая инфекция после трансплантации твердых органов и серьёзная проблема после трансплантации стволовых клеток. Пациенты высокого риска, например никогда не встречавшиеся с ЦМВ, но получившие орган от ЦМВ‑положительного донора, часто страдают от рецидивирующих или резистентных к лекарствам инфекций. Новые противовирусные препараты, такие как марибаовир, помогают, но многие пациенты всё равно не очищают вирус полностью или вскоре рецидивируют. Поскольку долгосрочный контроль ЦМВ зависит от устойчивого иммунного ответа, исследователи обращаются к клеточным терапиям, чтобы восстановить противовирусный иммунитет, а не просто временно подавлять вирус.
Другой тип клеточной иммунотерапии
Существующие экспериментальные клеточные терапии против ЦМВ в основном опираются на обычные αβ Т‑клетки, которые распознают фрагменты вируса только при предъявлении их специфическими молекулами, совпадающими по тканевому типу. Это требование ограничивает круг реципиентов для конкретного клеточного продукта и усложняет производство. γδ Т‑клетки, напротив, способны обнаруживать стрессированные или инфицированные клетки без такой строгой совместимости. Команда сосредоточилась на подмножестве Vδ2‑отрицательных γδ Т‑клеток, которые естественно расширяются при инфекции ЦМВ и способны поражать инфицированные клетки. С помощью клинического протокола «Delta One T» (DOT) они показали, что эти клетки можно вырастить в больших количествах как от ЦМВ‑положительных, так и от ЦМВ‑отрицательных доноров, а также из образцов самих пациентов с высоким риском после трансплантации почки, несмотря на низкое количество лимфоцитов и продолжающуюся иммуносупрессию.
Как клетки DOT распознают и контролируют ЦМВ
В лабораторных испытаниях DOT‑клетки смешивали с человеческими клетками, инфицированными клиническими штаммами ЦМВ. Расширенные γδ Т‑клетки продемонстрировали два ключевых поведения: они дегранулировали — признак прямого убийства — и секретировали большие количества интерферона‑γ, мощного противовирусного цитокина, который помогает остановить репликацию вируса и мобилизовать другие иммунные клетки. Эти реакции были высокоспецифичны для ЦМВ и не возникали при взаимодействии с родственными вирусами, такими как вирус простого герпеса или ветряная оспа. Важно, что DOT‑клетки замедляли распространение ЦМВ в фибробластных культурах в зависимости от дозы: с увеличением числа эффекторных клеток действие усиливалось. Неожиданно исследователи обнаружили, что такое распознавание не требовало обычного γδ‑TCR. Вместо этого адгезионная молекула LFA‑1, которая связывается с ICAM‑1 на инфицированных клетках, выступала в роли ключевого ко‑стимулятора: блокирование LFA‑1 или ICAM‑1 резко снижало выброс интерферона‑γ, тогда как искусственная активация LFA‑1 вызывала сильный ответ.
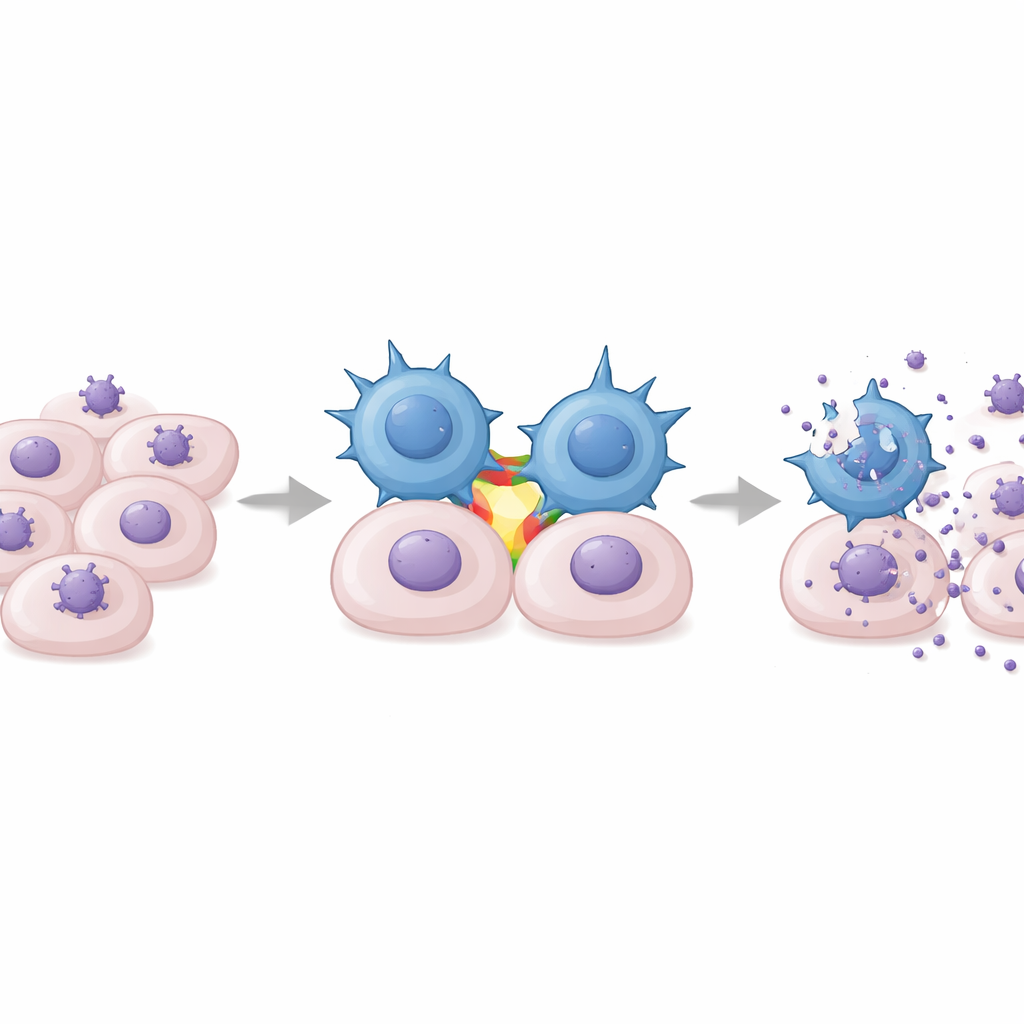
Доказательство защиты в мышиной модели
Поскольку человеческий ЦМВ не инфицирует мышей, команда создала модель на основе мышиного ЦМВ и мышиных γδ Т‑клеток, расширенных по протоколу, сходному с DOT. Эти мышиные клетки приобрели аналогичный активированный цитотоксический профиль. При введении в сильно иммунодефицитных мышей, инфицированных мышиным ЦМВ, расширенные γδ Т‑клетки мигрировали в ключевые органы, снижали вирусную нагрузку в селезёнке, печени и лёгких и значительно улучшали выживаемость по сравнению с нелечеными контролями. Защита наблюдалась независимо от того, сталкивался ли донор с ЦМВ ранее, что отражает человеческое наблюдение: предшествующее заражение ЦМВ не обязательно для получения эффективных DOT‑клеток.
Разработано для работы вместе с препаратами после трансплантации
Главная проблема для любой послетрансплантационной терапии — сможет ли она функционировать на фоне стандартных иммуносупрессивных препаратов. Исследователи выращивали человеческие DOT‑клетки в присутствии часто используемых средств, таких как такролимус, циклоспорин, эверолимус и микофенолат. Хотя антипролиферативный микофенолат фактически останавливал рост и функцию DOT‑клеток, такролимус, циклоспорин, эверолимус и типичные дозы стероидов позволяли клеткам выживать, делиться и всё ещё секретировать интерферон‑γ в ответ на инфицированные ЦМВ мишени. Это говорит о том, что при режимах, уже применяемых у пациентов с тяжёлым ЦМВ‑заболеванием — часто основанных на ингибиторах кальциневрина с уменьшенными или модифицированными партнёрами — терапия DOT‑клетками могла бы оставаться активной.
Что это может значить для пациентов
Для неспециалиста ключевой вывод таков: учёные создали тип иммунных клеток, которые можно вырастить в больших количествах, которые не зависят от строгой совместимости донора и реципиента и которые способны распознавать и сдерживать ЦМВ способами, дополняющими противовирусные препараты. В культурах клеток и на мышиных моделях эти DOT γδ Т‑клетки направляются в инфицированные ткани, сдерживают распространение вируса и остаются функциональными несмотря на обычные трансплантационные лекарства. Работа прокладывает путь к ранним клиническим испытаниям у реципиентов трансплантатов с рецидивирующим, рефрактерным или лекарственно‑резистентным ЦМВ, с долгосрочной целью превратить опасное послетрансплантационное осложнение в контролируемое состояние с помощью усиленного собственного иммунитета пациента.
Цитирование: Marsères, G., Gentil, C., Tinevez, C. et al. Adoptive γδ T cell therapy controls cytomegalovirus infection in preclinical transplantation models. Nat Commun 17, 2847 (2026). https://doi.org/10.1038/s41467-026-69538-2
Ключевые слова: цитомегаловирус, гамма-дельта Т-клетки, клеточная терапия, трансплантация органов, иммунотерапия