Clear Sky Science · nl
Adoptieve γδ-T-celtherapie beheerst cytomegalovirusinfectie in preklinische transplantatiemodellen
Nieuwe hoop tegen een verborgen virus
Cytomegalovirus, of CMV, is een veelvoorkomend virus dat de meeste gezonde mensen nauwelijks merken. Voor patiënten die een orgaan of beenmergtransplantatie hebben gekregen, kan CMV echter levensbedreigend zijn en met alleen geneesmiddelen moeilijk te behandelen. Deze studie onderzoekt een nieuw type immuunceltherapie, gebaseerd op een zeldzame T-celsubtype genaamd gamma-delta T-cellen, bedoeld om het lichaam te helpen CMV onder controle te houden wanneer standaardbehandelingen falen. Het werk suggereert een route naar een universele, kant-en-klare celtherapie die enkele van de meest kwetsbare transplantatieontvangers zou kunnen beschermen.
Waarom CMV zo gevaarlijk is na transplantatie
Na een transplantatie gebruiken patiënten krachtige medicijnen om te voorkomen dat hun immuunsysteem het nieuwe orgaan of de donorcellen afstoot. Diezelfde medicijnen verzwakken de afweer tegen infecties. CMV is daarbij bijzonder zorgwekkend: het is de meest voorkomende opportunistische infectie na transplantatie van vaste organen en een groot probleem na stamceltransplantaties. Hoogrisicopatiënten, zoals degenen die nog nooit in contact zijn geweest met CMV maar een orgaan ontvangen van een CMV-positieve donor, krijgen vaak terugkerende of geneesmiddelresistente infecties. Nieuwe antivirale middelen zoals maribavir helpen, maar veel patiënten weten het virus niet volledig uit te schakelen of krijgen snel een terugval. Omdat langdurige controle van CMV afhangt van een blijvende immuunrespons, wenden onderzoekers zich tot celtherapieën om antivirale immuniteit te herbouwen in plaats van het virus alleen tijdelijk te onderdrukken.
Een ander soort immuunceltherapie
Bestaande experimentele celtherapieën voor CMV berusten voornamelijk op conventionele alfa-bèta T-cellen, die virusfragmenten alleen herkennen wanneer die worden gepresenteerd door specifieke weefsel-compatibele moleculen. Deze eis beperkt wie een bepaald celproduct kan ontvangen en maakt de productie complex. Gamma-delta T-cellen daarentegen kunnen gestreste of geïnfecteerde cellen detecteren zonder die strikte matching. Het team concentreerde zich op een subset genaamd Vδ2-negatieve gamma-delta T-cellen, die van nature uitbreiden tijdens CMV-infectie en geïnfecteerde cellen kunnen aanvallen. Met behulp van een klinisch-geschikt protocol bekend als de “Delta One T” (DOT)-methode lieten ze zien dat deze cellen in grote aantallen kunnen worden gekweekt van zowel CMV-positieve als CMV-negatieve donors, en zelfs van niertransplantatieontvangers met hoog risico, ondanks lage lymfocytaantallen en voortdurende immunosuppressie.
Hoe DOT-cellen CMV waarnemen en beheersen
In laboratoriumtests werden DOT-cellen gemengd met menselijke cellen die geïnfecteerd waren met klinische CMV-stammen. De uitgezette gamma-delta T-cellen vertoonden twee belangrijke gedragingen: ze degranuleerden, een teken van directe killing, en ze scheidden grote hoeveelheden interferon-gamma af, een krachtig antiviraal cytokine dat helpt de virusreplicatie te stoppen en andere immuuncellen mobiliseert. Deze reacties waren sterk specifiek voor CMV en traden niet op bij verwante virussen zoals herpes simplex of varicella-zoster. Belangrijk was dat DOT-cellen de verspreiding van CMV door fibroblastculturen dosisafhankelijk vertraagden: hoe meer effectorcellen werden toegevoegd, hoe sterker het effect. Onverwacht vonden de onderzoekers dat deze herkenning niet de gebruikelijke gamma-delta T-celreceptor vereiste. In plaats daarvan fungeerde een adhesiemolecuul genaamd LFA-1, dat bindt aan ICAM-1 op geïnfecteerde cellen, als een cruciale co-stimulator: het blokkeren van LFA-1 of ICAM-1 verminderde de interferon-gamma-afgifte sterk, terwijl kunstmatige activatie van LFA-1 krachtige reacties opwekte.
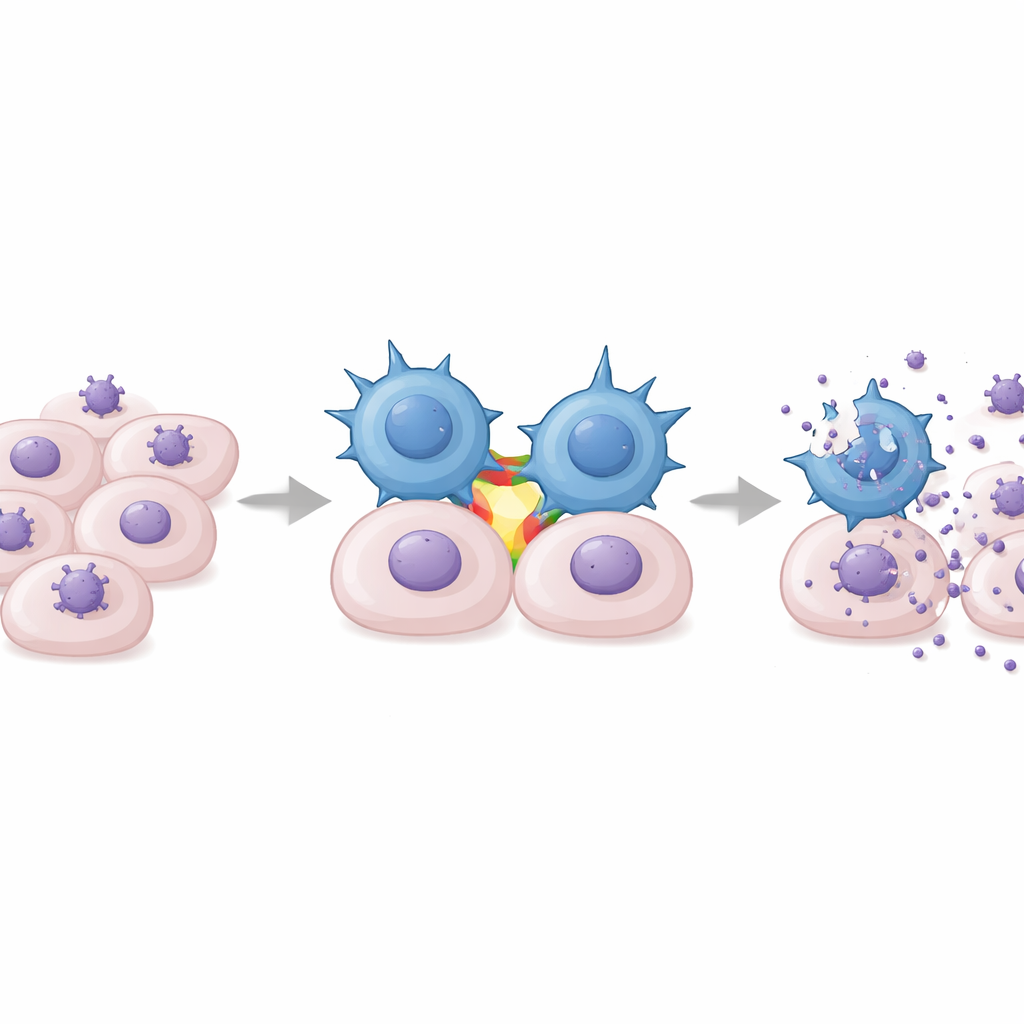
Bewijs van bescherming in een muismodel
Aangezien humaan CMV muizen niet infecteert, bouwde het team een diermodel met murien CMV en muizengamma-delta T-cellen die waren uitgebreid met een DOT-achtig protocol. Deze muizencellen kregen een vergelijkbaar geactiveerd, cytotoxisch profiel. Wanneer ze werden overgedragen aan ernstig immuungecompromitteerde muizen die met murien CMV waren geïnfecteerd, migreerden de uitgebreide gamma-delta T-cellen naar sleutelorganen, verminderden ze virale ladingen in milt, lever en longen, en verbeterden ze de overleving significant vergeleken met onbehandelde controles. Bescherming werd waargenomen ongeacht of donormuizen eerder CMV hadden doorgemaakt, wat het menselijke resultaat weerspiegelt dat eerdere CMV-blootstelling niet vereist is om effectieve DOT-cellen te genereren.
Ontworpen om samen te werken met transplantatiemedicatie
Een belangrijke zorg voor elke therapie na transplantatie is of deze kan functioneren in aanwezigheid van standaard immunosuppressieve geneesmiddelen. De onderzoekers kweekten menselijke DOT-cellen met vaak gebruikte middelen zoals tacrolimus, cyclosporine, everolimus en mycophenolaat. Terwijl het antiproliferatieve middel mycophenolaat de groei en functie van DOT-cellen vrijwel stopzette, lieten tacrolimus, cyclosporine, everolimus en gebruikelijke doses steroïden de cellen overleven, delen en nog steeds interferon-gamma afscheiden als reactie op CMV-geïnfecteerde doelwitten. Dit suggereert dat, onder regimens die al worden gebruikt voor patiënten met ernstige CMV-ziekte — vaak gebaseerd op calcineurineremmers met aangepaste of verminderde partners — DOT-celtherapie actief zou kunnen blijven.
Wat dit voor patiënten kan betekenen
Voor niet-specialisten is de kernboodschap dat wetenschappers een type immuuncel hebben ontwikkeld dat in grote aantallen kan worden gekweekt, niet afhankelijk is van strikte donor–ontvanger-matching, en CMV kan herkennen en beperken op manieren die antivirale geneesmiddelen aanvullen. In celkweken en muismodellen zoeken deze DOT gamma-delta T-cellen geïnfecteerde weefsels op, remmen ze virusverspreiding en blijven ze functioneel ondanks veelgebruikte transplantatiemedicatie. Het werk legt de basis voor vroege klinische proeven bij transplantatieontvangers met terugkerende, refractaire of geneesmiddelresistente CMV, met als langetermijndoel een gevaarlijke post-transplantatiecomplicatie te veranderen in een beheersbare toestand met behulp van het eigen immuunsysteem van de patiënt, versterkt.
Bronvermelding: Marsères, G., Gentil, C., Tinevez, C. et al. Adoptive γδ T cell therapy controls cytomegalovirus infection in preclinical transplantation models. Nat Commun 17, 2847 (2026). https://doi.org/10.1038/s41467-026-69538-2
Trefwoorden: cytomegalovirus, gamma-delta T-cellen, celtherapie, orgaantransplantatie, immunotherapie