Clear Sky Science · ar
علاج بالخلايا التائية γδ المُتبَنَّى يسيطر على عدوى الفيروس المضخم للخلايا في نماذج زراعة قبل سريرية
أمل جديد ضد فيروس خفي
الفيروس المضخم للخلايا، أو CMV، هو فيروس شائع لا يكاد يشعر به معظم الأصحاء. بالنسبة للمرضى الذين خضعوا لزرع عضو أو نخاع عظمي، قد يكون CMV مهدِّدًا للحياة وصعب العلاج بالأدوية وحدها. تستكشف هذه الدراسة نوعًا جديدًا من العلاجات الخلوية المناعية، قائمًا على نوع نادر من خلايا T يُدعى خلايا غاما-دلتا، مصممًا لمساعدة الجسم على السيطرة على CMV عندما تفشل العلاجات القياسية. تقترح النتائج مسارًا نحو علاج خلوية عام، جاهز للاستخدام، قد يحمي بعض المتلقين الأكثر عرضة للخطر بعد الزراعة.
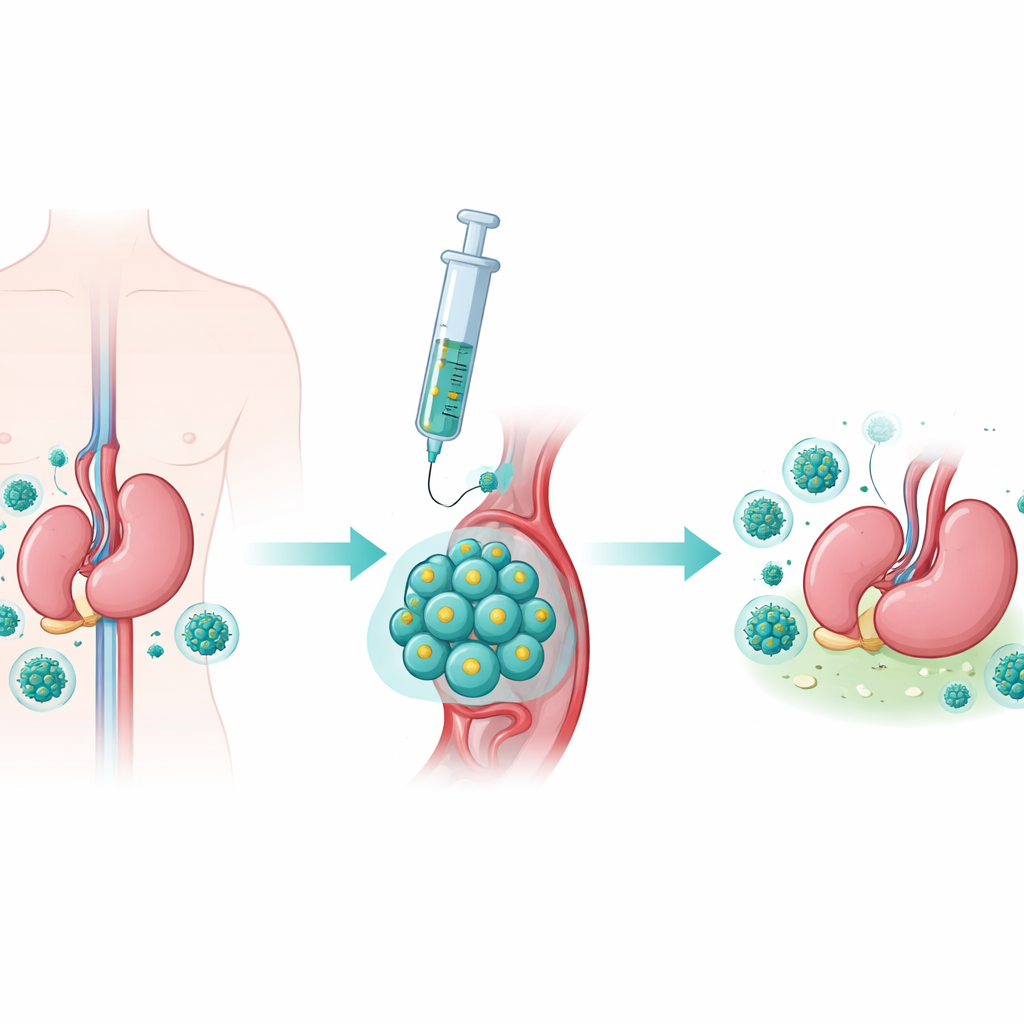
لماذا CMV خطير بعد الزرع
بعد الزرع، يتناول المرضى أدوية قوية لمنع جهازهم المناعي من رفض العضو الجديد أو خلايا المتبرع. هذه الأدوية نفسها تُضعف الدفاعات ضد العدوى. يشكل CMV مصدر قلق خاص: فهو أكثر العدوى الانتهازية تكرارًا بعد زرع الأعضاء الصلبة ومشكلة كبيرة بعد زرع الخلايا الجذعية. المرضى ذوو المخاطر العالية، مثل أولئك الذين لم يسبق لهم التعرض لـCMV لكنهم استلموا عضوًا من متبرع حامل للفيروس، يعانون غالبًا من عدوى متكررة أو مقاومة للأدوية. تساعد الأدوية المضادة للفيروسات الجديدة مثل ماريبافير، لكن العديد من المرضى لا يتخلصون تمامًا من الفيروس أو ينتكسون لاحقًا. بما أن السيطرة الطويلة الأمد على CMV تعتمد على استجابة مناعية مستمرة، يتجه الباحثون إلى العلاجات الخلوية لإعادة بناء المناعة المضادة للفيروسات بدلًا من مجرد كبح الفيروس مؤقتًا.
نوع مختلف من العلاج الخلوي المناعي
تعتمد العلاجات الخلوية التجريبية الحالية لـCMV أساسًا على خلايا T التقليدية ألفا-بيتا، التي تتعرف على شظايا الفيروس فقط عندما تُعرَض بواسطة جزيئات توافق نسيجية محددة. هذا المطلب يحد من المستفيدين من منتج خلوي معين ويُعقِّد التصنيع. خلايا غاما-دلتا، بالمقابل، يمكنها استشعار الخلايا المتوترة أو المصابة دون هذا التطابق الصارم. ركز الفريق على مجموعة فرعية تُدعى خلايا Vδ2 السالبة من غاما-دلتا، التي تتوسع طبيعيًا أثناء عدوى CMV ويمكنها مهاجمة الخلايا المصابة. باستخدام بروتوكول بمعايير سريرية يعرف باسم طريقة «دلتا واحد تي» (DOT)، أظهروا أنه يمكن تكاثر هذه الخلايا إلى أعداد كبيرة من متبرعين حاملين وغير حاملين لـCMV، ومن مستقبلين كلويين ذوي مخاطر عالية بأنفسهم، على الرغم من انخفاض أعداد اللمفاويات واستمرار التثبيط المناعي.
كيف تستشعر خلايا DOT وتسيطر على CMV
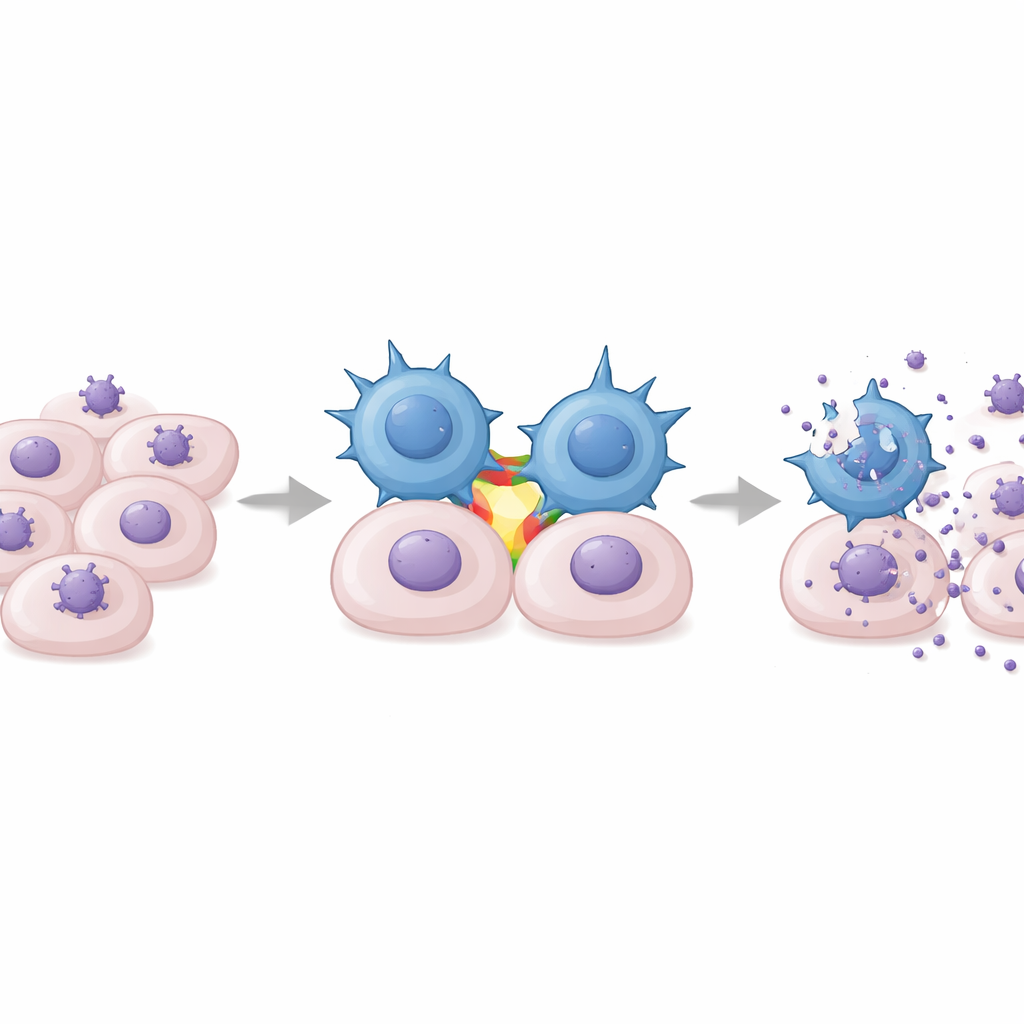
في اختبارات مخبرية، خُلطت خلايا DOT مع خلايا بشرية مُصابة بسلالات CMV السريرية. أظهرت خلايا غاما-دلتا الموسعة سلوكان رئيسيان: فرز الحبيبات، وهو علامة على القتل المباشر، وإفراز كميات كبيرة من الإنترفيرون-غاما، السيتوكين المضاد للفيروسات القوي الذي يحد من تكاثر الفيروس ويستدعي خلايا مناعية أخرى. كانت هذه الاستجابات محددة بشدة لـCMV ولم تظهر مع فيروسات قريبة مثل الهربس البسيط أو الحماق المنطقي. والأهم أن خلايا DOT أبطأت انتشار CMV عبر مزروعات الأرومة الليفية بطريقة تعتمد على الجرعة، فتصاعد التأثير مع زيادة عدد الخلايا الفعالة. وبشكل غير متوقع، وجد الباحثون أن هذا التعرف لم يتطلب مستقبل خلايا غاما-دلتا الاعتيادي. بدلًا من ذلك، عمل جزيء لاصق يدعى LFA-1، الذي يرتبط بـICAM-1 على الخلايا المصابة، كمحفز مساعد حاسم: حجب LFA-1 أو ICAM-1 قلل بشدة من إفراز الإنترفيرون-غاما، بينما أدى تفعيل LFA-1 اصطناعيًا إلى استجابات قوية.
دليل الحماية في نموذج فأري
نظرًا لأن CMV البشري لا يصيب الفئران، بنى الفريق نموذجًا حيوانيًا باستخدام CMV الفأري وخلايا غاما-دلتا الفأرية الموسعة ببروتوكول شبيه بDOT. اكتسبت هذه الخلايا الفأرية نمطًا مشابهًا من النشاط والسمية الخلوية. عند نقلها إلى فئران شديدة القصور المناعي مُصابة بـCMV الفأري، هاجرت خلايا غاما-دلتا الموسعة إلى أعضاء رئيسية، وخفضت الأحمال الفيروسية في الطحال والكبد والرئتين، وحسّنت البقاء على قيد الحياة بشكل ملحوظ مقارنة بالمجموعة الضابطة غير المعالجة. لوحظت الحماية سواء كان المتبرع الفأري قد تعرض سابقًا لـCMV أم لا، مما يعكس النتيجة البشرية بأن التعرض السابق لـCMV غير مطلوب لتوليد خلايا DOT فعّالة.
مصممة للعمل جنبًا إلى جنب مع أدوية الزرع
مخاوف رئيسية لأي علاج ما بعد الزرع هي ما إذا كان يستطيع العمل في وجود أدوية التثبيط المناعي القياسية. زرع الباحثون خلايا DOT بشرية مع عوامل مستخدمة شائعة مثل تاكروليموس، وسيكلوسبورين، وإيفروليموس، وميكوفينولات. بينما أوقف الدواء المضاد للتكاثر ميكوفينولات نمو خلايا DOT ووظيفتها عمليًا، سمحت أدوية مثل تاكروليموس، وسيكلوسبورين، وإيفروليموس، وجرعات الستيرويدات المعتادة للخلايا بالبقاء والانقسام وما زالت تفرز الإنترفيرون-غاما استجابةً لأهداف مصابة بـCMV. يشير هذا إلى أنه، تحت أنظمة علاجية مستخدمة حاليًا للمرضى ذوي CMV الحاد—التي غالبًا ما تعتمد على مثبطات الكالسينيفرين مع شركاء معدلين أو مخفضين—قد تظل خلايا DOT نشطة.
ماذا قد يعني هذا للمرضى
لغير المتخصص، الرسالة الأساسية هي أن العلماء طوروا نوعًا من الخلايا المناعية يمكن تكاثره بأعداد كبيرة، ولا يعتمد على تطابق صارم بين المتبرع والمستلم، ويمكنه التعرف على CMV وكبحه بطرق تكمل الأدوية المضادة للفيروسات. في مزروعات خلوية ونماذج فأرية، تتوجه هذه الخلايا غاما-دلتا DOT إلى الأنسجة المصابة، وتحد من انتشار الفيروس، وتبقى فعّالة رغم أدوية الزرع الشائعة. تضع هذه النتائج الأساس لتجارب طور مبكّر في مرضى الزرع الذين يعانون CMV متكررًا أو مقاومًا للعلاج، مع الهدف الطويل الأمد بجعل هذه المضاعفة ما بعد الزرع التي قد تكون خطيرة حالة يمكن التحكم بها بواسطة جهاز المريض المناعي المعزَّز.
الاستشهاد: Marsères, G., Gentil, C., Tinevez, C. et al. Adoptive γδ T cell therapy controls cytomegalovirus infection in preclinical transplantation models. Nat Commun 17, 2847 (2026). https://doi.org/10.1038/s41467-026-69538-2
الكلمات المفتاحية: الفيروس المضخم للخلايا, خلايا تي غاما-دلتا, علاج خلوية, زرع الأعضاء, العلاج المناعي