Clear Sky Science · de
Adoptive γδ-T-Zelltherapie kontrolliert Cytomegalovirus-Infektion in präklinischen Transplantationsmodellen
Neue Hoffnung gegen ein verborgendes Virus
Das Cytomegalovirus, kurz CMV, ist ein weit verbreitetes Virus, das bei den meisten gesunden Menschen kaum bemerkt wird. Für Patientinnen und Patienten, die ein Organ oder Knochenmark transplantiert bekommen haben, kann CMV jedoch lebensbedrohlich sein und sich oft nur schwer allein mit Medikamenten kontrollieren lassen. Diese Studie untersucht eine neue Form der Immunzelltherapie, basierend auf einer seltenen T‑Zell‑Untergruppe, den gamma‑delta‑T‑Zellen, die dem Körper helfen soll, CMV zu kontrollieren, wenn Standardtherapien versagen. Die Arbeit weist einen Weg zu einer universellen, sofort verfügbaren Zelltherapie, die einige der verletzlichsten Transplantatempfänger schützen könnte.
Warum CMV nach Transplantation so gefährlich ist
Nach einer Transplantation nehmen Patientinnen und Patienten starke Medikamente ein, um eine Abstoßung des neuen Organs oder der Spenderzellen zu verhindern. Dieselben Medikamente schwächen aber auch die Abwehr gegen Infektionen. CMV ist dabei besonders besorgniserregend: Es ist die häufigste opportunistische Infektion nach solider Organtransplantation und ein großes Problem nach Stammzelltransplantationen. Hochrisikopatienten, etwa solche, die selbst nie CMV hatten, aber ein Organ von einem CMV‑positiven Spender erhalten, leiden häufig unter wiederkehrenden oder medikamentenresistenten Infektionen. Neue antivirale Wirkstoffe wie Maribavir helfen, doch viele Patienten schaffen es nicht, das Virus vollständig zu eliminieren, oder erleiden bald einen Rückfall. Da die langfristige Kontrolle von CMV von einer anhaltenden Immunantwort abhängt, wenden sich Forscher Zelltherapien zu, um die antivirale Immunität wiederaufzubauen, statt das Virus nur vorübergehend zu unterdrücken.
Eine andere Art der Immunzelltherapie
Bisherige experimentelle Zelltherapien gegen CMV beruhen hauptsächlich auf konventionellen alpha‑beta‑T‑Zellen, die Virusfragmente nur erkennen, wenn sie von bestimmten, gewebeangepassten Molekülen präsentiert werden. Diese Voraussetzung schränkt ein, wer ein bestimmtes Zellprodukt erhalten kann, und macht die Herstellung kompliziert. Gamma‑delta‑T‑Zellen hingegen können gestresste oder infizierte Zellen ohne diese strikte Übereinstimmung wahrnehmen. Das Team konzentrierte sich auf eine Untergruppe, die Vδ2‑negativen gamma‑delta‑T‑Zellen, die sich während einer CMV‑Infektion natürlicherweise ausbreiten und infizierte Zellen angreifen können. Mit einem klinisch verwendbaren Protokoll, bekannt als „Delta One T“ (DOT)-Methode, zeigten sie, dass sich diese Zellen sowohl aus CMV‑positiven als auch CMV‑negativen Spendern sowie aus Hochrisiko‑Nierentransplantatempfängern selbst in großer Zahl züchten lassen, trotz niedriger Lymphozytenzahlen und andauernder Immunsuppression.
Wie DOT‑Zellen CMV erkennen und kontrollieren
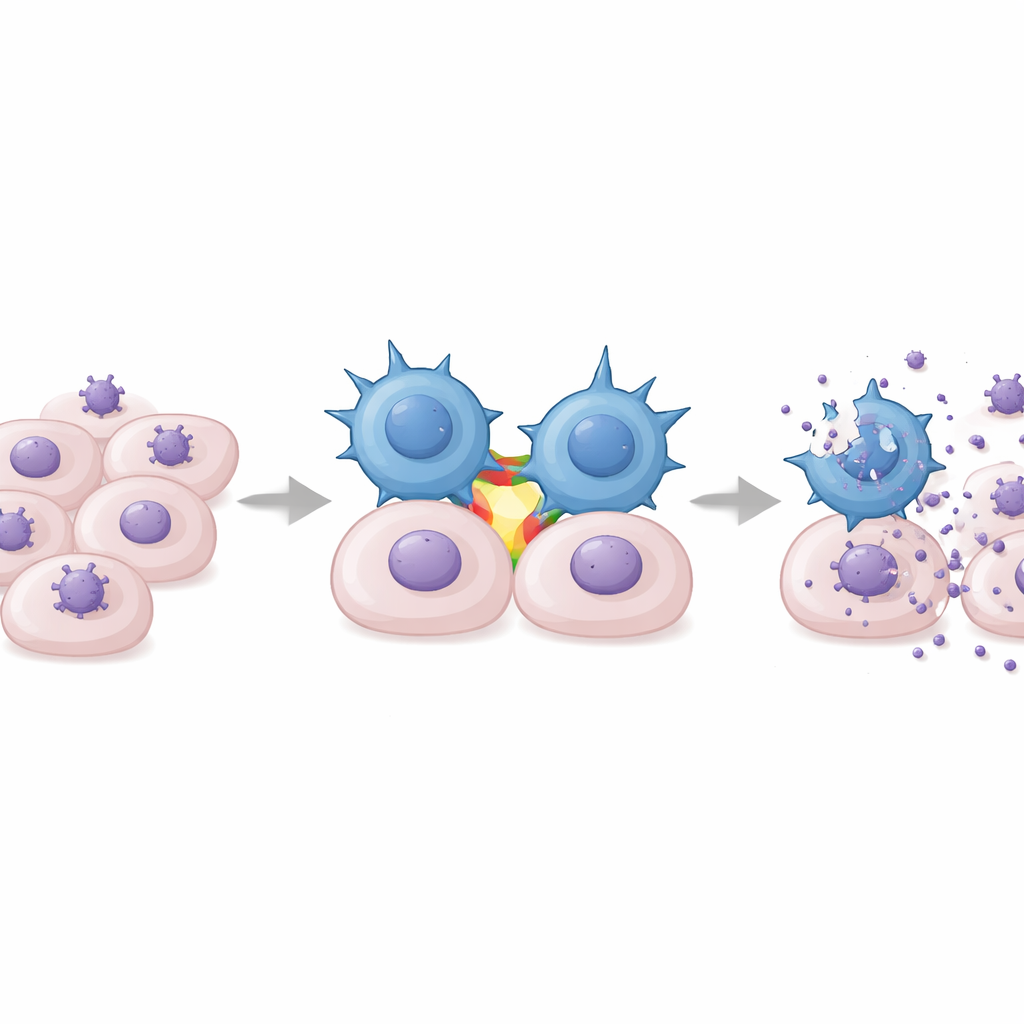
In Labortests wurden DOT‑Zellen mit menschlichen Zellen vermischt, die mit klinischen CMV‑Stämmen infiziert waren. Die expandierten gamma‑delta‑T‑Zellen zeigten zwei zentrale Verhaltensweisen: Sie degranulierten, ein Zeichen direkter Abtötung, und sie sezernierten große Mengen Interferon‑gamma, ein starkes antivirales Zytokin, das die virale Replikation hemmt und weitere Immunzellen aktiviert. Diese Reaktionen waren hochspezifisch für CMV und traten nicht mit verwandten Viren wie Herpes simplex oder Varizella‑zoster auf. Wichtig ist, dass DOT‑Zellen die Ausbreitung von CMV in Fibroblastenkulturen dosisabhängig verlangsamten und mit zunehmender Zahl von Effektorzellen stärker wirkten. Unerwartet stellten die Forschenden fest, dass diese Erkennung nicht den üblichen gamma‑delta‑T‑Zellrezeptor erforderte. Stattdessen fungierte ein Adhäsionsmolekül namens LFA‑1, das an ICAM‑1 auf infizierten Zellen bindet, als wesentlicher Kofaktor: Das Blockieren von LFA‑1 oder ICAM‑1 reduzierte die Interferon‑gamma‑Freisetzung deutlich, während eine künstliche Aktivierung von LFA‑1 starke Reaktionen auslöste.
Schutznachweis in einem Mausmodell
Weil humanes CMV Mäuse nicht infiziert, baute das Team ein Tiermodell mit murinem CMV und murinen gamma‑delta‑T‑Zellen, die mit einem DOT‑ähnlichen Protokoll expandiert wurden. Diese Maus‑Zellen entwickelten ein ähnliches aktiviertes, zytotoxisches Profil. Nach Transfer in schwer immundefiziente Mäuse, die mit murinem CMV infiziert waren, wanderten die expandierten gamma‑delta‑T‑Zellen in wichtige Organe, reduzierten die Viruslasten in Milz, Leber und Lunge und verbesserten das Überleben im Vergleich zu unbehandelten Kontrollen deutlich. Der Schutz trat sowohl bei Spendermäusen mit vorheriger CMV‑Exposition als auch bei naiven Spendern auf, was das humane Ergebnis widerspiegelt, dass eine vorherige CMV‑Exposition nicht erforderlich ist, um effektive DOT‑Zellen zu erzeugen.
Entwickelt, um mit Transplantationsmedikamenten zusammenzuarbeiten
Eine zentrale Frage für jede Therapie nach Transplantation ist, ob sie in Gegenwart gängiger Immunsuppressiva funktionieren kann. Die Forschenden kultivierten humane DOT‑Zellen mit häufig verwendeten Wirkstoffen wie Tacrolimus, Cyclosporin, Everolimus und Mycophenolat. Während das antiproliferative Mycophenolat das Wachstum und die Funktion der DOT‑Zellen praktisch zum Erliegen brachte, erlaubten Tacrolimus, Cyclosporin, Everolimus und typische Kortisondosen den Zellen zu überleben, sich zu teilen und weiterhin Interferon‑gamma als Reaktion auf CMV‑infizierte Zielzellen zu sezernieren. Dies deutet darauf hin, dass DOT‑Zelltherapie unter Regimen, die bereits bei Patientinnen und Patienten mit schwerer CMV‑Erkrankung verwendet werden—oft auf Calcineurin‑Inhibitoren mit reduzierten oder modifizierten Begleitmedikamenten basierend—aktiv bleiben könnte.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht‑Spezialisten lautet die zentrale Botschaft: Forschende haben eine Art Immunzelle entwickelt, die in großen Mengen gezüchtet werden kann, nicht auf eine strikte Spender‑Empfänger‑Übereinstimmung angewiesen ist und CMV auf Weisen erkennt und eindämmt, die antivirale Medikamente sinnvoll ergänzen. In Zellkulturen und Mausmodellen wandern diese DOT‑gamma‑delta‑T‑Zellen in infizierte Gewebe, bremsen die Virusausbreitung und bleiben trotz üblicher Transplantationsmedikamente funktionstüchtig. Die Arbeit bereitet den Boden für frühe klinische Studien bei Transplantatempfängern mit rezidivierendem, refraktärem oder medikamentenresistentem CMV, mit dem langfristigen Ziel, eine gefährliche Komplikation nach Transplantation durch Verstärkung des eigenen Immunsystems der Patientinnen und Patienten beherrschbar zu machen.
Zitation: Marsères, G., Gentil, C., Tinevez, C. et al. Adoptive γδ T cell therapy controls cytomegalovirus infection in preclinical transplantation models. Nat Commun 17, 2847 (2026). https://doi.org/10.1038/s41467-026-69538-2
Schlüsselwörter: Cytomegalovirus, gamma-delta T-Zellen, Zelltherapie, Organtransplantation, Immuntherapie