Clear Sky Science · es
Terapia adoptiva con células T γδ controla la infección por citomegalovirus en modelos preclínicos de trasplante
Nueva esperanza contra un virus oculto
El citomegalovirus, o CMV, es un virus común que la mayoría de las personas sanas apenas nota. Sin embargo, para los pacientes que han recibido un órgano trasplantado o médula ósea, el CMV puede ser potencialmente mortal y difícil de tratar solo con fármacos. Este estudio explora un nuevo tipo de terapia con células inmunitarias, basada en un subtipo raro de linfocitos T llamado células T gamma-delta, diseñada para ayudar al organismo a controlar el CMV cuando los tratamientos estándar fallan. El trabajo sugiere un camino hacia una terapia celular universal y lista para usar que podría proteger a algunos de los receptores de trasplante más vulnerables.
Por qué el CMV es tan peligroso tras un trasplante
Tras un trasplante, los pacientes toman medicamentos potentes para evitar que su sistema inmunitario rechace el nuevo órgano o las células del donante. Esos mismos medicamentos debilitan las defensas frente a las infecciones. El CMV es particularmente preocupante: es la infección oportunista más frecuente después de un trasplante de órgano sólido y un problema mayor tras los trasplantes de células madre. Los pacientes de alto riesgo, como aquellos que nunca han estado expuestos al CMV pero reciben un órgano de un donante CMVpositivo, con frecuencia sufren infecciones recurrentes o resistentes a los fármacos. Nuevos antivirales como maribavir ayudan, pero muchos pacientes aún no eliminan completamente el virus o recaen poco después. Dado que el control a largo plazo del CMV depende de una respuesta inmunitaria sostenida, los investigadores se están orientando hacia terapias celulares para reconstruir la inmunidad antiviral en lugar de solo suprimir temporalmente el virus.
Un tipo distinto de terapia con células inmunitarias
Las terapias celulares experimentales existentes para el CMV se basan principalmente en linfocitos T convencionales alfa‑beta, que reconocen fragmentos virales solo cuando se muestran mediante moléculas de compatibilidad tisular específicas. Este requisito limita quién puede recibir un producto celular concreto y complica la fabricación. Las células T gamma‑delta, en cambio, pueden detectar células estresadas o infectadas sin esa coincidencia estricta. El equipo se centró en un subconjunto denominado células T gamma‑delta Vδ2‑negativas, que se expanden de forma natural durante la infección por CMV y pueden atacar células infectadas. Usando un protocolo de grado clínico conocido como método “Delta One T” (DOT), demostraron que estas células pueden multiplicarse hasta obtener grandes cantidades tanto de donantes CMV‑positivos como CMV‑negativos, y también a partir de receptores de trasplante renal de alto riesgo, a pesar de contar con recuentos bajos de linfocitos y con inmunosupresión en curso.
Cómo las células DOT detectan y controlan el CMV
En pruebas de laboratorio, mezclaron células DOT con células humanas infectadas por cepas clínicas de CMV. Las células gamma‑delta expandidas mostraron dos comportamientos clave: desgranulación, indicativa de citotoxicidad directa, y secreción de grandes cantidades de interferón‑gamma, una citocina antiviral potente que ayuda a frenar la replicación viral y a reclutar a otras células inmunitarias. Estas respuestas fueron altamente específicas para CMV y no se produjeron con virus relacionados como el herpes simple o el varicela‑zóster. De forma importante, las células DOT ralentizaron la propagación del CMV en cultivos de fibroblastos de manera dependiente de la dosis, actuando con mayor intensidad al aumentar el número de células efectoras. De modo inesperado, los investigadores hallaron que este reconocimiento no requería el receptor habitual de las células T gamma‑delta. En su lugar, una molécula de adhesión llamada LFA‑1, que se une a ICAM‑1 en las células infectadas, actuó como coestimulador crucial: bloquear LFA‑1 o ICAM‑1 redujo marcadamente la liberación de interferón‑gamma, mientras que la activación artificial de LFA‑1 desencadenó respuestas intensas.
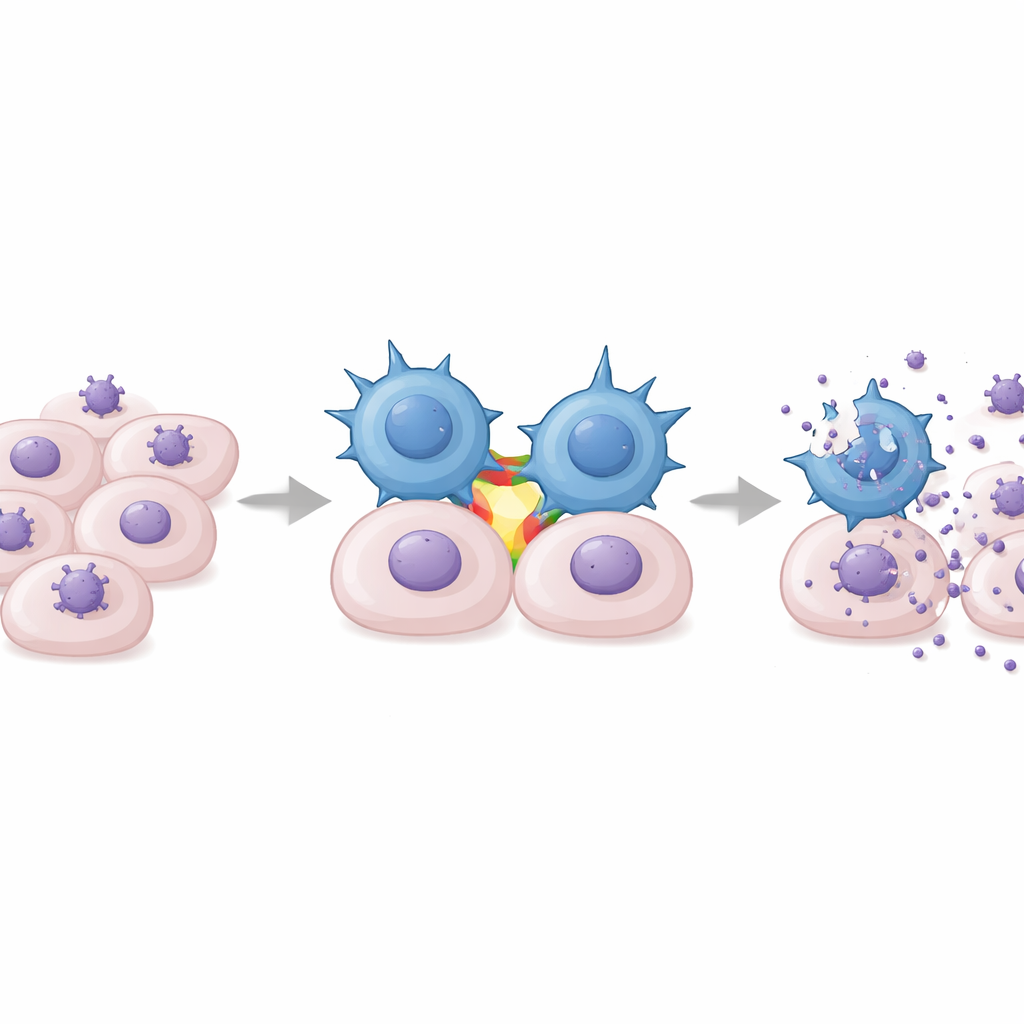
Prueba de protección en un modelo murino
Puesto que el CMV humano no infecta ratones, el equipo construyó un modelo animal usando citomegalovirus murino y células T gamma‑delta de ratón expandidas con un protocolo similar al DOT. Estas células murinas adquirieron un perfil activado y citotóxico similar. Cuando se transfirieron a ratones gravemente inmunodeprimidos infectados con CMV murino, las células gamma‑delta expandidas migraron a órganos clave, redujeron las cargas virales en bazo, hígado y pulmones, y mejoraron de forma significativa la supervivencia frente a controles no tratados. La protección se observó tanto si los ratones donantes habían estado expuestos previamente al CMV como si no, reflejando el hallazgo humano de que la exposición previa al CMV no es necesaria para generar células DOT efectivas.
Diseñadas para funcionar junto con los fármacos de trasplante
Una preocupación importante para cualquier terapia postrasplante es si puede funcionar en presencia de los fármacos inmunosupresores estándar. Los investigadores cultivaron células DOT humanas con agentes de uso común como tacrolimus, ciclosporina, everolimus y micofenolato. Mientras que el fármaco antiproliferativo micofenolato detuvo esencialmente el crecimiento y la función de las células DOT, tacrolimus, ciclosporina, everolimus y dosis habituales de esteroides permitieron que las células sobrevivieran, se dividieran y aun así secretaran interferón‑gamma en respuesta a objetivos infectados por CMV. Esto sugiere que, dentro de los regímenes ya usados en pacientes con enfermedad por CMV grave —a menudo basados en inhibidores de la calcineurina con socios reducidos o modificados— la terapia con células DOT podría permanecer activa.
Qué podría significar esto para los pacientes
Para un público no especializado, el mensaje clave es que los científicos han diseñado un tipo de célula inmunitaria que puede crecer en grandes cantidades, no depende de una coincidencia estricta entre donante y receptor, y puede reconocer y restringir el CMV de maneras que complementan a los antivirales. En cultivos celulares y modelos murinos, estas células T gamma‑delta DOT se dirigen a los tejidos infectados, frenan la propagación viral y mantienen su funcionalidad a pesar de los fármacos de trasplante habituales. El trabajo sienta las bases para ensayos clínicos en fase temprana en receptores de trasplante con CMV recurrente, refractario o resistente a fármacos, con el objetivo a largo plazo de convertir una complicación peligrosa postrasplante en una condición controlable mediante el refuerzo del propio sistema inmunitario del paciente.
Cita: Marsères, G., Gentil, C., Tinevez, C. et al. Adoptive γδ T cell therapy controls cytomegalovirus infection in preclinical transplantation models. Nat Commun 17, 2847 (2026). https://doi.org/10.1038/s41467-026-69538-2
Palabras clave: citomegalovirus, células T gamma-delta, terapia celular, trasplante de órganos, inmunoterapia