Clear Sky Science · pl
Adoptatywna terapia komórkami γδ kontroluje zakażenie cytomegalowirusem w przedklinicznych modelach transplantacyjnych
Nowa nadzieja przeciw ukrytemu wirusowi
Cytomegalowirus, w skrócie CMV, to powszechny wirus, który u większości zdrowych osób przechodzi niemal niezauważony. Dla pacjentów po przeszczepie narządu lub szpiku kostnego CMV może jednak mieć charakter zagrażający życiu i być trudny do wyleczenia samymi lekami. W tym badaniu badacze analizują nowy rodzaj terapii komórkowej opartej na rzadkim podtypie limfocytów T, zwanych komórkami gamma-delta, zaprojektowanej, by pomóc organizmowi kontrolować CMV, gdy standardowe metody zawodzą. Praca wskazuje drogę ku uniwersalnej, gotowej do użycia terapii komórkowej, która mogłaby chronić najbardziej narażonych biorców przeszczepów.
Dlaczego CMV jest tak niebezpieczny po przeszczepie
Po przeszczepie pacjenci przyjmują silne leki zapobiegające odrzuceniu nowego organu lub komórek dawcy. Te same leki osłabiają jednak obronę przed infekcjami. CMV budzi szczególny niepokój: jest najczęstszą infekcją oportunistyczną po przeszczepie narządów i poważnym problemem po transplantacji komórek macierzystych. Pacjenci wysokiego ryzyka, na przykład ci, którzy nigdy wcześniej nie mieli kontaktu z CMV, a otrzymują organ od dawcy CMV-dodatniego, często doświadczają nawrotów lub infekcji opornych na leki. Nowe leki przeciwwirusowe, takie jak maribawir, pomagają, ale wielu pacjentów nadal nie eliminuje wirusa całkowicie lub wkrótce dochodzi do nawrotu. Ponieważ długotrwała kontrola CMV zależy od utrzymującej się odpowiedzi immunologicznej, naukowcy zwracają się ku terapiom komórkowym, aby odbudować odporność przeciwwirusową zamiast jedynie czasowo tłumić wirusa.
Inny rodzaj terapii komórkowej
Dotychczasowe eksperymentalne terapie komórkowe przeciw CMV opierały się głównie na konwencjonalnych limfocytach T alfa-beta, które rozpoznają fragmenty wirusa tylko wtedy, gdy są one prezentowane przez określone, dopasowane cząsteczki tkankowe. Ten wymóg ogranicza krąg biorców danego produktu komórkowego i komplikuje produkcję. Komórki gamma-delta, przeciwnie, potrafią wykrywać komórki w stanie stresu lub zainfekowane bez tak rygorystycznego dopasowania. Zespół skupił się na podzbiorze zwanym komórkami Vδ2-ujemnymi gamma-delta, które naturalnie się rozszerzają podczas zakażenia CMV i potrafią atakować zainfekowane komórki. Stosując kliniczny protokół znany jako „Delta One T” (DOT), wykazali, że te komórki można wyhodować w dużych ilościach zarówno od dawców CMV-dodatnich, jak i CMV-ujemnych, a także od samych biorców wysokiego ryzyka po przeszczepie nerki, pomimo niskiej liczby limfocytów i trwającej immunosupresji.
Jak komórki DOT rozpoznają i kontrolują CMV
W testach laboratoryjnych komórki DOT mieszano z ludzkimi komórkami zainfekowanymi klinicznymi szczepami CMV. Rozszerzone komórki gamma-delta wykazały dwa kluczowe zachowania: degranulację, co świadczy o bezpośrednim zabijaniu, oraz wydzielanie dużych ilości interferonu‑gamma, silnego cytokiny przeciwwirusowej, która hamuje replikację wirusa i angażuje inne komórki układu odpornościowego. Odpowiedzi te były wyraźnie specyficzne dla CMV i nie występowały wobec pokrewnych wirusów, takich jak wirus opryszczki zwykłej czy wirus ospy wietrznej i półpaśca. Co ważne, komórki DOT spowalniały rozprzestrzenianie się CMV w hodowlach fibroblastów w sposób zależny od dawki — im więcej komórek efektorowych, tym silniejszy efekt. Niespodziewanie badacze odkryli, że to rozpoznanie nie wymagało zwykłego receptora komórek gamma-delta. Zamiast tego cząsteczka adhezyjna LFA‑1, która wiąże się z ICAM‑1 na zainfekowanych komórkach, pełniła rolę istotnego kostymulatora: blokada LFA‑1 lub ICAM‑1 ostro zmniejszała wydzielanie interferonu‑gamma, podczas gdy sztuczne pobudzenie LFA‑1 wywoływało silne reakcje.
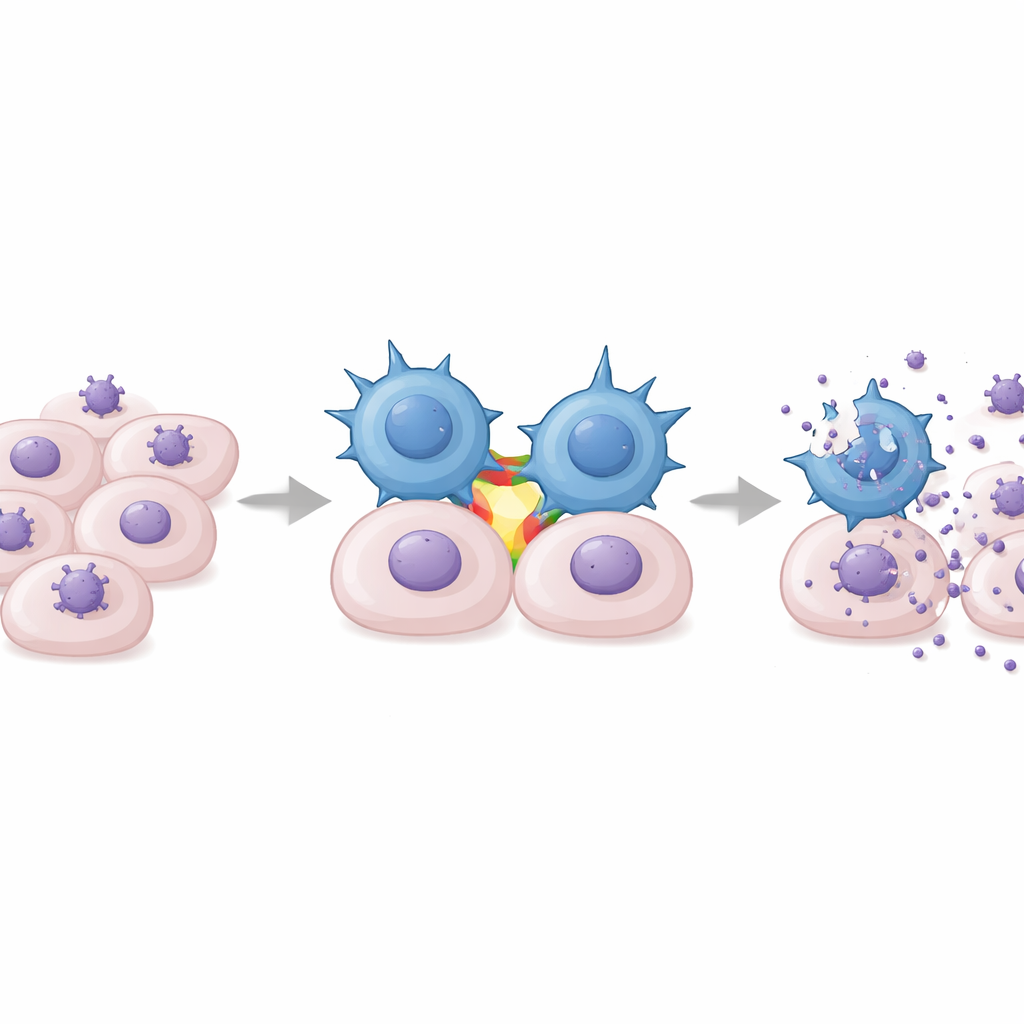
Dowód ochrony w modelu myszy
Ponieważ ludzki CMV nie infekuje myszy, zespół zbudował model zwierzęcy używając mysiowego CMV i mysich komórek gamma-delta rozszerzanych przy użyciu protokołu podobnego do DOT. Te mysie komórki nabrały podobnego aktywowanego, cytotoksycznego profilu. Po przeszczepieniu do ciężko immunodeficytnych myszy zainfekowanych mysiowym CMV, rozszerzone komórki gamma-delta migrowały do kluczowych narządów, zmniejszały ładunki wirusa w śledzionie, wątrobie i płucach oraz znacząco poprawiały przeżywalność w porównaniu z nieleczonymi kontrolami. Ochrona obserwowana była niezależnie od tego, czy myszy-dawcy wcześniej miały kontakt z CMV, co odzwierciedla wynik ludzki mówiący, że wcześniejsza ekspozycja na CMV nie jest wymagana do uzyskania efektywnych komórek DOT.
Projektowane, by działać razem z lekami przeszczepowymi
Głównym zmartwieniem każdej terapii po przeszczepie jest to, czy będzie ona funkcjonować w obecności standardowych leków immunosupresyjnych. Badacze hodowali ludzkie komórki DOT w obecności powszechnie stosowanych środków, takich jak takrolimus, cyklosporyna, ewerolimus i mykofenolan. Podczas gdy lek antyproliferacyjny mykofenolan w zasadzie zatrzymał wzrost i funkcję komórek DOT, takrolimus, cyklosporyna, ewerolimus i typowe dawki steroidów pozwalały komórkom przetrwać, dzielić się i nadal wydzielać interferon‑gamma w odpowiedzi na cele zainfekowane CMV. Sugeruje to, że w schematach już stosowanych u pacjentów z ciężką chorobą CMV — często opartych na inhibitorach kalcyneuryny przy zmniejszonych lub zmodyfikowanych partnerach — terapia komórkami DOT mogłaby pozostać aktywna.
Co to może znaczyć dla pacjentów
Dla osoby niebędącej specjalistą kluczowe przesłanie jest takie, że naukowcy opracowali rodzaj komórki odpornościowej, którą można wyhodować w dużych liczbach, która nie zależy od ścisłego dopasowania dawca–biorca i potrafi rozpoznawać oraz hamować CMV w sposób uzupełniający działanie leków przeciwwirusowych. W hodowlach komórkowych i modelach mysich te komórki DOT gamma-delta trafiają do zainfekowanych tkanek, ograniczają rozprzestrzenianie wirusa i pozostają funkcjonalne mimo powszechnych leków przeszczepowych. Praca ta tworzy podstawy do wczesnofazowych badań klinicznych u biorców przeszczepów z nawrotowym, opornym lub lekoopornym CMV, z długoterminowym celem przekształcenia groźnego powikłania po przeszczepie w stan możliwy do kontrolowania przy użyciu wzmocnionego własnego układu odpornościowego pacjenta.
Cytowanie: Marsères, G., Gentil, C., Tinevez, C. et al. Adoptive γδ T cell therapy controls cytomegalovirus infection in preclinical transplantation models. Nat Commun 17, 2847 (2026). https://doi.org/10.1038/s41467-026-69538-2
Słowa kluczowe: cytomegalowirus, komórki T gamma-delta, terapia komórkowa, przeszczep narządów, immunoterapia