Clear Sky Science · ru
Потеря Pum2 усугубляет колит, нарушая диалог макрофагов и эпителия и стимулируя некроптоз эпителиальных клеток
Почему это важно для людей с проблемами кишечника
Язвенный колит — хроническое заболевание, при котором слизистая ободочной кишки становится болезненно воспалённой и склонной к обострениям. Многие пациенты чередуют периоды спокойствия с внезапными приступами кровотечений, спазмами и неотложными позывами в туалет. В этом исследовании обнаружен ранее упущенный «тормоз» внутри иммунных и эпителиальных клеток кишечника — белок Pum2, который помогает сдерживать воспаление. Понимание работы этого внутреннего тормоза может указать новые пути для успокоения кишечника, защиты стенки кишечника и потенциально улучшения лечения язвенного колита.
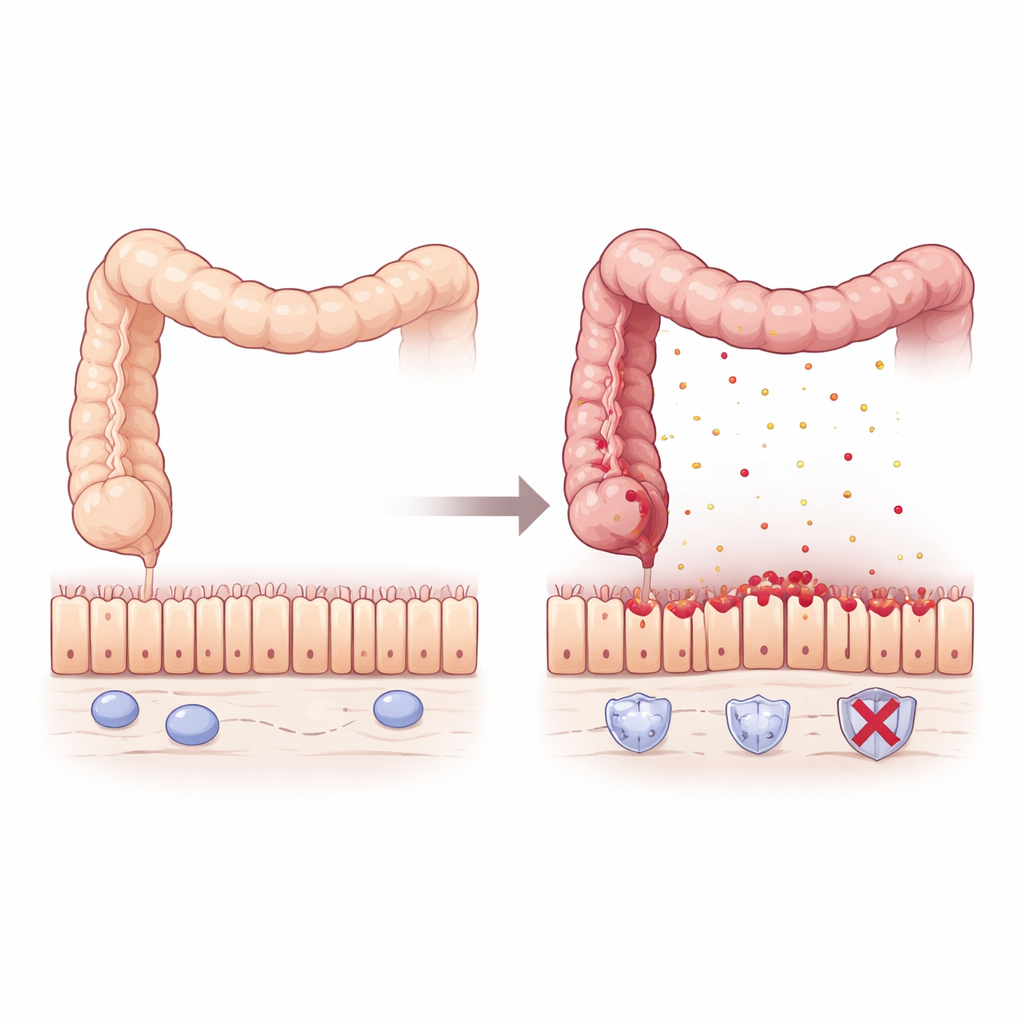
Тихий хранитель в воспалённом кишечнике
Исследователи начали с анализа больших массивов данных тканей пациентов с воспалительными заболеваниями кишечника и колоректальным раком. Они обнаружили, что уровни Pum2, белка, связывающего РНК и тонко регулирующего синтез других белков, последовательно снижались в участках активного воспаления толстой и прямой кишки. После заживления слизистой и лечения уровни Pum2 снова повышались, особенно у пациентов, у которых наступала стойкая ремиссия. Любопытно, что в опухолях кишечника, возникающих после длительного колита, Pum2 вновь включался до уровней, похожих на нормальные ткани, что намекает на разные роли этого белка при воспалении и при раке.
Когда тормоза нет, колит ухудшается
Чтобы понять последствия потери Pum2, команда использовала мышей, лишённых гена Pum2, и подвергла их действию химического вещества, вызывающего колит путём повреждения слизистой. По сравнению с нормальными мышами животные без Pum2 теряли больше веса, имели укороченные и более воспалённые ободочные кишки, увеличенные селезёнки и более высокую смертность. Микроскопическое исследование показало тяжёлое разрушение слизистой: деформированные железы и значительную инфильтрацию иммунных клеток. Ещё до явных признаков болезни генетический профиль показал, что ободочные кишки без Pum2 были «заранее настроены» на проблемы: они тихо вырабатывали больше хемокинов — сигнальных молекул, привлекающих воспалительные клетки, особенно тех, которые привлекают макрофаги, ключевой тип иммунных клеток.
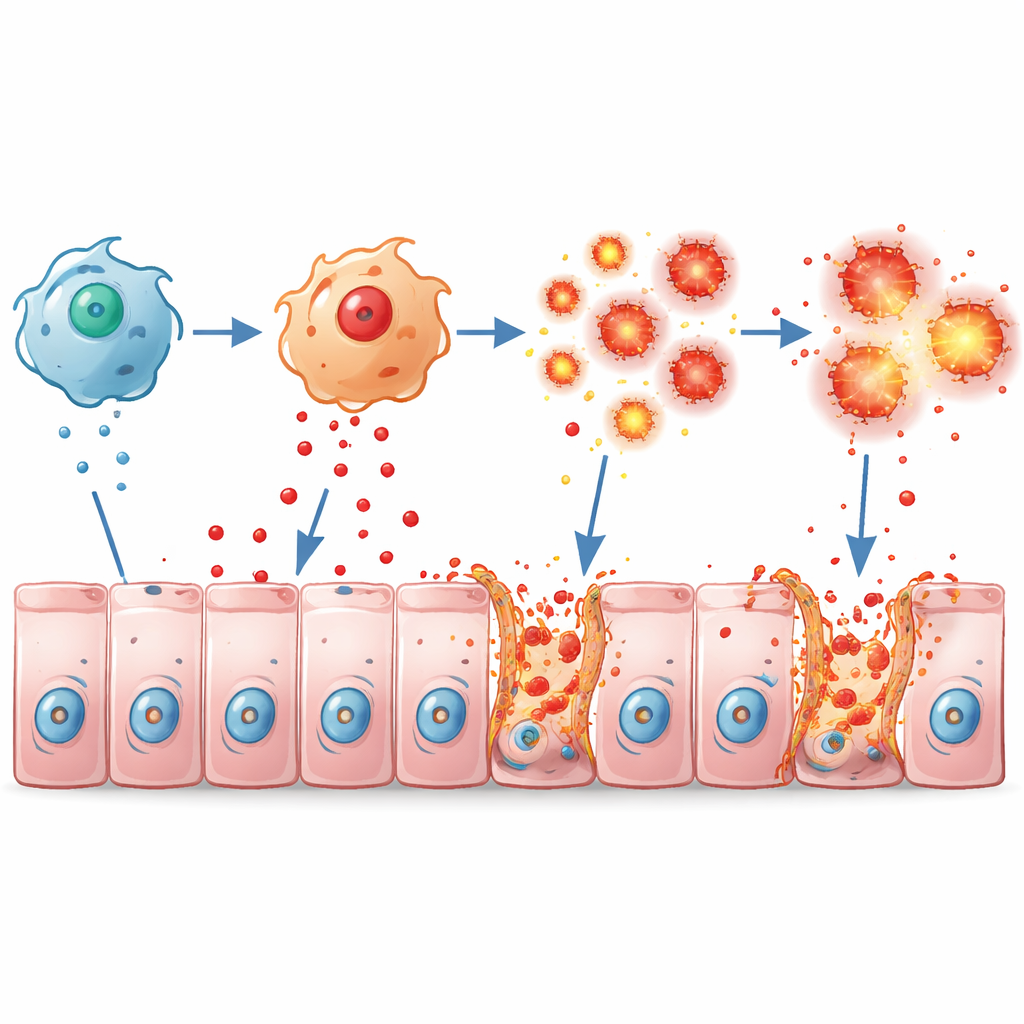
Перегретые иммунные клетки и хрупкий барьер
Макрофаги обычно помогают защищать кишечник, но при гиперактивации они могут вызывать повреждения. В лабораторных условиях макрофаги от мышей без Pum2 реагировали на бактериальные компоненты, выбрасывая значительно больше провоспалительных медиаторов, таких как TNFα, IL-1β и IL-6, и переходили в выраженно агрессивное состояние. У живых мышей с колитом эти гиперактивные макрофаги скапливались в ободочной кишке и заливали ткань TNFα. Слизистая реагировала широкомасштабной гибелью клеток и разрушением плотных контактов — белковых «молний» вроде ZO-1, Occludin и Claudin1, которые обычно герметично соединяют соседние клетки. В результате образовывался протекающий, хрупкий барьер, который позволял воспалению подпитывать само себя.
Как стресс клеток приводит к их гибели и открывает шлюзы
Исследование также сосредоточилось на самих эпителиальных клетках кишечника. Pum2 обычно помогает этим клеткам держать под контролем реактивные формы кислорода — высокоактивные производные кислорода. При повышении Pum2 в человеческих клеточных линиях кишечника клетки вырабатывали меньше оксидативного стресса в ответ на перекись водорода или TNFα и реже умирали. При недостатке Pum2 оксидативный стресс возрастал, и включалась специфическая форма взрывной клеточной смерти — некроптоз, отмечаемый активацией молекул, таких как RIPK1 и MLKL, пробивающих отверстия в мембранах клеток. В системе ко-культуры, имитировавшей воспалённый кишечник, макрофаги заливали эпителиальные клетки TNFα, что вызывало некроптоз, утечку клеточного содержимого и потерю белков барьера — эффекты, которые в значительной мере можно было обратить либо восстановлением Pum2 в макрофагах, либо блокировкой TNFα.
Что это означает для будущего лечения
В сумме результаты показывают Pum2 как ключевого миротворца на границе между иммунными клетками кишечника и его стенкой. Когда уровни Pum2 падают во время обострения, макрофаги становятся чрезмерно активными и продуцируют избыток TNFα, а эпителиальные клетки делаются более уязвимыми к оксидативному стрессу и некроптозной гибели. Этот токсичный диалог разъедает барьер и усугубляет колит. Поскольку уровни Pum2 коррелируют с активностью болезни и восстановлением, а усиление Pum2 ослабляет вредные сигналы в иммунных и эпителиальных клетках, нацеливание на этот путь — или сохранение активности Pum2 — может предложить новую стратегию укрепления кишечного барьера и снижения числа обострений при язвенном колите.
Цитирование: Wang, X., Han, X., Qiu, W. et al. Loss of Pum2 exacerbates colitis by disrupting macrophage–epithelial crosstalk and promoting epithelial necroptosis. Cell Death Discov. 12, 137 (2026). https://doi.org/10.1038/s41420-026-03041-x
Ключевые слова: язвенный колит, кишечный барьер, макрофаги, клеточная гибель, РНК-связывающие белки