Clear Sky Science · pl
Utrata Pum2 pogłębia zapalenie jelita grubego przez zaburzenie komunikacji makrofag–nabłonek i promowanie nekroptozy nabłonka
Dlaczego to ma znaczenie dla osób z problemami jelitowymi
Colitis ulcerosa to przewlekła choroba, w której wyściółka jelita grubego ulega bolesnemu zapaleniu i jest podatna na nawracające zaostrzenia. Wielu pacjentów przechodzi cykle między okresami spokoju a nagłymi epizodami krwawienia, skurczów i nagłymi parciami. To badanie ujawnia wcześniej pomijany „hamulec” wewnątrz komórek odpornościowych i nabłonka jelitowego — białko o nazwie Pum2 — które pomaga utrzymać stan zapalny w ryzach. Zrozumienie, jak działa ten wewnętrzny hamulec, może wskazać nowe sposoby łagodzenia objawów, ochrony ściany jelita i potencjalnie poprawy leczenia colitis ulcerosa.
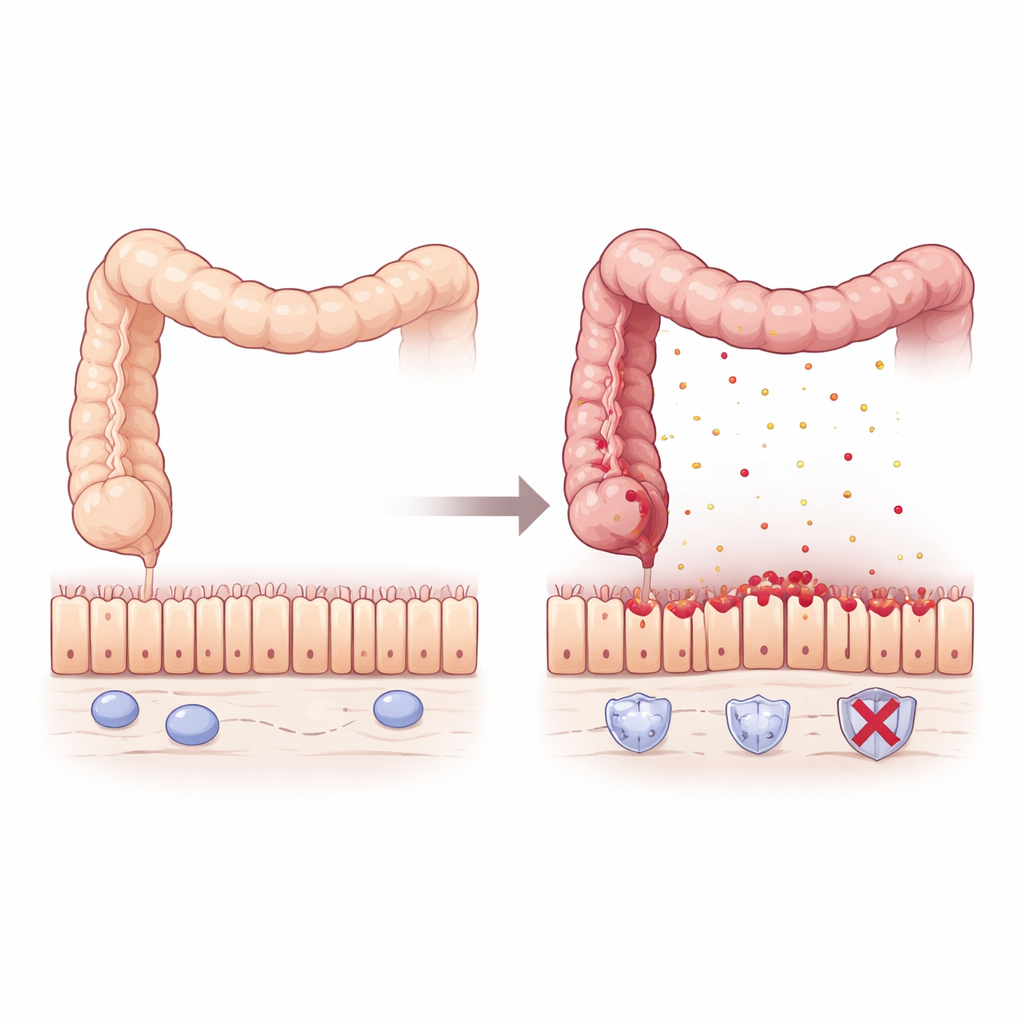
Cichy strażnik w zapalnym jelicie
Naukowcy zaczęli od analizy dużych zbiorów danych tkankowych od pacjentów z zapalnymi chorobami jelit i rakiem jelita grubego. Stwierdzili, że poziomy Pum2, białka wiążącego RNA i regulującego syntezę innych białek, były konsekwentnie niższe w obszarach aktywnego zapalenia okrężnicy i odbytnicy. Gdy wyściółka jelita goiła się po leczeniu, poziomy Pum2 ponownie wzrastały, szczególnie u pacjentów, u których choroba przeszła w trwałą remisję. Co ciekawe, w nowotworach jelita powstających po długotrwałym zapaleniu Pum2 ponownie był aktywowany do poziomów zbliżonych do zdrowej tkanki, co sugeruje, że białko to może pełnić różne role podczas zapalenia i nowotworzenia.
Kiedy hamulec znika, colitis się nasila
Aby sprawdzić skutki braku Pum2, zespół użył myszy zmodyfikowanych tak, by nie miały genu Pum2, i wystawił je na substancję chemiczną wywołującą colitis przez uszkodzenie wyściółki jelita. W porównaniu z myszami normalnymi, zwierzęta bez Pum2 traciły więcej masy ciała, miały krótsze, silniej zapalone jelito grube, powiększone śledzione i wyższy wskaźnik zgonów. Badanie mikroskopowe wykazało ciężkie zaburzenia wyściółki jelita, z zniekształconymi gruczołami i intensywnym naciekiem komórek odpornościowych. Nawet przed pojawieniem się oczywistych objawów choroby, profilowanie genetyczne ujawniło, że okrężnice pozbawione Pum2 były „zaprzyjaźnione” z kłopotami: cicho produkowały więcej chemokin — cząsteczek sygnalizacyjnych przyciągających komórki zapalne — zwłaszcza tych przyciągających makrofagi, kluczowy rodzaj komórek odpornościowych.
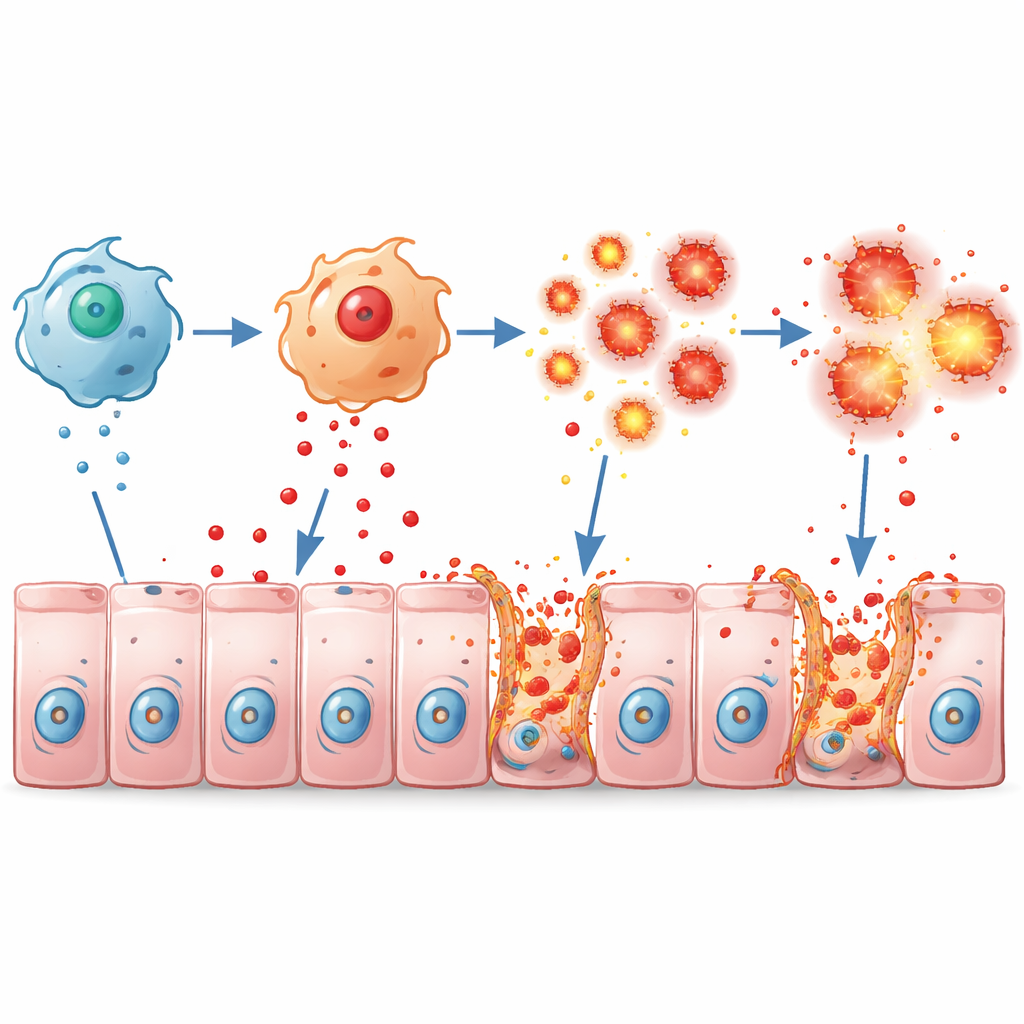
Przegrzane komórki odpornościowe i krucha bariera
Makrofagi normalnie pomagają bronić jelita, ale mogą powodować uszkodzenia, gdy są nadmiernie aktywowane. W hodowlach komórkowych makrofagi z myszy pozbawionych Pum2 reagowały na składniki bakteryjne przez wydzielanie znacznie większych ilości mediatorów zapalnych, takich jak TNFα, IL-1β i IL-6, przyjmując silnie agresywny stan. U żywych myszy z colitis te nadaktywne makrofagi gromadziły się w okrężnicy i zalewały tkankę TNFα. Wyściółka jelita odpowiedziała powszechną śmiercią komórek i rozluźnieniem połączeń zamykających — białkowych „zameczków” takich jak ZO-1, Occludin i Claudin1 — które zwykle uszczelniają sąsiednie komórki. W efekcie powstała przeciekająca, krucha bariera, która pozwalała, by zapalenie napędzało samo siebie.
Jak zestresowane komórki umierają i wpuszczają wodę do ognia
Badanie przyjrzało się także komórkom wyściółki jelitowej. Pum2 normalnie pomaga tym komórkom kontrolować reaktywne formy tlenu — wysoce reaktywne rodzaje tlenu. Gdy Pum2 był zwiększany w ludzkich liniach komórkowych jelita, komórki wytwarzały mniej stresu oksydacyjnego w odpowiedzi na nadtlenek wodoru lub TNFα i rzadziej umierały. Bez wystarczającego Pum2 stres oksydacyjny wzrastał, a specyficzna forma wybuchowej śmierci komórkowej zwana nekroptozą włączała się, oznaczona aktywacją cząsteczek takich jak RIPK1 i MLKL, które przebijają błony komórkowe. W systemie ko-kultury imitującym zapalne jelito, makrofagi oblewały komórki nabłonkowe TNFα, co wywoływało nekroptozę, wyciek zawartości komórek i utratę białek bariery — efekty, które w dużej mierze można było odwrócić albo przez przywrócenie Pum2 w makrofagach, albo przez blokowanie TNFα.
Co to oznacza dla przyszłej opieki
W sumie wyniki malują obraz Pum2 jako kluczowego stróża na pograniczu między komórkami odpornościowymi jelita a ścianą jelita. Gdy poziomy Pum2 spadają podczas zaostrzenia, makrofagi stają się nadgorliwe i produkują nadmiar TNFα, podczas gdy komórki nabłonkowe stają się bardziej podatne na stres oksydacyjny i nekroptoza. Ta toksyczna rozmowa niszczy barierę i pogarsza colitis. Ponieważ poziomy Pum2 korelują z aktywnością choroby i wyzdrowieniem, a zwiększenie Pum2 tłumi szkodliwe sygnały zarówno w komórkach odpornościowych, jak i nabłonkowych, ukierunkowanie tej ścieżki — lub zachowanie aktywności Pum2 — mogłoby stanowić nową strategię wzmocnienia bariery jelitowej i zmniejszenia nawrotów w colitis ulcerosa.
Cytowanie: Wang, X., Han, X., Qiu, W. et al. Loss of Pum2 exacerbates colitis by disrupting macrophage–epithelial crosstalk and promoting epithelial necroptosis. Cell Death Discov. 12, 137 (2026). https://doi.org/10.1038/s41420-026-03041-x
Słowa kluczowe: colitis ulcerosa, bariera jelitowa, makrofagi, śmierć komórkowa, białka wiążące RNA