Clear Sky Science · it
La perdita di Pum2 aggrava la colite interrompendo il dialogo macrofago–epitelio e favorendo la necroptosi epiteliale
Perché questo è importante per chi ha problemi intestinali
La colite ulcerosa è una malattia cronica in cui il rivestimento del grosso intestino si infiamma dolorosamente e tende a reazioni acute. Molti pazienti alternano periodi di calma a episodi improvvisi di sanguinamento, crampi e urgente bisogno di defecare. Questo studio individua un «freno» interno finora trascurato nelle cellule immunitarie e nel rivestimento intestinale — una proteina chiamata Pum2 — che contribuisce a contenere l’infiammazione. Comprendere come funziona questo freno interno potrebbe indicare nuove vie per calmare l’intestino, proteggere la parete intestinale e forse migliorare i trattamenti per la colite ulcerosa.
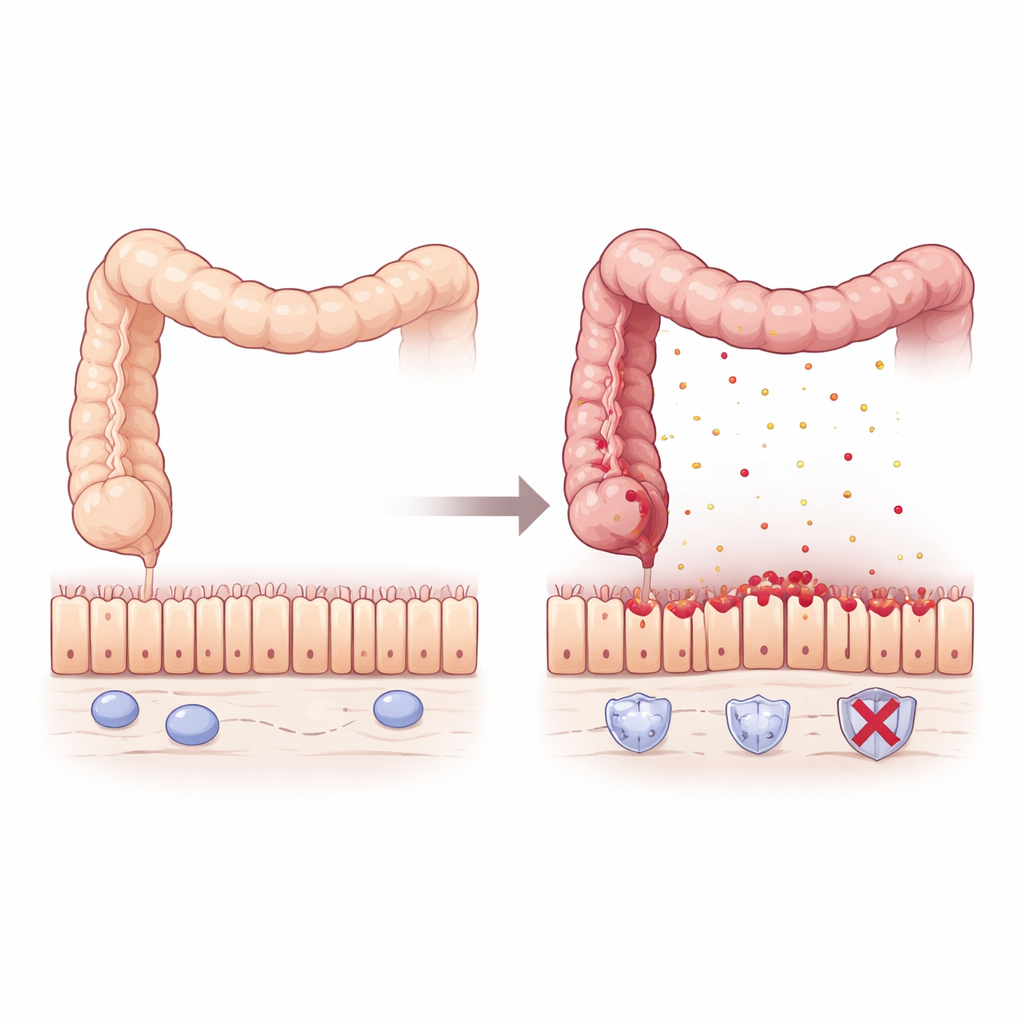
Un guardiano silenzioso nell’intestino infiammato
I ricercatori hanno iniziato analizzando grandi collezioni di dati tissutali di pazienti con malattia infiammatoria intestinale e cancro colorettale. Hanno scoperto che i livelli di Pum2, una proteina che si lega all’RNA e regola finemente la sintesi di altre proteine, risultavano costantemente più bassi nelle aree attivamente infiammate del colon e del retto. Quando il rivestimento intestinale guarisce dopo il trattamento, i livelli di Pum2 aumentano di nuovo, soprattutto nei pazienti la cui malattia entra in remissione sostenuta. In modo intrigante, nei tumori intestinali che insorgono dopo coliti di lunga durata, Pum2 risultava riattivata a livelli simili ai tessuti sani, suggerendo che questa proteina possa avere ruoli diversi durante l’infiammazione e il cancro.
Quando il freno manca, la colite peggiora
Per capire cosa succede in assenza di Pum2, il team ha usato topi ingegnerizzati privi del gene Pum2 ed esposti a una sostanza chimica che induce la colite danneggiando il rivestimento intestinale. Rispetto ai topi normali, gli animali privi di Pum2 hanno perso più peso, avevano colon più corti e infiammati, milza ingrossata e tassi di mortalità maggiori. L’esame microscopico ha mostrato una grave alterazione del rivestimento intestinale, con ghiandole deformate e massiccia infiltrazione di cellule immunitarie. Anche prima che la malattia fosse evidente, il profilo genetico rivelava che i colon senza Pum2 erano «in allerta»: producevano silenziosamente più chemochine — molecole segnale che attirano cellule infiammatorie — in particolare quelle che richiamano i macrofagi, un tipo chiave di cellule immunitarie.
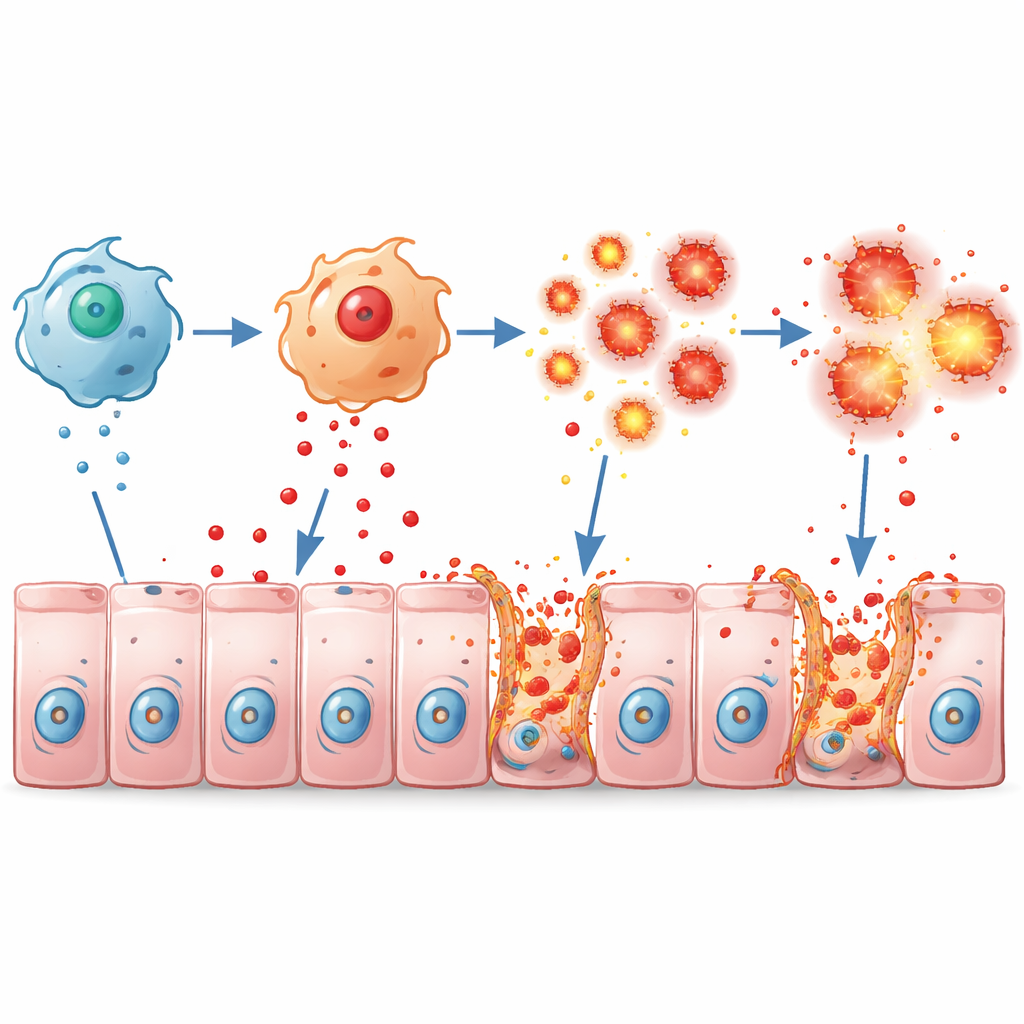
Cellule immunitarie surriscaldate e una barriera fragile
I macrofagi normalmente aiutano a difendere l’intestino ma possono favorire il danno se iperattivati. In colture cellulari, i macrofagi provenienti da topi privi di Pum2 rispondevano ai componenti batterici producendo molto più messaggeri infiammatori come TNFα, IL-1β e IL-6, assumendo uno stato fortemente aggressivo. Nei topi viventi con colite, questi macrofagi iperattivi si accumulavano nel colon e inundavano il tessuto di TNFα. Il rivestimento intestinale rispondeva con ampia morte cellulare e la rottura delle giunzioni serrate — «cerniere» proteiche come ZO-1, Occludin e Claudin1 — che normalmente sigillano le cellule vicine. Il risultato era una barriera permeabile e fragile che permetteva all’infiammazione di autoalimentarsi.
Come le cellule stressate muoiono e spalancano le porte
Lo studio si è poi concentrato sulle stesse cellule del rivestimento intestinale. Pum2 normalmente aiuta queste cellule a mantenere sotto controllo le specie reattive dell’ossigeno — forme altamente reattive dell’ossigeno. Quando Pum2 veniva aumentata in linee cellulari intestinali umane, le cellule producevano meno stress ossidativo in risposta al perossido di idrogeno o al TNFα e avevano una minore propensione alla morte. In assenza di adeguati livelli di Pum2, lo stress ossidativo aumentava e si attivava una forma specifica di morte cellulare esplosiva chiamata necroptosi, segnata dall’attivazione di molecole come RIPK1 e MLKL che perforano le membrane cellulari. In un sistema a co-coltura che imitava l’intestino infiammato, i macrofagi sommergevano le cellule epiteliali di TNFα, innescando necroptosi, fuga di contenuti cellulari e perdita di proteine di barriera — effetti che potevano essere in larga parte annullati sia ripristinando Pum2 nei macrofagi sia bloccando il TNFα.
Cosa significa per le cure future
Nel complesso, i risultati ritraggono Pum2 come un importante pacificatore al confine tra le cellule immunitarie intestinali e la parete intestinale. Quando i livelli di Pum2 diminuiscono durante una riacutizzazione, i macrofagi diventano iperattivi e producono TNFα in eccesso, mentre le cellule epiteliali diventano più vulnerabili allo stress ossidativo e alla morte necroptotica. Questa conversazione tossica erode la barriera e peggiora la colite. Poiché i livelli di Pum2 seguono l’attività della malattia e la guarigione, e poiché potenziare Pum2 attenua i segnali dannosi sia nelle cellule immunitarie sia in quelle del rivestimento, mirare a questa via — o preservare l’attività di Pum2 — potrebbe offrire una nuova strategia per rafforzare la barriera intestinale e ridurre le riacutizzazioni nella colite ulcerosa.
Citazione: Wang, X., Han, X., Qiu, W. et al. Loss of Pum2 exacerbates colitis by disrupting macrophage–epithelial crosstalk and promoting epithelial necroptosis. Cell Death Discov. 12, 137 (2026). https://doi.org/10.1038/s41420-026-03041-x
Parole chiave: colite ulcerosa, barriera intestinale, macrofagi, morte cellulare, proteine leganti RNA