Clear Sky Science · fr
La perte de Pum2 aggrave la colite en perturbant le dialogue macrophage–épithélium et en favorisant la nécroptose épithéliale
Pourquoi c’est important pour les personnes souffrant de troubles intestinaux
La colite ulcéreuse est une maladie chronique où la muqueuse du gros intestin s’enflamme douloureusement et est sujette à des poussées. De nombreux patients alternent entre des périodes calmes et des épisodes soudains de saignements, de crampes et d’envies impérieuses d’aller à la selle. Cette étude met au jour un « frein » jusqu’ici négligé au sein des cellules immunitaires et de la muqueuse intestinale — une protéine appelée Pum2 — qui aide à contenir l’inflammation. Comprendre le fonctionnement de ce frein interne pourrait indiquer de nouvelles voies pour calmer l’intestin, protéger la paroi intestinale et peut‑être améliorer les traitements de la colite ulcéreuse.
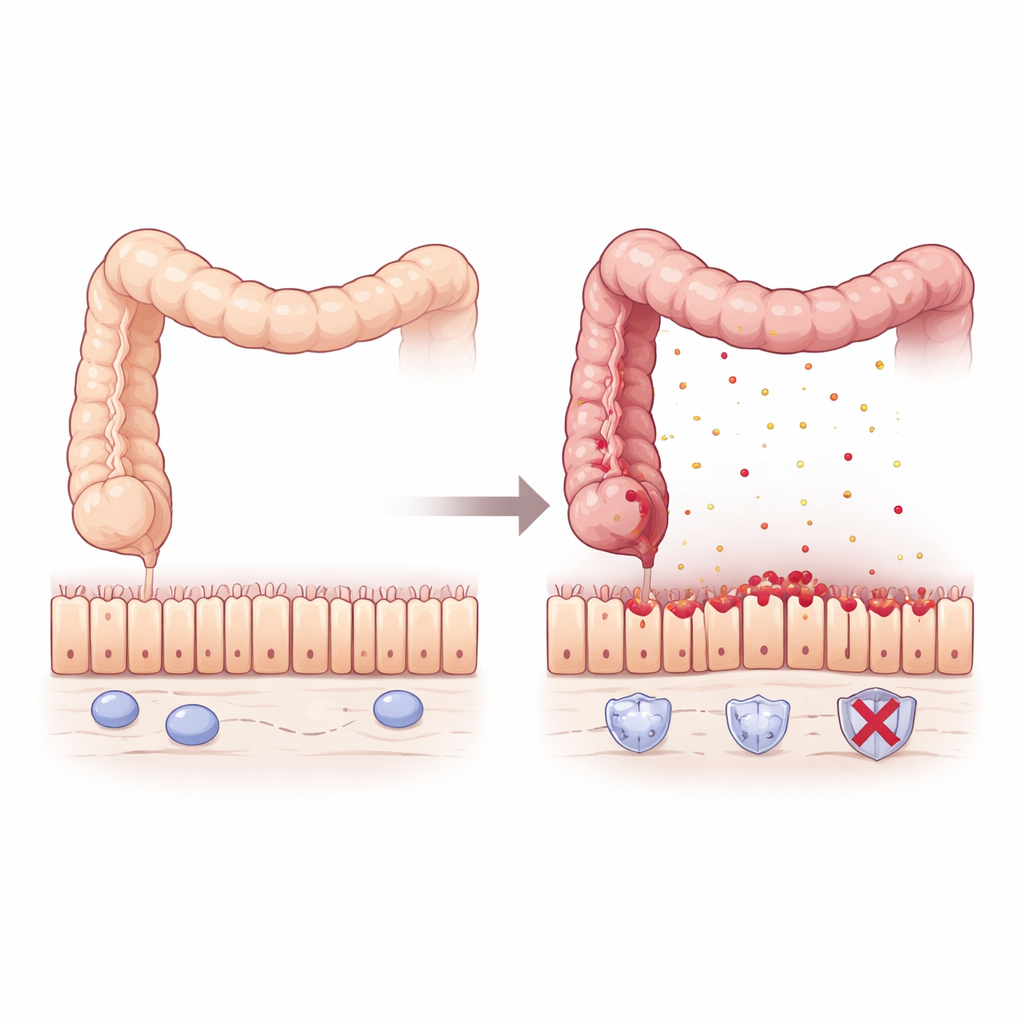
Un gardien discret dans l’intestin enflammé
Les chercheurs ont commencé par exploiter de larges jeux de données de tissus de patients atteints de maladies inflammatoires de l’intestin et de cancers colorectaux. Ils ont constaté que les niveaux de Pum2, une protéine qui se lie à l’ARN et ajuste la production d’autres protéines, étaient systématiquement plus faibles dans les zones activement enflammées du côlon et du rectum. Lorsque la muqueuse intestinale guérissait après traitement, les niveaux de Pum2 remontaient, surtout chez les patients dont la maladie passait en rémission durable. Fait intrigant, dans les tumeurs intestinales qui apparaissent après une colite prolongée, Pum2 était réactivée à des niveaux proches de ceux des tissus sains, suggérant que cette protéine peut jouer des rôles différents pendant l’inflammation et le cancer.
Quand le frein manque, la colite s’aggrave
Pour évaluer l’impact de la perte de Pum2, l’équipe a utilisé des souris génétiquement modifiées dépourvues du gène Pum2 et les a exposées à un produit chimique provoquant une colite en endommageant la muqueuse intestinale. Par rapport aux souris normales, les animaux sans Pum2 perdaient plus de poids, avaient des côlons plus courts et plus enflammés, des rate élargies et des taux de mortalité plus élevés. L’examen au microscope a montré une perturbation sévère de la muqueuse, avec des glandes déformées et une forte infiltration de cellules immunitaires. Même avant l’apparition de signes cliniques évidents, le profilage génétique révélait que les côlons dépourvus de Pum2 étaient « prêts » à la dérive : ils produisaient silencieusement plus de chimiokines — des molécules‑signal qui attirent les cellules inflammatoires — en particulier celles qui recrutent les macrophages, un type clé de cellules immunitaires.
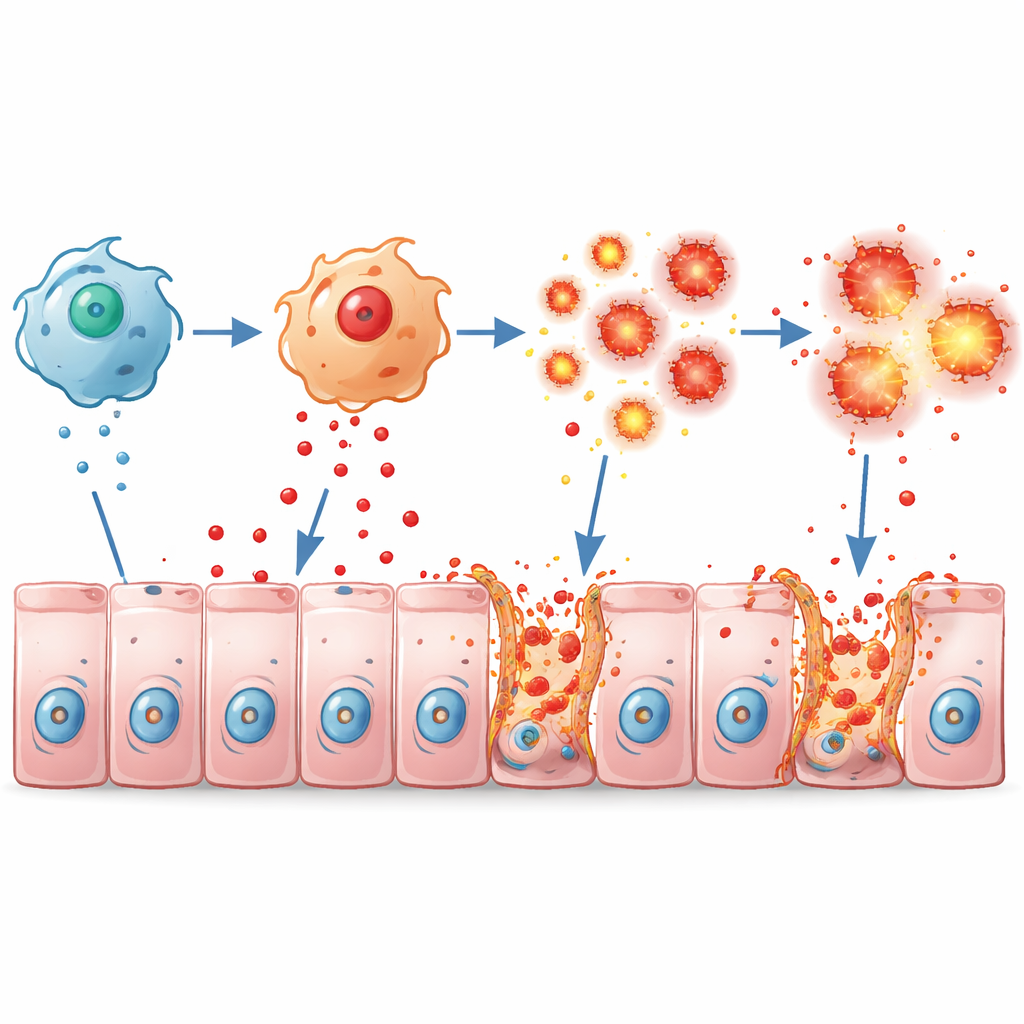
Des cellules immunitaires en surrégime et une barrière fragile
Les macrophages aident normalement à défendre l’intestin mais peuvent provoquer des dégâts lorsqu’ils sont suractivés. En culture, les macrophages de souris dépourvues de Pum2 réagissaient aux composants bactériens en sécrétant beaucoup plus de médiateurs inflammatoires tels que TNFα, IL‑1β et IL‑6, et adoptaient un état fortement agressif. Chez les souris vivantes atteintes de colite, ces macrophages hyperactifs s’accumulaient dans le côlon et inondaient le tissu de TNFα. La muqueuse réagissait par une mort cellulaire généralisée et une rupture des jonctions serrées — des « fermetures éclair » protéiques comme ZO‑1, Occludin et Claudin1 — qui scellent habituellement les cellules voisines. Il en résultait une barrière perméable et fragile permettant à l’inflammation de s’auto‑entretenir.
Comment les cellules stressées meurent et ouvrent les vannes
L’étude s’est également penchée sur les cellules de la muqueuse elle‑même. Pum2 aide normalement ces cellules à maîtriser les espèces réactives de l’oxygène — des formes d’oxygène très réactives. Lorsqu’on augmentait Pum2 dans des lignées cellulaires intestinales humaines, les cellules produisaient moins de stress oxydatif en réponse au peroxyde d’hydrogène ou au TNFα, et elles étaient moins susceptibles de mourir. En l’absence d’un Pum2 suffisant, le stress oxydatif augmentait, et une forme spécifique de mort cellulaire explosive appelée nécroptose s’activait, marquée par l’activation de molécules comme RIPK1 et MLKL qui perforent les membranes cellulaires. Dans un système de co‑culture mimant l’intestin enflammé, les macrophages baignaient les cellules épithéliales de TNFα, ce qui déclenchait la nécroptose, la fuite du contenu cellulaire et la perte de protéines de barrière — effets qui pouvaient être largement inversés soit en restaurant Pum2 dans les macrophages, soit en bloquant le TNFα.
Ce que cela signifie pour les soins futurs
Pris ensemble, ces résultats dressent le portrait de Pum2 comme d’un pacificateur crucial à la frontière entre les cellules immunitaires intestinales et la paroi intestinale. Lorsque les niveaux de Pum2 chutent lors d’une poussée, les macrophages deviennent hyper‑zélés et produisent un excès de TNFα, tandis que les cellules épithéliales deviennent plus vulnérables au stress oxydatif et à la mort nécroptotique. Cette conversation toxique érode la barrière et aggrave la colite. Étant donné que les niveaux de Pum2 reflètent l’activité et la récupération de la maladie, et que l’augmentation de Pum2 atténue les signaux délétères à la fois dans les cellules immunitaires et la muqueuse, cibler cette voie — ou préserver l’activité de Pum2 — pourrait offrir une nouvelle stratégie pour renforcer la barrière intestinale et réduire les poussées de colite ulcéreuse.
Citation: Wang, X., Han, X., Qiu, W. et al. Loss of Pum2 exacerbates colitis by disrupting macrophage–epithelial crosstalk and promoting epithelial necroptosis. Cell Death Discov. 12, 137 (2026). https://doi.org/10.1038/s41420-026-03041-x
Mots-clés: colite ulcéreuse, barrière intestinale, macrophages, mort cellulaire, protéines liant l'ARN