Clear Sky Science · de
Verlust von Pum2 verschlimmert Colitis durch Störung des Makrophagen–Epithel-Dialogs und Förderung epithelialer Nekroptose
Warum das für Menschen mit Darmproblemen wichtig ist
Die ulzerative Colitis ist eine chronische Erkrankung, bei der die Schleimhaut des Dickdarms schmerzhaft entzündet ist und zu Schüben neigt. Viele Patientinnen und Patienten wechseln zwischen ruhigen Phasen und plötzlichen Episoden mit Blutungen, Krämpfen und starkem Stuhldrang. Diese Studie enthüllt eine bislang wenig beachtete „Handbremse“ in Immun- und Epithelzellen des Darms – ein Protein namens Pum2 –, das hilft, Entzündungen im Zaum zu halten. Ein besseres Verständnis dieses inneren Reglers könnte neue Wege eröffnen, den Darm zu beruhigen, die Darmwand zu schützen und möglicherweise die Behandlung der ulzerativen Colitis zu verbessern.
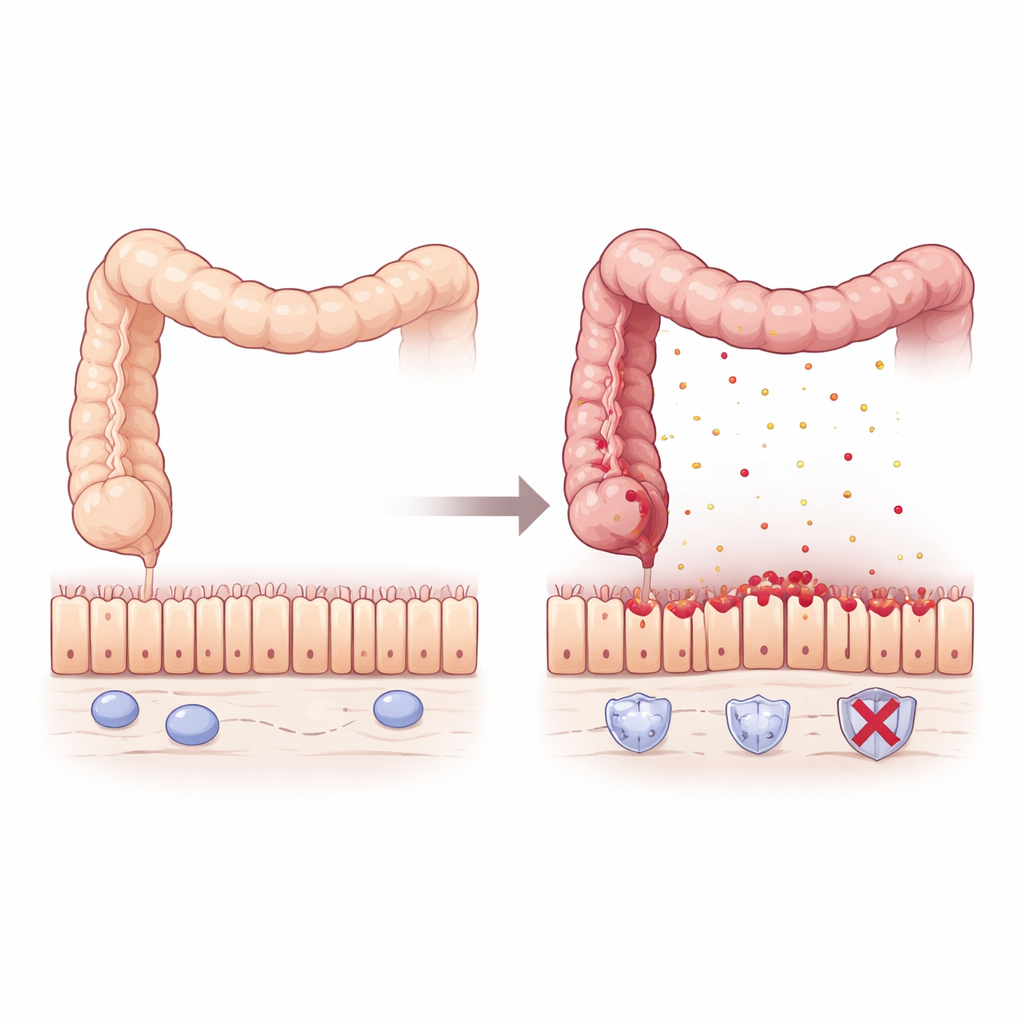
Ein leiser Wächter im entzündeten Darm
Die Forschenden begannen damit, umfangreiche Gewebedaten von Patientinnen und Patienten mit entzündlichen Darmerkrankungen und Dickdarmkrebs auszuwerten. Sie stellten fest, dass die Mengen an Pum2, einem RNA-bindenden Protein, das die Produktion anderer Proteine feinregelt, in aktiv entzündeten Bereichen von Kolon und Rektum durchgehend niedriger waren. Wenn sich die Darmschleimhaut nach einer Behandlung erholte, stiegen die Pum2-Spiegel wieder an, besonders bei Patientinnen und Patienten, deren Erkrankung in anhaltende Remission überging. Auffällig war außerdem, dass Pum2 in Darmtumoren, die nach langjähriger Colitis entstehen, wieder auf ähnliche Werte wie im gesunden Gewebe hochreguliert war, was darauf hindeutet, dass dieses Protein während Entzündung und Krebs unterschiedlich wirken könnte.
Fehlt die Bremse, verschlechtert sich die Colitis
Um zu untersuchen, was passiert, wenn Pum2 fehlt, nutzte das Team Mäuse, denen das Pum2-Gen fehlte, und setzte sie einem Chemikalienmodell aus, das durch Schädigung der Darmschleimhaut Colitis auslöst. Im Vergleich zu normalen Mäusen verloren die Tiere ohne Pum2 mehr Gewicht, hatten kürzere, stärker entzündete Kolons, größere Milzen und höhere Sterblichkeitsraten. Die mikroskopische Untersuchung zeigte eine starke Zerstörung der Darmschleimhaut mit deformierten Drüsen und massiver Infiltration durch Immunzellen. Selbst bevor offensichtliche Symptome auftraten, deutete die genetische Profilierung darauf hin, dass Pum2-defiziente Kolons für Probleme „vorbereitet“ waren: sie produzierten stillschweigend mehr Chemokine – Botenstoffe, die entzündliche Zellen anziehen – insbesondere solche, die Makrophagen anlocken, eine zentrale Immunzellpopulation.
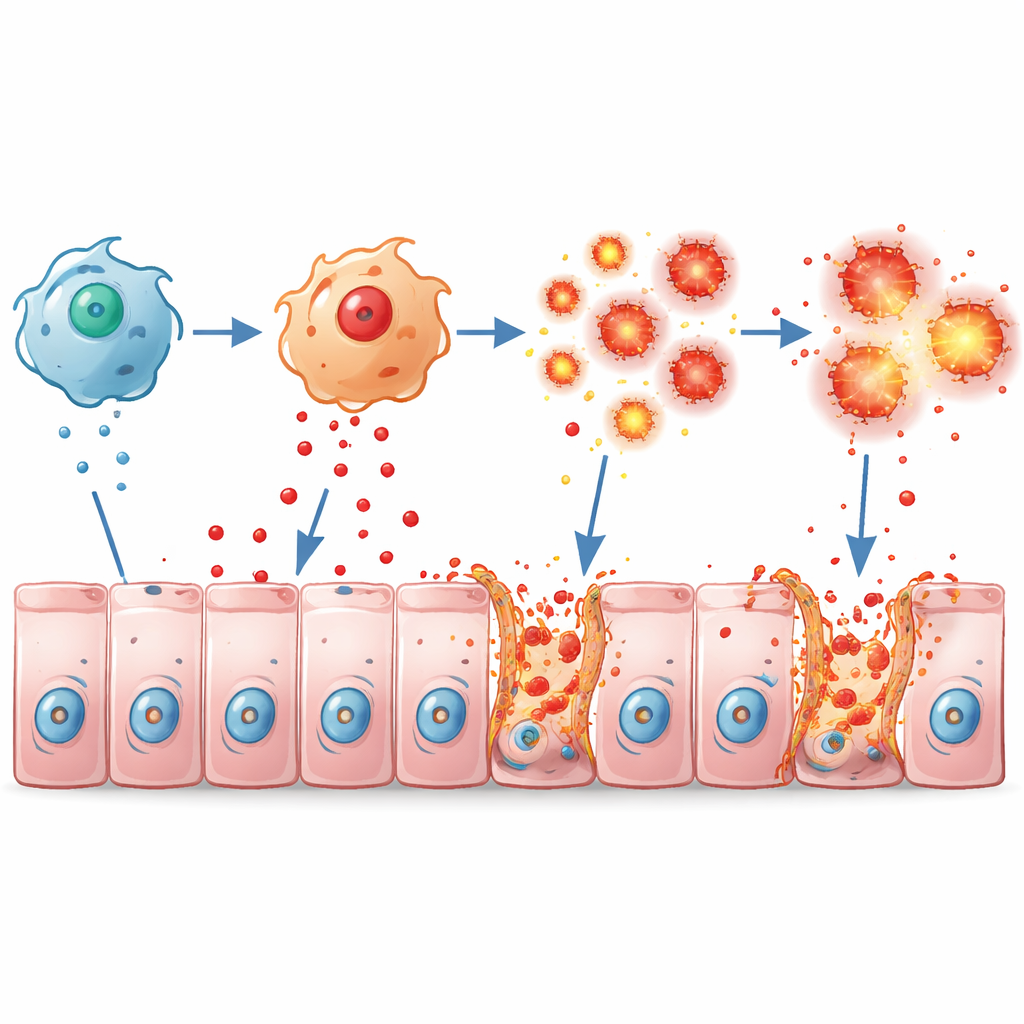
Überhitzte Immunzellen und eine fragile Barriere
Makrophagen helfen normalerweise bei der Abwehr im Darm, können aber bei Überaktivierung Schaden verursachen. In Zellkulturen reagierten Makrophagen aus Pum2-defizienten Mäusen auf bakterielle Komponenten mit einer deutlich stärkeren Freisetzung entzündlicher Botenstoffe wie TNFα, IL-1β und IL-6 und nahmen einen stark aggressiven Zustand ein. In lebenden Mäusen mit Colitis drängten sich diese hyperaktiven Makrophagen im Kolon zusammen und überschwemmten das Gewebe mit TNFα. Die Darmschleimhaut reagierte mit weitverbreitetem Zelltod und dem Zusammenbruch der Tight Junctions – proteinähnlichen „Reißverschlüssen“ wie ZO-1, Occludin und Claudin1 –, die normalerweise benachbarte Zellen abdichten. Das Resultat war eine undichte, fragile Barriere, die die Entzündung weiter anheizte.
Wie gestresste Zellen sterben und die Flut öffnet
Die Studie richtete den Blick auch auf die Epithelzellen der Darmschleimhaut selbst. Pum2 hilft diesen Zellen normalerweise, reaktive Sauerstoffspezies – hochreaktive Formen von Sauerstoff – unter Kontrolle zu halten. Wenn Pum2 in menschlichen Darmzelllinien hochreguliert wurde, erzeugten die Zellen weniger oxidativen Stress als Reaktion auf Wasserstoffperoxid oder TNFα und hatten eine geringere Sterbewahrscheinlichkeit. Fehlt ausreichend Pum2, steigt der oxidative Stress, und eine spezifische, explosionsartige Form des Zelltods namens Nekroptose wird aktiviert, erkennbar an Aktivierung von Molekülen wie RIPK1 und MLKL, die Löcher in Zellmembranen schlagen. In einem Ko-Kultursystem, das den entzündeten Darm nachahmt, badeten Makrophagen Epithelzellen in TNFα, was Nekroptose, Auslaufen von Zellinhalten und Verlust von Barrierproteinen auslöste – Effekte, die weitgehend umkehrbar waren, wenn entweder Pum2 in Makrophagen wiederhergestellt oder TNFα blockiert wurde.
Was das für die künftige Versorgung bedeutet
Insgesamt zeichnen die Befunde Pum2 als entscheidenden Friedensstifter an der Grenze zwischen Darm-Immunzellen und der Darmwand. Fallen die Pum2-Spiegel während eines Schubs, werden Makrophagen übermäßig aktiv und produzieren zu viel TNFα, während Epithelzellen anfälliger für oxidativen Stress und nekroptotischen Zelltod werden. Dieses toxische Gespräch zersetzt die Barriere und verschlechtert die Colitis. Da Pum2-Spiegel mit Krankheitsaktivität und Erholung korrelieren und eine Erhöhung von Pum2 schädliche Signale in Immun- und Epithelzellen dämpft, könnte das Ansteuern dieses Weges – oder der Erhalt der Pum2-Aktivität – eine neue Strategie bieten, die Darmbarriere zu stärken und Schübe bei ulzerativer Colitis zu reduzieren.
Zitation: Wang, X., Han, X., Qiu, W. et al. Loss of Pum2 exacerbates colitis by disrupting macrophage–epithelial crosstalk and promoting epithelial necroptosis. Cell Death Discov. 12, 137 (2026). https://doi.org/10.1038/s41420-026-03041-x
Schlüsselwörter: ulzerative Colitis, intestinaler Schutzschirm, Makrophagen, Zellsterben, RNA-bindende Proteine