Clear Sky Science · pt
Resgate dependente do sexo de déficits de memória e sinápticos em camundongos modelo de DA ao aumentar a palmitoilação de PSD-95
Por que isso importa para a saúde cerebral no dia a dia
A doença de Alzheimer não afeta todas as pessoas da mesma forma: mulheres têm maior probabilidade do que homens de desenvolver perda de memória, e seus sintomas muitas vezes pioram mais rápido. Este estudo explora uma possível razão para isso — e testa uma estratégia farmacológica que protege diretamente as conexões entre neurônios, em vez de visar as clássicas placas cerebrais. O trabalho, realizado em um modelo de camundongo amplamente usado para Alzheimer, sugere que reforçar sinapses frágeis no centro de memória do cérebro pode resgatar seletivamente a memória em fêmeas com maior risco.
Um pequeno andaime no coração da memória
Nossas memórias dependem de trilhões de sinapses — pontos de contato microscópicos onde neurônios se comunicam. Em cada sinapse excitatória, uma proteína andaime chamada PSD-95 ajuda a ancorar receptores que recebem sinais químicos. Para que a PSD-95 permaneça no lugar certo, ela precisa ser revestida por cadeias gordurosas em um processo químico reversível chamado palmitoilação. Trabalhos anteriores mostraram que os níveis de PSD-95 caem precocemente na doença de Alzheimer e que a palmitoilação de muitas proteínas cerebrais é alterada. Os autores perguntaram se as mudanças na palmitoilação de PSD-95 poderiam diferir entre machos e fêmeas, e se restaurar essa modificação poderia proteger sinapses e memória.
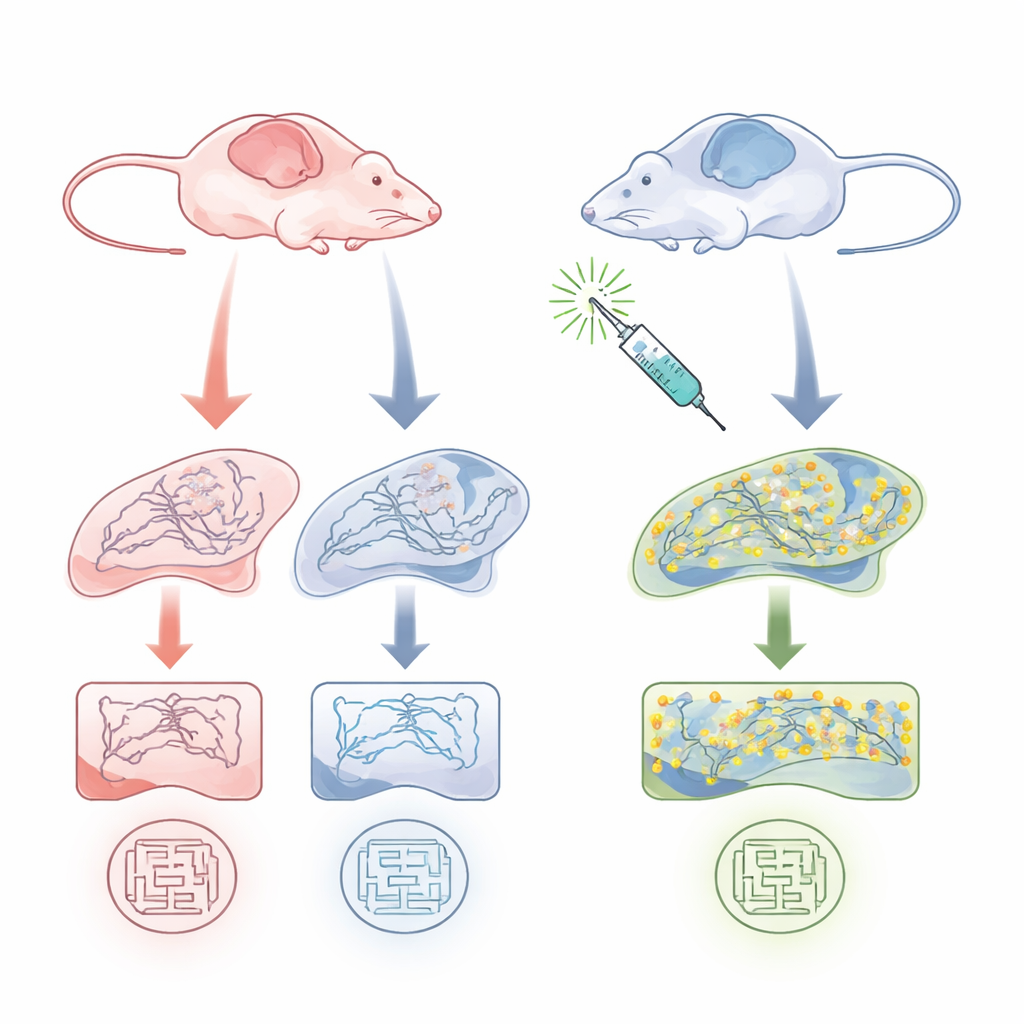
Cérebros femininos mostram uma fraqueza oculta
A equipe estudou camundongos APP/PS1 de 9–10 meses, um modelo padrão de Alzheimer que desenvolve placas amiloides e problemas de memória, e os comparou com irmãos saudáveis. Eles se concentraram no hipocampo, uma região-chave da memória. Usando ensaios bioquímicos, encontraram que a palmitoilação total de muitas proteínas, e especialmente a palmitoilação da PSD-95, estava marcadamente reduzida em fêmeas do modelo de Alzheimer, mas não em machos. Importante, a quantidade total de proteína PSD-95 era similar entre os grupos nessa idade — o que diferia era quanto dela estava na forma palmitoilada, que estabiliza sinapses. Comportamentalmente, apenas as fêmeas do modelo mostraram déficits claros de memória espacial em um teste de labirinto aquático, enquanto os machos performaram aproximadamente tão bem quanto os controles saudáveis. Isso apontou para uma vulnerabilidade específica por sexo que liga a palmitoilação de PSD-95, a saúde sináptica e a memória.
Um fármaco que fixa a PSD-95 no lugar
Para testar se aumentar a palmitoilação de PSD-95 poderia restaurar a função, os pesquisadores usaram Palmostatin B, um composto que bloqueia enzimas que removem cadeias gordurosas de proteínas e que havia mostrado previamente ampliar aglomerados de PSD-95 em neurônios. Eles injetaram uma baixa dose de Palmostatin B em camundongos modelo de Alzheimer machos e fêmeas antes e durante o treinamento no labirinto aquático. Nas fêmeas do modelo, o tratamento restaurou a performance no teste de sonda de memória para níveis próximos ao normal, sem alterar a velocidade de nado dos animais nem a aprendizagem para encontrar uma plataforma visível. A análise bioquímica mostrou que o Palmostatin B aumentou substancialmente a fração de PSD-95 em sua forma palmitoilada no hipocampo feminino, enquanto deixou a palmitoilação total e os níveis de PSD-95 amplamente inalterados. Em machos, onde a palmitoilação de PSD-95 e o comportamento já eram normais, o fármaco teve pouco efeito.
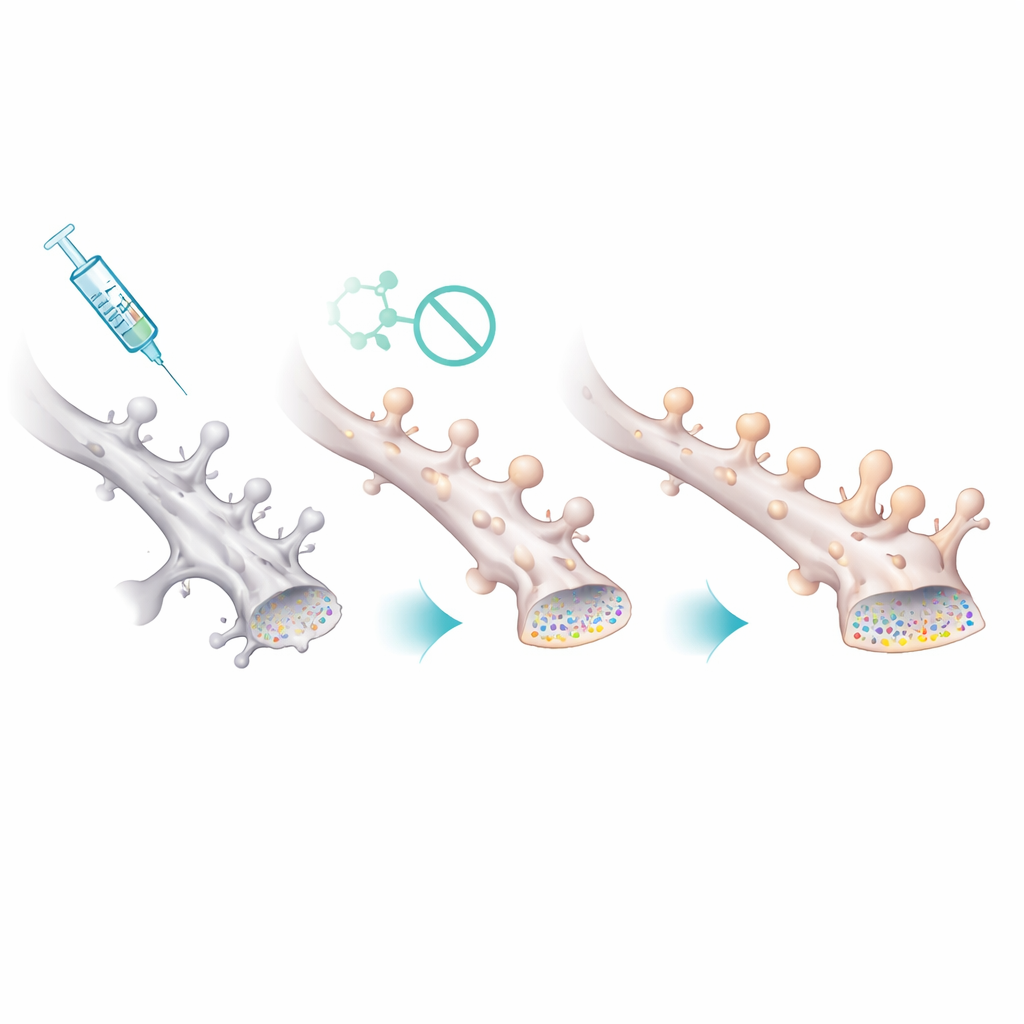
Protegendo as sinapses menores e mais frágeis
Como essa modificação química se traduziu em circuitos mais saudáveis? Registros eletrofisiológicos de neurônios do hipocampo revelaram que as fêmeas do modelo de Alzheimer tinham atividade sináptica espontânea mais fraca, com eventos ocorrendo com menor frequência, porém de tamanho ligeiramente maior — consistente com a perda de muitas sinapses pequenas e a sobrevivência de menos sinapses maiores. Após o tratamento com Palmostatin B, a frequência e o tamanho desses eventos retornaram em direção ao normal. A imagem microscópica de espinhas dendríticas — as pequenas protrusões que abrigam sinapses excitatórias — confirmou esse quadro. As fêmeas do modelo tinham menos espinhas no geral, e as remanescentes eram anormalmente grandes. O fármaco restaurou a densidade de espinhas e deslocou a distribuição de volta para muitas espinhas pequenas e finas, sugerindo que aumentar a palmitoilação de PSD-95 estabiliza especificamente as conexões finas e vulneráveis que são mais importantes para a aprendizagem flexível.
Não por remover placas, mas por reforçar conexões
Uma descoberta crucial é o que o Palmostatin B não fez. O tratamento não reduziu o número ou o tamanho das placas amiloides, nem alterou a ativação de células de suporte próximas conhecidas como astrócitos. Em vez disso, o fármaco alterou o balanço de ácidos graxos livres e proteínas palmitoiladas de maneira dependente do sexo e melhorou a estrutura e a função sináptica apenas onde a palmitoilação de PSD-95 estava inicialmente baixa. Isso indica que o resgate da memória veio do reforço das sinapses, em vez de atacar a patologia clássica do Alzheimer.
O que isso significa para futuras terapias contra Alzheimer
Para leitores não especialistas, a mensagem-chave é que o Alzheimer pode ser visto não apenas como uma doença de placas, mas como uma doença de conexões em colapso — especialmente em mulheres. Este estudo mostra que “colar” quimicamente um andaime sináptico crítico no lugar, aumentando seu revestimento gorduroso, pode restaurar memória e saúde sináptica em fêmeas de um modelo de Alzheimer, mesmo após o desenvolvimento de patologia substancial. Embora o Palmostatin B em si não esteja pronto para uso humano e afete mais de um alvo, o trabalho destaca a palmitoilação de PSD-95 e seus reguladores como pistas promissoras para terapias que fortaleçam sinapses e que, um dia, possam ajudar a proteger aqueles em maior risco.
Citação: Du, Y., Prinkey, K., Pham, A.Q. et al. Sex-dependent rescue of memory and synaptic deficits in AD model mice by increasing PSD-95 palmitoylation. Commun Biol 9, 451 (2026). https://doi.org/10.1038/s42003-026-09702-y
Palavras-chave: Doença de Alzheimer, perda de sinapses, PSD-95, diferenças entre sexos, palmitoilação