Clear Sky Science · de
Geschlechtsabhängige Rettung von Gedächtnis- und synaptischen Defiziten in einem AD-Mausmodell durch Erhöhung der PSD-95-Palmitoylierung
Warum das für die alltägliche Gehirngesundheit wichtig ist
Die Alzheimer-Krankheit trifft nicht alle gleichermaßen: Frauen entwickeln eher als Männer Gedächtnisstörungen, und ihre Symptome verschlechtern sich häufig schneller. Diese Studie untersucht einen möglichen Grund dafür und testet eine Wirkstoffstrategie, die gezielt die Verbindungen zwischen Nervenzellen schützt, statt die klassischen Plaques im Gehirn anzugreifen. Die Arbeit, durchgeführt in einem weit verbreiteten Mausmodell der Alzheimer-Krankheit, deutet darauf hin, dass das Stabilisieren fragiler Synapsen im Gedächtniszentrum des Gehirns selektiv das Gedächtnis bei weiblichen Tieren retten kann, die ein höheres Risiko tragen.
Ein winziges Gerüst im Zentrum des Gedächtnisses
Unsere Erinnerungen beruhen auf Billionen von Synapsen – mikroskopischen Kontaktpunkten, an denen Neuronen miteinander kommunizieren. An jeder exzitatorischen Synapse hilft ein Gerüstprotein namens PSD-95, Rezeptoren zu verankern, die chemische Signale empfangen. Damit PSD-95 an der richtigen Stelle bleibt, muss es mit Fettsäureketten bedeckt sein in einem reversiblen chemischen Prozess, der Palmitoylierung genannt wird. Frühere Arbeiten zeigten, dass PSD-95-Spiegel in frühen Stadien der Alzheimer-Krankheit abnehmen und dass die Palmitoylierung vieler Gehirnproteine verändert ist. Die Autoren fragten, ob sich die Palmitoylierung von PSD-95 zwischen Männchen und Weibchen unterscheidet und ob die Wiederherstellung dieser Modifikation Synapsen und Gedächtnis schützen könnte.
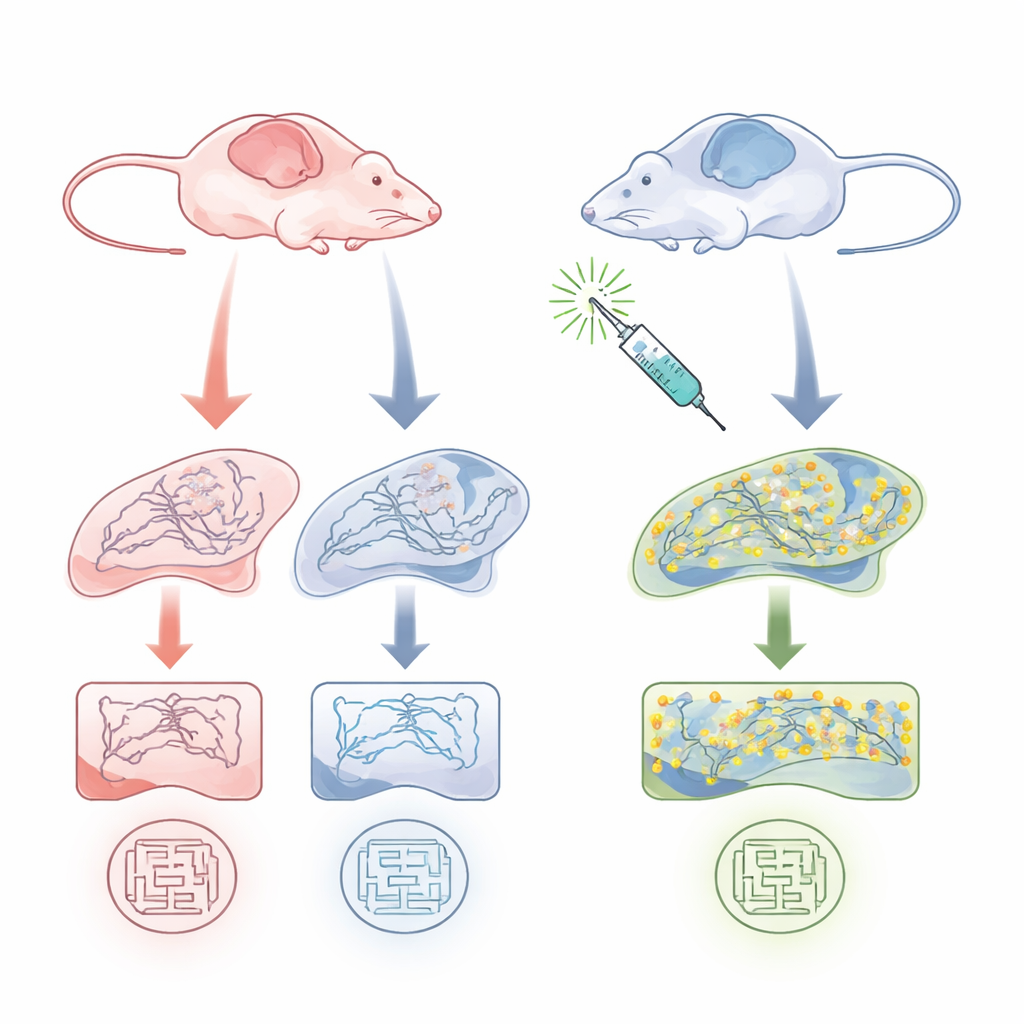
Weibliche Gehirne zeigen eine verborgene Schwäche
Das Team untersuchte 9–10 Monate alte APP/PS1-Mäuse, ein Standardmodell für Alzheimer, das Amyloid-Plaques und Gedächtnisprobleme entwickelt, und verglich sie mit gesunden Wurfgeschwistern. Sie konzentrierten sich auf den Hippocampus, eine zentrale Gedächtnisregion. Biochemische Tests zeigten, dass die gesamte Palmitoylierung vieler Proteine, und besonders die Palmitoylierung von PSD-95, bei weiblichen Alzheimer-Modellmäusen deutlich reduziert war, nicht jedoch bei Männchen. Wichtig war, dass die Gesamtmenge an PSD-95-Protein in diesem Alter zwischen den Gruppen ähnlich war – entscheidend war, wie viel davon in der palmitoylierten, synapsenstabilisierenden Form vorlag. Im Verhaltenstest zeigten nur die weiblichen Modellmäuse deutliche räumliche Gedächtnisdefizite im Wassermaze, während die Männchen etwa genauso gut abschnitten wie gesunde Kontrollen. Das deutet auf eine geschlechtsspezifische Verwundbarkeit hin, die PSD-95-Palmitoylierung, Synapsengesundheit und Gedächtnis verbindet.
Ein Wirkstoff, der PSD-95 an seinem Platz befestigt
Um zu testen, ob das Anheben der PSD-95-Palmitoylierung die Funktion wiederherstellen kann, verwendeten die Forscher Palmostatin B, eine Verbindung, die Enzyme blockiert, die Fettsäureketten von Proteinen entfernen, und die zuvor gezeigt hatte, dass sie PSD-95-Cluster in Neuronen vergrößert. Sie injizierten eine niedrige Dosis Palmostatin B in männliche und weibliche Alzheimer-Modellmäuse vor und während des Trainings im Wassermaze. Bei weiblichen Modellmäusen stellte die Behandlung die Leistung im Gedächtnistest nahezu auf Normalwerte wieder her, ohne die Schwimmgeschwindigkeit oder das Lernen einer sichtbaren Plattform zu verändern. Biochemische Analysen zeigten, dass Palmostatin B den Anteil von PSD-95 in seiner palmitoylierten Form im weiblichen Hippocampus deutlich erhöhte, während Gesamtpalmitoylierung und PSD-95-Gesamtspiegel weitgehend unverändert blieben. Bei Männchen, bei denen PSD-95-Palmitoylierung und Verhalten bereits normal waren, hatte das Medikament kaum einen Effekt.
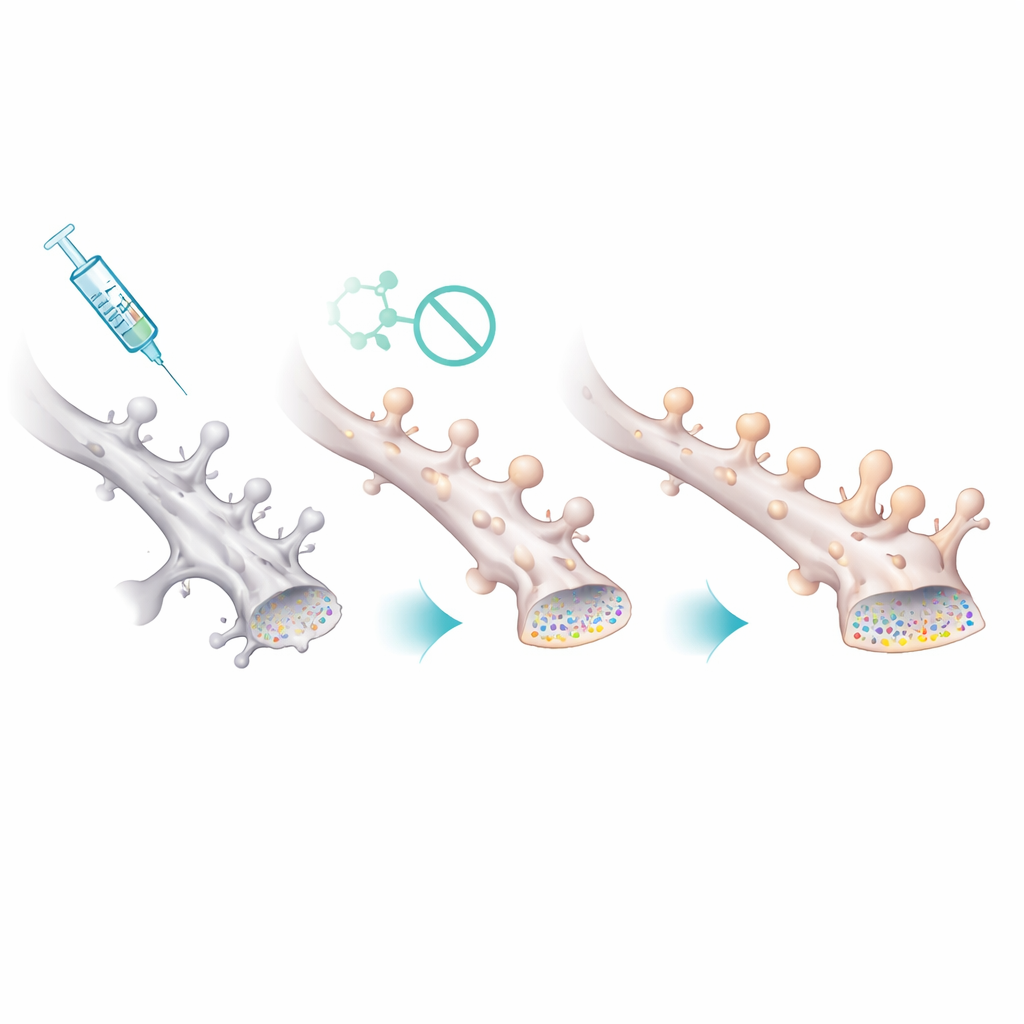
Schutz der kleinsten, empfindlichsten Synapsen
Wie übersetzte sich diese chemische Modifikation in gesündere Schaltkreise? Elektrophysiologische Aufzeichnungen aus Hippocampusneuronen zeigten, dass weibliche Alzheimer-Modellmäuse eine schwächere spontane synaptische Aktivität hatten, mit Ereignissen, die seltener, aber etwas größer auftraten – konsistent mit dem Verlust vieler kleiner Synapsen und dem Überleben weniger, größerer Synapsen. Nach der Behandlung mit Palmostatin B kehrten Frequenz und Größe dieser Ereignisse wieder in Richtung Normalwerte zurück. Mikroskopische Aufnahmen von dendritischen Dornen – den winzigen Vorsprüngen, die exzitatorische Synapsen beherbergen – bestätigten dieses Bild. Weibliche Modellmäuse hatten insgesamt weniger Dornen, und die verbleibenden waren ungewöhnlich groß. Das Medikament stellte die Dornendichte wieder her und verschob die Verteilung zurück zu vielen kleinen, dünnen Dornen, was darauf hindeutet, dass die Erhöhung der PSD-95-Palmitoylierung speziell die verwundbaren, feinen Verbindungen stabilisiert, die für flexibles Lernen besonders wichtig sind.
Nicht durch Beseitigung von Plaques, sondern durch Verstärkung von Verbindungen
Eine entscheidende Erkenntnis ist, was Palmostatin B nicht bewirkte. Die Behandlung reduzierte weder die Anzahl noch die Größe von Amyloid-Plaques, und sie veränderte nicht die Aktivierung benachbarter Stütz-Zellen, der Astrozyten. Stattdessen veränderte das Medikament das Verhältnis freier Fettsäuren zu palmitoylierten Proteinen geschlechtsabhängig und verbesserte synaptische Struktur und Funktion nur dort, wo die PSD-95-Palmitoylierung ursprünglich gering war. Das deutet darauf hin, dass die Rettung des Gedächtnisses von einer Verstärkung der Synapsen ausging und nicht von einer Bekämpfung der klassischen Alzheimer-Pathologie.
Was das für zukünftige Alzheimer-Therapien bedeutet
Für Nicht-Fachleute ist die zentrale Botschaft, dass Alzheimer nicht nur als Plaque-Krankheit gesehen werden sollte, sondern auch als Krankheit der versagenden Verbindungen – insbesondere bei Frauen. Diese Studie zeigt, dass das chemische „Verkleben" eines kritischen synaptischen Gerüstproteins durch Erhöhung seiner Fettschicht das Gedächtnis und die synaptische Gesundheit in weiblichen Alzheimer-Modellmäusen wiederherstellen kann, selbst nachdem bereits erhebliche Pathologie entstanden ist. Während Palmostatin B selbst nicht für den Einsatz am Menschen bereit ist und mehrere Ziele beeinflusst, hebt die Arbeit die Palmitoylierung von PSD-95 und deren Regulatoren als vielversprechende Ansatzpunkte für Therapien hervor, die Synapsen stärken und eines Tages denen helfen könnten, die am stärksten gefährdet sind.
Zitation: Du, Y., Prinkey, K., Pham, A.Q. et al. Sex-dependent rescue of memory and synaptic deficits in AD model mice by increasing PSD-95 palmitoylation. Commun Biol 9, 451 (2026). https://doi.org/10.1038/s42003-026-09702-y
Schlüsselwörter: Alzheimer-Krankheit, Synapsenverlust, PSD-95, Geschlechtsunterschiede, Palmitoylierung