Clear Sky Science · fr
Sauvetage dépendant du sexe des déficits de mémoire et synaptiques chez des souris modèle de la MA par l’augmentation de la palmitoylation de PSD-95
Pourquoi c’est important pour la santé cérébrale au quotidien
La maladie d’Alzheimer n’affecte pas tout le monde de la même façon : les femmes sont plus susceptibles que les hommes de développer des troubles de la mémoire, et leurs symptômes évoluent souvent plus rapidement. Cette étude explore une raison possible à cela — et teste une stratégie médicamenteuse qui protège directement les connexions entre neurones, plutôt que de cibler les plaques classiques du cerveau. Les travaux, réalisés dans un modèle murin largement utilisé de la maladie d’Alzheimer, suggèrent que renforcer des synapses fragiles dans le centre de la mémoire pourrait permettre de restaurer sélectivement la mémoire chez les femelles, qui présentent un risque plus élevé.
Un petit échafaudage au cœur de la mémoire
Nos souvenirs reposent sur des milliards de synapses — des points de contact microscopiques où les neurones communiquent. À chaque synapse excitatrice, une protéine d’échafaudage nommée PSD-95 aide à ancrer les récepteurs qui reçoivent les signaux chimiques. Pour que PSD-95 reste à sa place, elle doit être enduite de chaînes grasses via un processus réversible appelé palmitoylation. Des travaux antérieurs ont montré que les niveaux de PSD-95 diminuent tôt dans la maladie d’Alzheimer et que la palmitoylation de nombreuses protéines cérébrales est altérée. Les auteurs ont cherché à savoir si les modifications de la palmitoylation de PSD-95 différaient entre mâles et femelles, et si restaurer cette modification pouvait protéger les synapses et la mémoire.
Les cerveaux féminins révèlent une vulnérabilité cachée
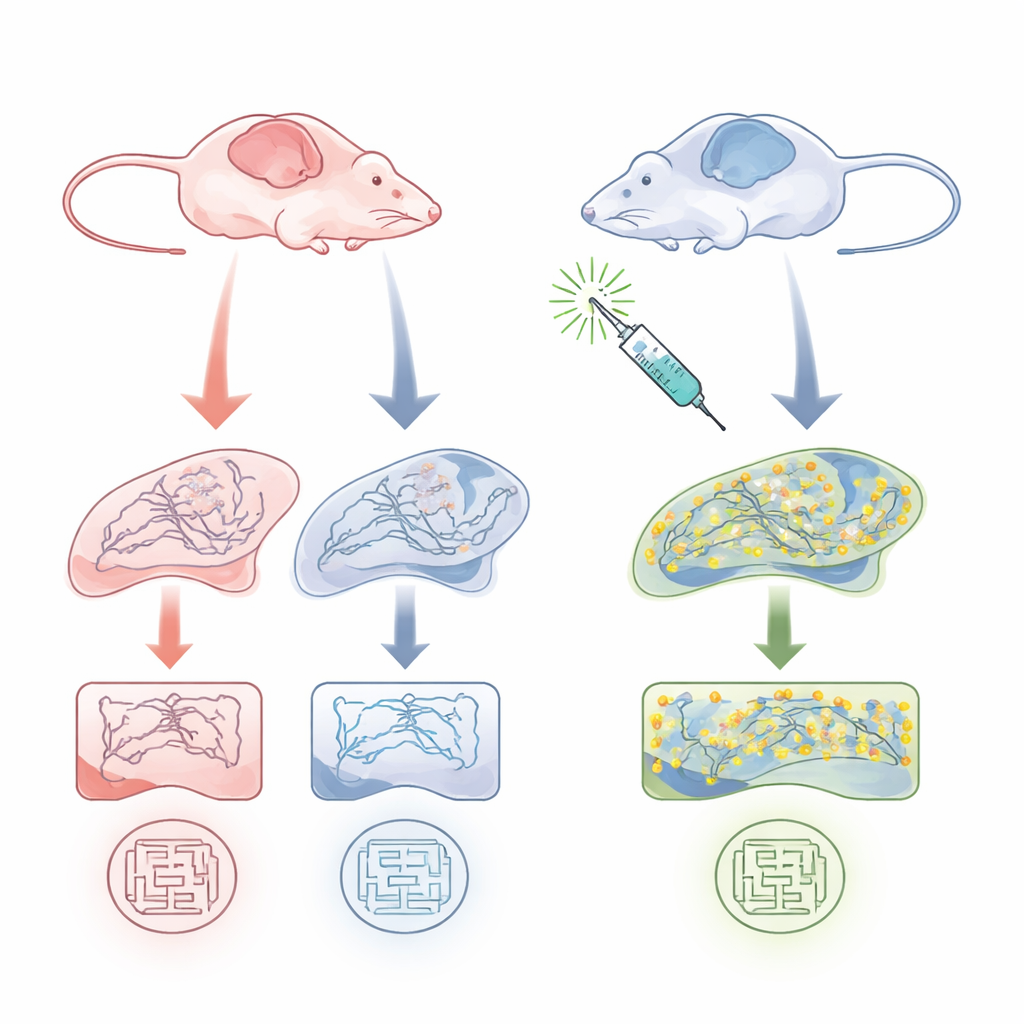
L’équipe a étudié des souris APP/PS1 âgées de 9 à 10 mois, un modèle standard de la maladie d’Alzheimer qui développe des plaques amyloïdes et des troubles de la mémoire, et les a comparées à des congénères sains. Ils se sont concentrés sur l’hippocampe, une région clé de la mémoire. Par des essais biochimiques, ils ont constaté que la palmitoylation totale de nombreuses protéines, et en particulier la palmitoylation de PSD-95, était nettement réduite chez les souris modèles féminines, mais pas chez les mâles. Importamment, la quantité globale de protéine PSD-95 était similaire entre les groupes à cet âge — ce qui différait était la proportion sous forme palmitoylée, stabilisante pour les synapses. Au niveau comportemental, seules les femelles modèles présentaient des déficits spatiaux évidents dans une épreuve du labyrinthe aquatique, tandis que les mâles se comportaient à peu près comme les témoins sains. Cela montre une vulnérabilité spécifique au sexe reliant la palmitoylation de PSD-95, la santé synaptique et la mémoire.
Un médicament qui verrouille PSD-95 en place
Pour tester si augmenter la palmitoylation de PSD-95 pouvait restaurer la fonction, les chercheurs ont utilisé le Palmostatin B, un composé qui bloque les enzymes dépalmitylantes et qui avait précédemment été montré pour agrandir les amas de PSD-95 dans les neurones. Ils ont injecté une faible dose de Palmostatin B à des souris modèles mâles et femelles avant et pendant l’entraînement au labyrinthe aquatique. Chez les femelles modèles, le traitement a ramené les performances au test de mémoire proche des niveaux normaux, sans modifier la vitesse de nage ni l’apprentissage de la localisation d’une plateforme visible. L’analyse biochimique a montré que le Palmostatin B augmentait sensiblement la fraction de PSD-95 sous forme palmitoylée dans l’hippocampe féminin, tout en laissant la palmitoylation totale et les niveaux de PSD-95 globalement inchangés. Chez les mâles, où la palmitoylation de PSD-95 et le comportement étaient déjà normaux, le médicament n’a eu que peu d’effet.
Protéger les synapses les plus petites et les plus fragiles
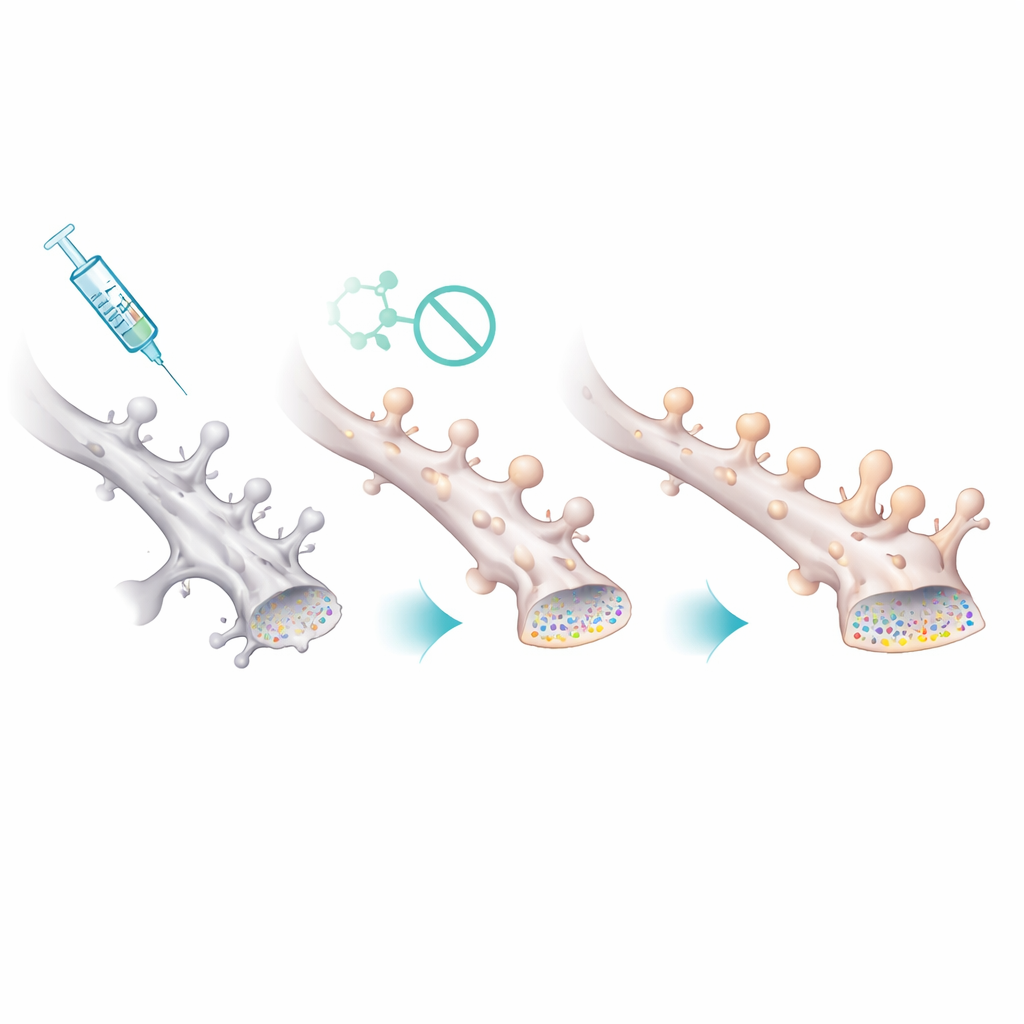
Comment cette modification chimique s’est-elle traduite en circuits plus sains ? Des enregistrements électrophysiologiques de neurones hippocampiques ont révélé que les femelles modèles avaient une activité synaptique spontanée plus faible, avec des événements moins fréquents mais d’amplitude légèrement plus importante — cohérent avec la perte de nombreuses petites synapses et la survie de quelques synapses plus grosses. Après traitement au Palmostatin B, la fréquence et l’amplitude de ces événements sont revenues vers la normale. L’imagerie microscopique des épines dendritiques — les petites protrusions qui abritent les synapses excitatrices — a confirmé ce constat. Les femelles modèles présentaient moins d’épines au total, et celles restantes étaient anormalement grandes. Le médicament a rétabli la densité d’épines et a réorienté la distribution vers de nombreuses petites épines fines, suggérant que l’augmentation de la palmitoylation de PSD-95 stabilise spécifiquement les connexions fines et vulnérables qui sont les plus importantes pour un apprentissage flexible.
Pas en supprimant les plaques, mais en renforçant les connexions
Un résultat crucial est ce que le Palmostatin B n’a pas fait. Le traitement n’a pas réduit le nombre ou la taille des plaques amyloïdes, ni modifié l’activation des cellules de soutien voisines appelées astrocytes. À la place, le médicament a modifié l’équilibre des acides gras libres et des protéines palmitoylées de façon dépendante du sexe et a amélioré la structure et la fonction synaptique uniquement là où la palmitoylation de PSD-95 était initialement faible. Cela indique que la restauration de la mémoire provient du renforcement des synapses plutôt que d’une action contre la pathologie classique de la maladie d’Alzheimer.
Ce que cela signifie pour les futures thérapies contre la maladie d’Alzheimer
Pour le grand public, le message clé est que la maladie d’Alzheimer peut être vue non seulement comme une maladie des plaques, mais comme une maladie des connexions défaillantes — en particulier chez les femmes. Cette étude montre que « coller » chimiquement un échafaudage synaptique critique en renforçant son manteau gras peut restaurer la mémoire et la santé synaptique chez des souris modèles féminines de la maladie d’Alzheimer, même après l’apparition d’une pathologie importante. Bien que le Palmostatin B lui-même ne soit pas prêt pour un usage humain et cible plusieurs protéines, ces travaux mettent en lumière la palmitoylation de PSD-95 et ses régulateurs comme des pistes prometteuses pour des thérapies visant à renforcer les synapses et éventuellement protéger les personnes les plus à risque.
Citation: Du, Y., Prinkey, K., Pham, A.Q. et al. Sex-dependent rescue of memory and synaptic deficits in AD model mice by increasing PSD-95 palmitoylation. Commun Biol 9, 451 (2026). https://doi.org/10.1038/s42003-026-09702-y
Mots-clés: Maladie d’Alzheimer, perte de synapses, PSD-95, différences entre les sexes, palmitoylation