Clear Sky Science · es
Rescate dependiente del sexo de déficits de memoria y sinápticos en ratones modelo de EA mediante el aumento de la palmitoilación de PSD-95
Por qué esto importa para la salud cerebral cotidiana
La enfermedad de Alzheimer no afecta a todo el mundo por igual: las mujeres tienen más probabilidades que los hombres de desarrollar pérdida de memoria y sus síntomas suelen empeorar más rápido. Este estudio explora una posible razón y prueba una estrategia farmacológica que protege directamente las conexiones entre neuronas, en lugar de centrarse en las placas clásicas del cerebro. El trabajo, realizado en un modelo de ratón ampliamente usado de Alzheimer, sugiere que reforzar sinapsis frágiles en el centro de la memoria del cerebro podría rescatar selectivamente la memoria en las hembras, que están en mayor riesgo.
Un andamiaje diminuto en el corazón de la memoria
Nuestras memorias dependen de billones de sinapsis: puntos de contacto microscópicos donde las neuronas se comunican. En cada sinapsis excitatoria, una proteína andamiaje llamada PSD-95 ayuda a anclar los receptores que reciben señales químicas. Para que PSD-95 permanezca en el lugar correcto, debe estar recubierta por cadenas grasas mediante un proceso químico reversible llamado palmitoilación. Trabajos previos mostraron que los niveles de PSD-95 caen al inicio de la enfermedad de Alzheimer y que la palmitoilación de muchas proteínas cerebrales está alterada. Los autores se preguntaron si los cambios en la palmitoilación de PSD-95 podrían diferir entre machos y hembras, y si restaurar esta modificación podría proteger sinapsis y memoria.
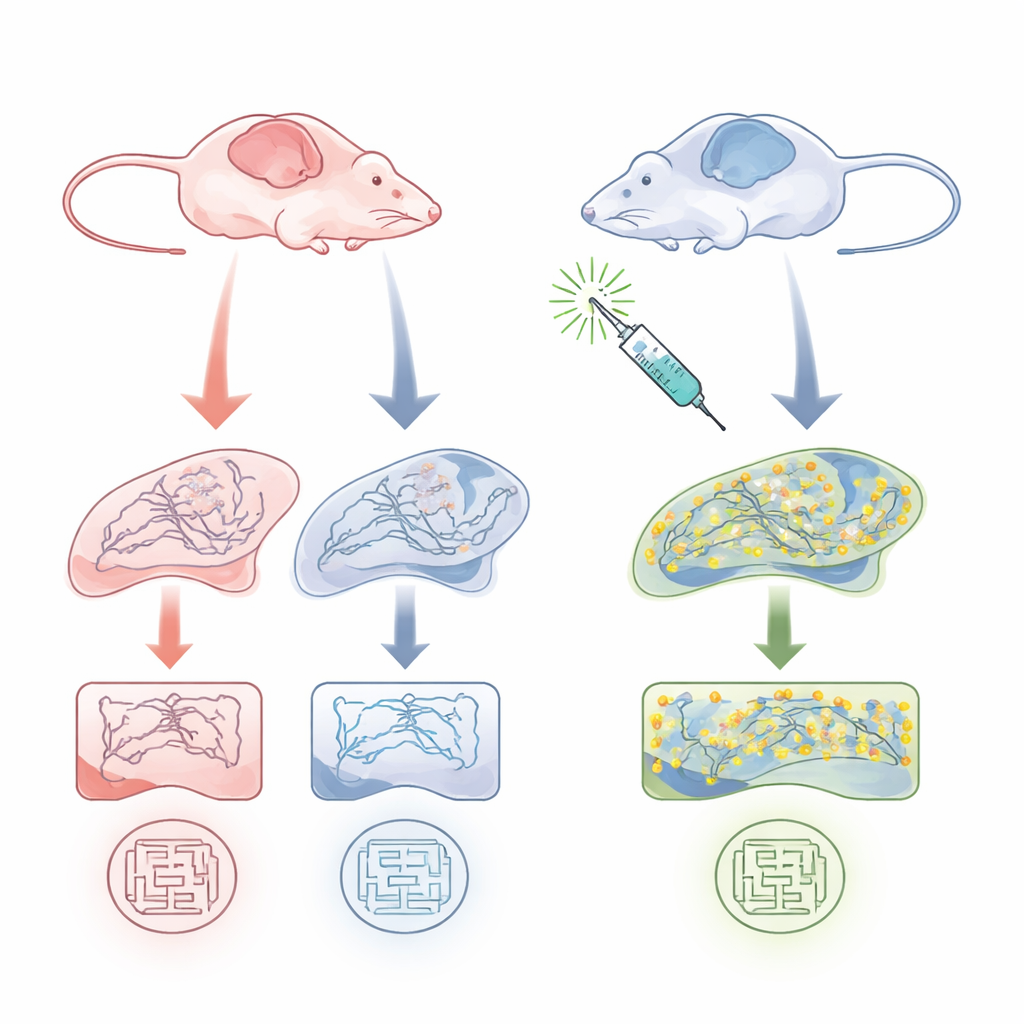
Los cerebros femeninos muestran una debilidad oculta
El equipo estudió ratones APP/PS1 de 9–10 meses, un modelo estándar de Alzheimer que desarrolla placas amiloides y problemas de memoria, y los comparó con compañeros de camada sanos. Se centraron en el hipocampo, una región clave para la memoria. Mediante ensayos bioquímicos, encontraron que la palmitoilación total de muchas proteínas, y en especial la palmitoilación de PSD-95, se redujo de forma marcada en las ratonas del modelo de Alzheimer, pero no en los machos. Es importante que la cantidad total de proteína PSD-95 fue similar entre los grupos a esa edad: lo que difería era cuánto de ella estaba en la forma palmitoilada que estabiliza la sinapsis. A nivel conductual, solo las hembras del modelo mostraron déficits claros en la memoria espacial en una prueba del laberinto acuático, mientras que los machos se desempeñaron más o menos igual que los controles sanos. Esto apuntó a una vulnerabilidad específica por sexo que relaciona la palmitoilación de PSD-95, la salud sináptica y la memoria.
Un fármaco que fija PSD-95 en su sitio
Para probar si aumentar la palmitoilación de PSD-95 podía rescatar la función, los investigadores usaron Palmostatin B, un compuesto que bloquea enzimas que quitan las cadenas grasas de las proteínas y que previamente se había demostrado que agranda los agregados de PSD-95 en neuronas. Inyectaron una baja dosis de Palmostatin B en ratones machos y hembras del modelo de Alzheimer antes y durante el entrenamiento en el laberinto acuático. En las hembras del modelo, el tratamiento restauró el rendimiento en la prueba de memoria a niveles cercanos a los normales, sin cambiar la velocidad de natación ni el aprendizaje para encontrar una plataforma visible. El análisis bioquímico mostró que Palmostatin B aumentó sustancialmente la fracción de PSD-95 en su forma palmitoilada en el hipocampo femenino, mientras que dejó la palmitoilación total y los niveles totales de PSD-95 en gran parte sin cambios. En los machos, donde la palmitoilación de PSD-95 y la conducta ya eran normales, el fármaco tuvo poco efecto.
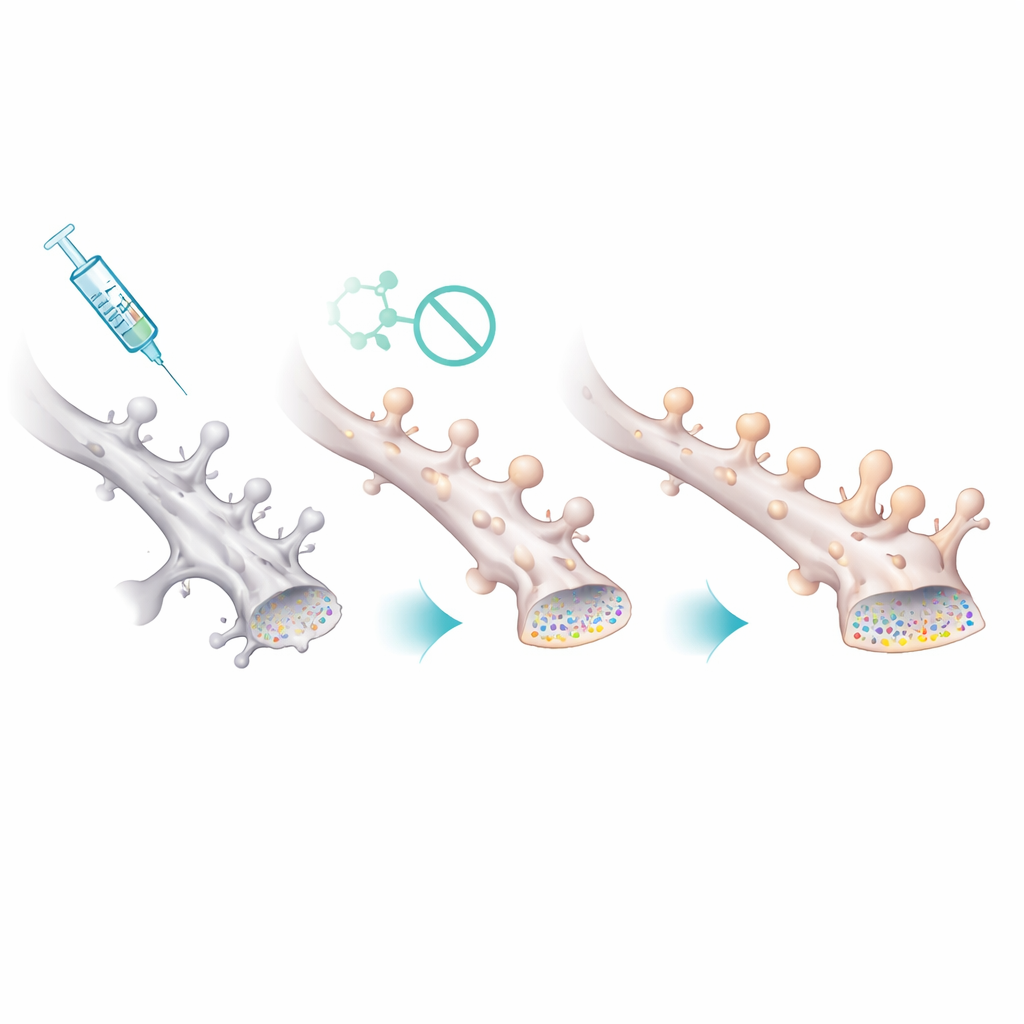
Protegiendo las sinapsis más pequeñas y frágiles
¿Cómo se tradujo este ajuste químico en circuitos más saludables? Registros electrofisiológicos de neuronas del hipocampo revelaron que las hembras del modelo de Alzheimer tenían actividad sináptica espontánea más débil, con eventos que ocurrían con menor frecuencia pero de tamaño algo mayor, coherente con la pérdida de muchas sinapsis pequeñas y la supervivencia de menos sinapsis más grandes. Tras el tratamiento con Palmostatin B, la frecuencia y el tamaño de estos eventos retornaron hacia la normalidad. La imagen microscópica de espinas dendríticas —las diminutas protuberancias que alojan sinapsis excitatorias— confirmó este panorama. Las hembras del modelo tenían menos espinas en general, y las que quedaban eran anormalmente grandes. El fármaco restauró la densidad de espinas y desplazó la distribución de nuevo hacia muchas espinas pequeñas y delgadas, lo que sugiere que aumentar la palmitoilación de PSD-95 estabiliza específicamente las conexiones finas y vulnerables que son más importantes para el aprendizaje flexible.
No por eliminar placas, sino por reforzar conexiones
Un hallazgo crucial es lo que Palmostatin B no hizo. El tratamiento no redujo el número ni el tamaño de las placas amiloides, ni cambió la activación de las células de soporte cercanas conocidas como astrocitos. En cambio, el fármaco alteró el equilibrio entre ácidos grasos libres y proteínas palmitoiladas de forma dependiente del sexo y mejoró la estructura y función sináptica solo donde la palmitoilación de PSD-95 era inicialmente baja. Esto indica que el rescate de la memoria provino de reforzar las sinapsis en lugar de atacar la patología clásica del Alzheimer.
Qué significa esto para futuras terapias contra el Alzheimer
Para el público general, el mensaje clave es que el Alzheimer puede verse no solo como una enfermedad de placas, sino como una enfermedad de conexiones que fallan, especialmente en mujeres. Este estudio muestra que “pegando” químicamente un andamiaje sináptico crítico en su lugar, aumentando su recubrimiento graso, puede restaurar la memoria y la salud sináptica en ratonas de un modelo de Alzheimer, incluso después de que se haya desarrollado una patología sustancial. Si bien Palmostatin B en sí no está listo para uso humano y actúa sobre más de un objetivo, el trabajo destaca la palmitoilación de PSD-95 y sus reguladores como pistas prometedoras para terapias que fortalezcan las sinapsis y que algún día podrían ayudar a proteger a quienes tienen mayor riesgo.
Cita: Du, Y., Prinkey, K., Pham, A.Q. et al. Sex-dependent rescue of memory and synaptic deficits in AD model mice by increasing PSD-95 palmitoylation. Commun Biol 9, 451 (2026). https://doi.org/10.1038/s42003-026-09702-y
Palabras clave: Enfermedad de Alzheimer, pérdida de sinapsis, PSD-95, diferencias entre sexos, palmitoilación