Clear Sky Science · he
הצלת תלותית במין של פגמים בזיכרון ובסינפסות בעכברים בדגם של אלצהיימר על ידי הגברת פלמיטוילציה של PSD-95
מדוע זה חשוב לבריאות המוח היומיומית
מחלת אלצהיימר אינה פוגעת בכל אדם באותה מידה: נשים נוטות יותר מגברים לפתח אובדן זיכרון ותסמיניהן לעתים מחמירים מהר יותר. מחקר זה חוקר סיבה אפשרית אחת לכך — ובוחן אסטרטגיית תרופה שמגנה ישירות על החיבורים בין תאי העצב, במקום לכוון לפלטות הקלאסיות במוח. העבודה, המבוססת על דגם עכבר נפוץ של אלצהיימר, מצביעה על כך שחיזוק סינפסות שבריריות במרכז הזיכרון של המוח עשוי להציל באופן סלקטיבי את הזיכרון בנקבות הנמצאות בסיכון גבוה יותר.
תבנית זעירה בלב הזיכרון
הזיכרונות שלנו מסתמכים על טריליוני סינפסות — נקודות מגע מיקרוסקופיות שבהן נוירונים מתקשרים זה עם זה. בכל סינפסה מעוררת יש חלבון שלד הנקרא PSD-95 שעוזר לעגן קולטנים המקבלים אותות כימיים. כדי ש-PSD-95 יישאר במיקום הנכון עליו להיות מצופה בשרשראות שומניות בתהליך כימי הפיך שנקרא פלמיטוילציה. עבודות קודמות הראו שרמות PSD-95 נפגעות מוקדם במחלת אלצהיימר ושהפלמיטוילציה של חלבונים רבים במוח משתנה. החוקרים תהו האם השינויים בפלמיטוילציה של PSD-95 עשויים להשתנות בין זכרים לנקבות, והאם שיקום המודיפיקציה הזו יכול להגן על סינפסות וזיכרון.
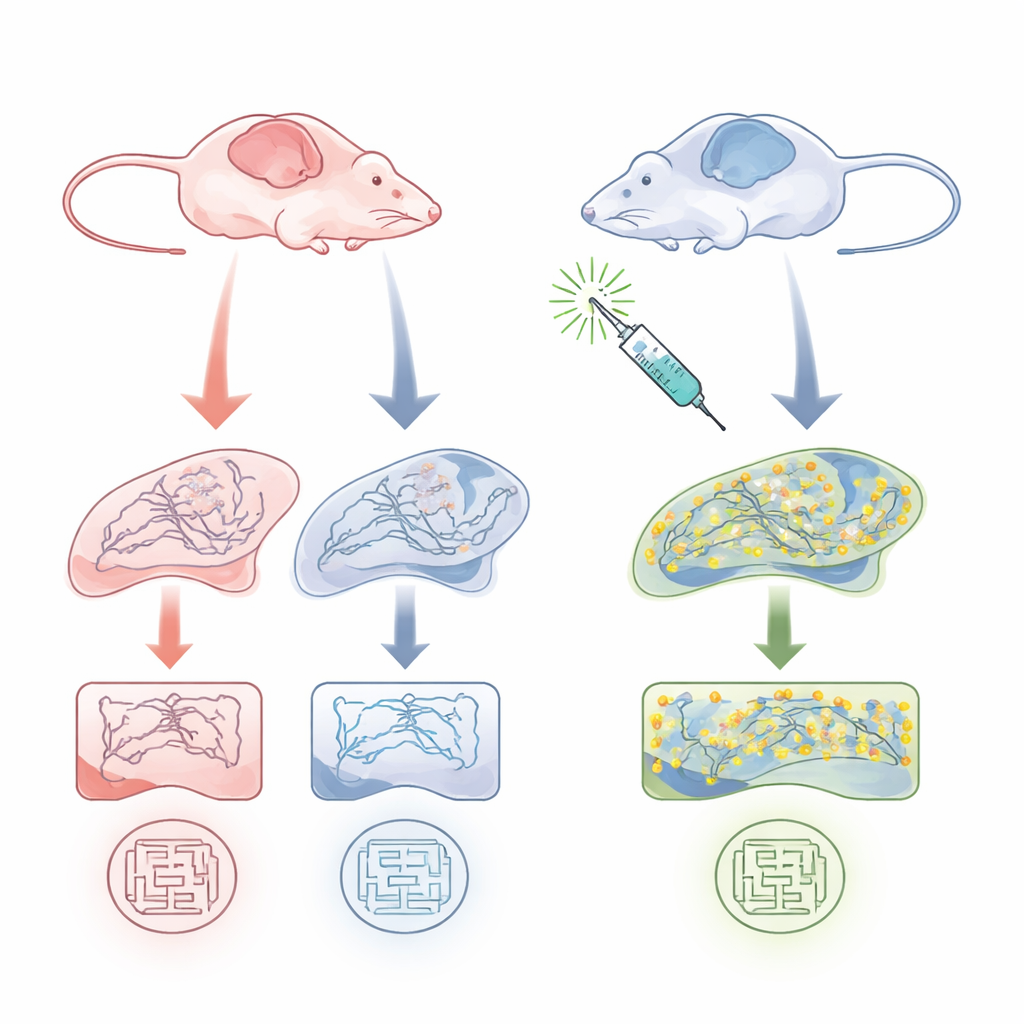
מוחות נקבות מגלים חולשה חבויה
הצוות חקר עכברי APP/PS1 בני 9–10 חודשים, דגם סטנדרטי של אלצהיימר המפתח פלאקות אמילואידיות ובעיות זיכרון, והשווה אותם לאחיותיהם הבריאות. הם התמקדו בהיפוקמפוס, אזור מרכזי לזיכרון. בעזרת בדיקות ביוכימיות נמצא כי הפלמיטוילציה הכוללת של חלבונים רבים, ובפרט הפלמיטוילציה של PSD-95, ירדה באופן מובהק בעכברי הדגם הנקבות אך לא בזכרים. חשוב לציין שכמות ה-PSD-95 הכוללת הייתה דומה בקבוצות בגיל זה — מה ששונה היה כמה ממנו נמצא בצורתו המפלמיטוילטת, המייצבת סינפסות. בהתנהגות, רק עכברי הדגם הנקבות הראו פגיעות ברורה בזיכרון מרחבי במשימת מבוך המים, בעוד שהזכרים הופיעו בביצועים דומים לשליטה הבריאה. ממצא זה מצביע על פגיעות תלוית־מין המקשרת בין פלמיטוילציה של PSD-95, בריאות הסינפסה והזיכרון.
תרופה שמנעלת את PSD-95 במקומו
כדי לבחון האם הגברה של פלמיטוילציה של PSD-95 יכולה להציל פונקציה, החוקרים השתמשו בפਲמוסטטין B, תרכובת החוסמת אנזימים המסירים שרשראות שומניות מחלבונים ושנודעה בעבר כמגדילת אשכולות PSD-95 בנוירונים. הם הזריקו מנה נמוכה של פלמוסטטין B לעכברי דגם אלצהיימר זכרים ונקבות לפני ובמהלך אימוני מבוך המים. בעכברי הדגם הנקבות הטיפול השיב את הביצועים בבדיקת פרוב לזיכרון לערכים קרובים לנורמליים, מבלי לשנות את מהירות השחייה או את קצב הלמידה של מציאת פלטפורמה נראית. ניתוח ביוכימי הראה שפלמוסטטין B הגדיל באופן ניכר את החלק של PSD-95 בצורתו המפלמיטוילטת בהיפוקמפוס הנקבי, בעוד שהפלמיטוילציה הכוללת ורמות ה-PSD-95 נשארו ברובן ללא שינוי. אצל הזכרים, שבהם הפלמיטוילציה של PSD-95 וההתנהגות כבר היו תקינות, לתרופה הייתה השפעה מזערית.
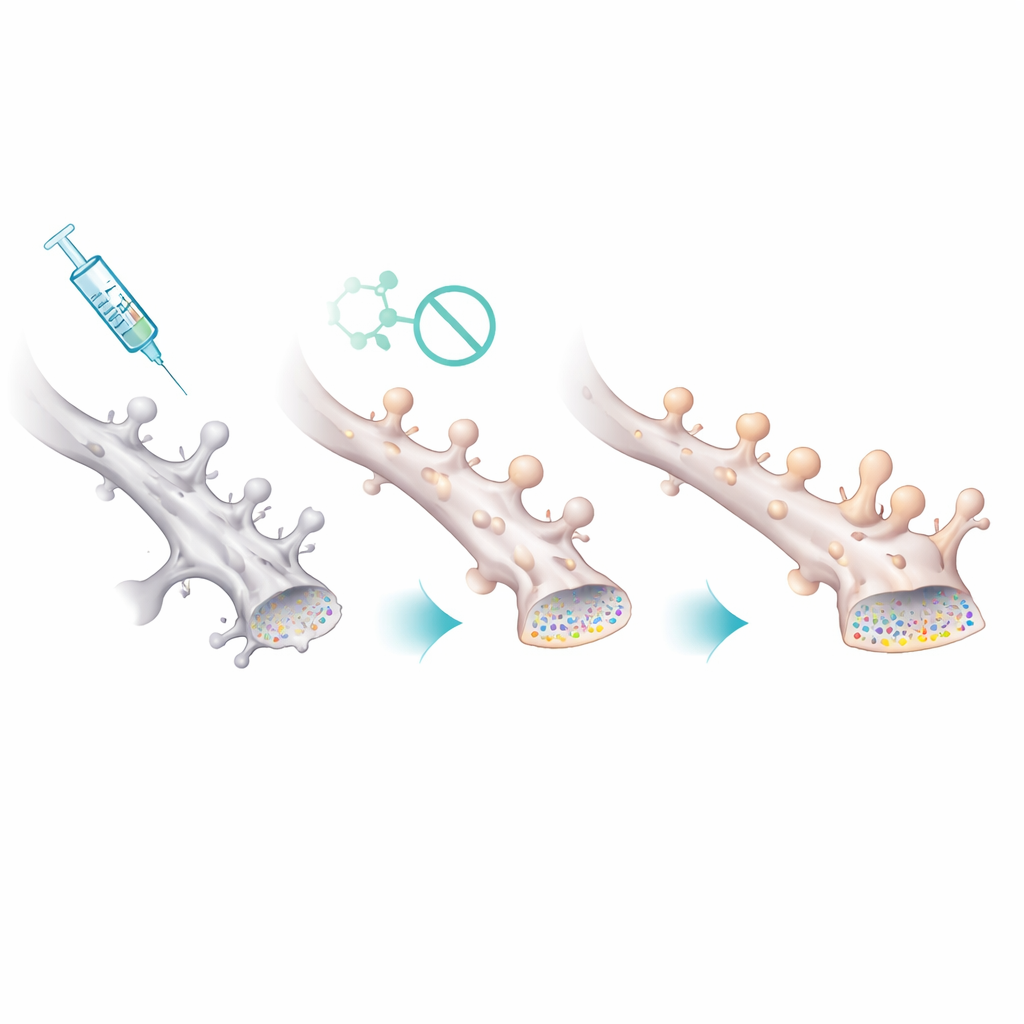
הגנה על הסינפסות הקטנות והשבריריות ביותר
איך השינוי הכימי הזה תורגם למעגלים בריאים יותר? הקלטות אלקטרופיזיולוגיות מתאי עצב בהיפוקמפוס חשפו שעכברי הדגם הנקבות הראו פעילות סינפטית ספונטנית חלשה יותר, עם אירועים המתרחשים בתדירות נמוכה אך בגודל מעט גדול יותר — תואם לאובדן של סינפסות רבות וקטנות ולשרידות של פחות, גדולות יותר. לאחר טיפול בפלמוסטטין B חזרו תדירות וגודל האירועים לכיוון נורמלי. דימות מיקרוסקופי של הקוצים הדנדריטיים — הבליטות הזעירות שמכילות סינפסות מעוררות — אישר תמונה זו. לעכברי הדגם הנקבות היו פחות קוצים באופן כללי, והקוצים שנותרו היו גדולים באופן חריג. התרופה שחזרה את צפיפות הקוצים והזיזה את ההתפלגות חזרה לעבר הרבה קוצים קטנים ודקים, מה שמרמז שהגברת הפלמיטוילציה של PSD-95 מייצבת באופן ספציפי את החיבורים העדינים הרגישים שחשובים ביותר ללמידה גמישה.
לא על ידי ניקוי פלאקות, אלא על ידי חיזוק חיבורים
ממצא מכריע הוא מה שפלמוסטטין B לא עשה. הטיפול לא הקטין את מספר או את גודל הפלאקות האמילואידיות, ולא שינה את הפעילות של תאי תמיכה סמוכים הידועים כאסטרוציטים. במקום זאת, התרופה שינתה את האיזון בין חומצות שומן חופשיות לחלבונים מפלמיטוילטים באופן תלוית־מין ושיפרה מבנה ותפקוד סינפטי רק היכן שפלמיטוילציה של PSD-95 הייתה נמוכה בתחילה. הדבר מרמז שההצלה של הזיכרון נבעה מחיזוק הסינפסות ולא מהתקפה על פתולוגיית האלצהיימר הקלאסית.
מה משמעות הדבר עבור טיפולים עתידיים באלצהיימר
ללא מומחיות מיוחדת, המסר המרכזי הוא כי ניתן לראות באלצהיימר לא רק מחלה של פלאקות, אלא גם מחלה של קריסת חיבורים — במיוחד בנשים. מחקר זה מראה כי "הדבקת" כימית של שלד סינפטי קריטי בעזרת הגברת הציפוי השומני שלו יכולה לשקם זיכרון ובריאות סינפטית בעכברות בדגם של אלצהיימר, גם לאחר שהתפתחה פתולוגיה משמעותית. בעוד שפלאמוסטטין B עצמו אינו מוכן לשימוש אנושי ומשפיע על יותר ממטרה אחת, העבודה מדגישה את פלמיטוילציה של PSD-95 ואת המווסתים שלה כמובילים מבטיחים לטיפולים שמחזקים סינפסות ועלולים יום אחד לעזור להגן על אלה בסיכון הגבוה ביותר.
ציטוט: Du, Y., Prinkey, K., Pham, A.Q. et al. Sex-dependent rescue of memory and synaptic deficits in AD model mice by increasing PSD-95 palmitoylation. Commun Biol 9, 451 (2026). https://doi.org/10.1038/s42003-026-09702-y
מילות מפתח: מחלת אלצהיימר, אובדן סינפסות, PSD-95, הבדלים בין המינים, פלמיטוילציה