Clear Sky Science · nl
Geslachtsafhankelijke herstel van geheugen- en synaptische tekorten in AD-modelmuizen door toename van PSD-95-palmitoylering
Waarom dit van belang is voor alledaagse hersengezondheid
De ziekte van Alzheimer treft niet iedereen gelijk: vrouwen lopen meer risico dan mannen op geheugenverlies en hun klachten verergeren vaak sneller. Deze studie onderzoekt één mogelijke verklaring en test een geneesmiddelstrategie die rechtstreeks de verbindingen tussen zenuwcellen beschermt, in plaats van de klassieke hersenplaques te richten. Het werk, uitgevoerd in een veelgebruikt muismodel van Alzheimer, suggereert dat het verstevigen van kwetsbare synapsen in het geheugencentrum van de hersenen selectief het geheugen bij vrouwtjes zou kunnen herstellen die een hoger risico lopen.
Een klein steigerwerk in het hart van het geheugen
Onze herinneringen berusten op biljoenen synapsen — microscopische contactpunten waar neuronen met elkaar communiceren. Bij elke exciterende synaps helpt een steigerproteïne genaamd PSD-95 receptoren te verankeren die chemische signalen ontvangen. Om PSD-95 op de juiste plek te houden, moet het worden gecoat met vetachtige ketens in een omkeerbaar chemisch proces dat palmitoylering heet. Eerder werk toonde aan dat PSD-95-niveaus vroeg dalen bij Alzheimer en dat de palmitoylering van veel herseneiwitten veranderd is. De auteurs vroegen of veranderingen in PSD-95-palmitoylering tussen mannetjes en vrouwtjes konden verschillen, en of het herstellen van deze modificatie synapsen en geheugen zou beschermen.
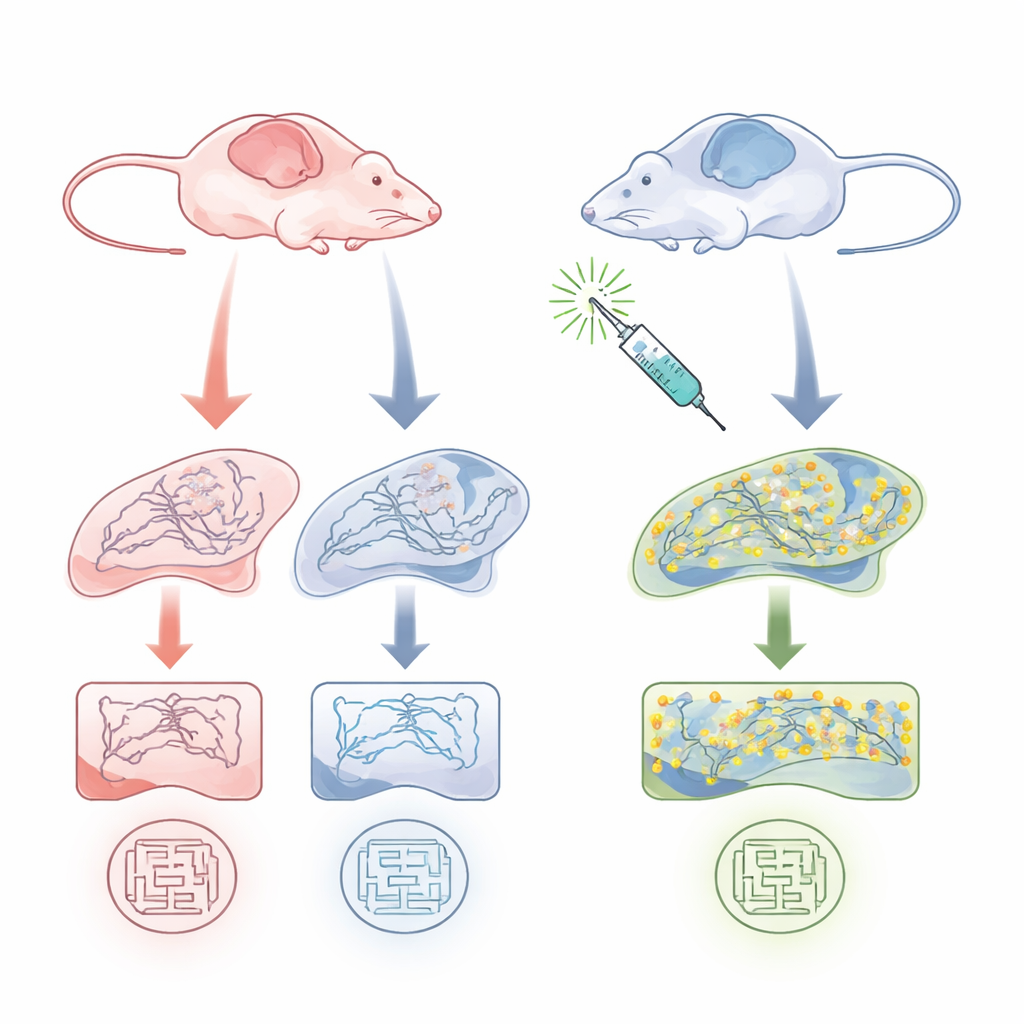
Vrouwelijke hersenen tonen een verborgen zwakte
Het team bestudeerde 9–10 maanden oude APP/PS1-muizen, een standaard Alzheimer-model dat amyloïde plaques en geheugenproblemen ontwikkelt, en vergeleek ze met gezonde nestgenoten. Ze concentreerden zich op de hippocampus, een belangrijke geheugenregio. Met biochemische assays vonden ze dat de totale palmitoylering van veel eiwitten, en in het bijzonder de palmitoylering van PSD-95, duidelijk gereduceerd was in vrouwelijke Alzheimer-modelmuizen maar niet in mannelijke. Belangrijk is dat de totale hoeveelheid PSD-95-eiwit op deze leeftijd vergelijkbaar was tussen de groepen — wat verschilde, was hoeveel daarvan in de gepalmitoyleerde, synapsstabiliserende vorm voorkwam. In gedragstests toonden alleen vrouwelijke modelmuizen duidelijke ruimtelijke geheugenstoornissen in een watermaze-taak, terwijl mannetjes ongeveer even goed presteerden als gezonde controles. Dit wees op een geslachtsspecifieke kwetsbaarheid die PSD-95-palmitoylering, synapsgezondheid en geheugen verbindt.
Een middel dat PSD-95 op zijn plaats verankert
Om te testen of het verhogen van PSD-95-palmitoylering functie kon herstellen, gebruikten de onderzoekers Palmostatin B, een verbinding die enzymen blokkeert die vetketens van eiwitten verwijderen en eerder was aangetoond dat het PSD-95-clusters in neuronen vergroot. Ze gaven een lage dosis Palmostatin B aan mannelijke en vrouwelijke Alzheimer-modelmuizen vóór en tijdens de training in de watermaze. Bij vrouwelijke modelmuizen herstelde de behandeling de prestatie in de geheugentest tot bijna normale niveaus, zonder de zwemsnelheid of het leren een zichtbaar platform te vinden te veranderen. Biochemische analyse toonde aan dat Palmostatin B het aandeel PSD-95 in zijn gepalmitoyleerde vorm in de vrouwelijke hippocampus aanzienlijk verhoogde, terwijl de totale palmitoylering en PSD-95-niveaus grotendeels onveranderd bleven. Bij mannetjes, waarbij PSD-95-palmitoylering en gedrag al normaal waren, had het middel weinig effect.
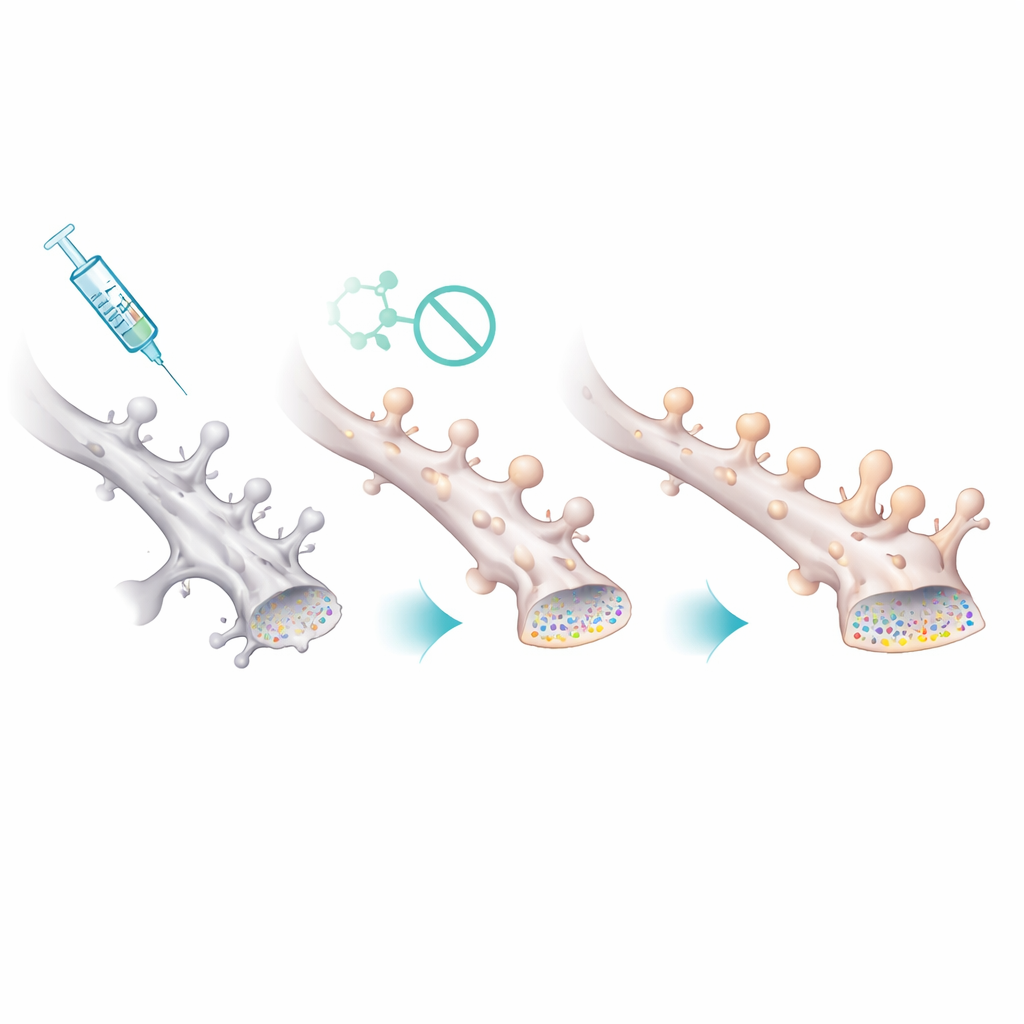
Het beschermen van de kleinste, meest kwetsbare synapsen
Hoe vertaalde deze chemische aanpassing zich naar gezondere circuits? Elektrofysiologische opnamen van hippocampale neuronen lieten zien dat vrouwelijke Alzheimer-modelmuizen zwakkere spontane synaptische activiteit hadden, met gebeurtenissen die minder vaak voorkwamen maar iets groter van amplitude waren — in overeenstemming met het verlies van vele kleine synapsen en het overleven van minder, grotere synapsen. Na behandeling met Palmostatin B keerden frequentie en grootte van deze gebeurtenissen weer richting normaal. Microscopische beeldvorming van dendritische spines — de kleine uitstulpingen die exciterende synapsen huisvesten — bevestigde dit beeld. Vrouwelijke modelmuizen hadden minder spines in totaal, en de overgebleven spines waren abnormaal groot. Het middel herstelde de spinedichtheid en verschuiven van de verdeling terug naar veel kleine, dunne spines, wat suggereert dat het verhogen van PSD-95-palmitoylering specifiek de kwetsbare, fijne verbindingen stabiliseert die het belangrijkst zijn voor flexibel leren.
Niet door plaques te verwijderen, maar door verbindingen te versterken
Een cruciale bevinding is wat Palmostatin B niet deed. De behandeling verminderde niet het aantal of de grootte van amyloïde plaques, noch veranderde het de activatie van nabijgelegen ondersteunende cellen bekend als astrocyten. In plaats daarvan veranderde het middel de balans van vrije vetzuren en gepalmitoyleerde eiwitten op een geslachtsafhankelijke manier en verbeterde het synaptische structuur en functie alleen daar waar PSD-95-palmitoylering aanvankelijk laag was. Dit wijst erop dat het herstel van geheugen voortkwam uit het versterken van synapsen in plaats van het bestrijden van klassieke Alzheimer-pathologie.
Wat dit betekent voor toekomstige Alzheimer-behandelingen
Voor niet-specialisten is de kernboodschap dat Alzheimer niet alleen gezien moet worden als een ziekte van plaques, maar ook als een ziekte van falende verbindingen — vooral bij vrouwen. Deze studie toont aan dat het chemisch "vastlijmen" van een kritisch synaptisch steigerwerk op zijn plaats door het versterken van zijn vetlaag geheugen en synaptische gezondheid kan herstellen in vrouwelijke Alzheimer-modelmuizen, zelfs nadat er aanzienlijke pathologie is ontwikkeld. Hoewel Palmostatin B zelf niet klaar is voor gebruik bij mensen en meer dan één doelwit beïnvloedt, benadrukt het werk PSD-95-palmitoylering en zijn regulatoren als veelbelovende aanknopingspunten voor therapieën die synapsen versterken en op een dag mogelijk degenen met het grootste risico kunnen beschermen.
Bronvermelding: Du, Y., Prinkey, K., Pham, A.Q. et al. Sex-dependent rescue of memory and synaptic deficits in AD model mice by increasing PSD-95 palmitoylation. Commun Biol 9, 451 (2026). https://doi.org/10.1038/s42003-026-09702-y
Trefwoorden: Ziekte van Alzheimer, verlies van synapsen, PSD-95, geslachtsverschillen, palmitoylering