Clear Sky Science · pt
Dinâmica de um catalisador Cu/ZnO/Al2O3 revelada por microscopia eletrônica de transmissão operando durante a hidrogenação do CO2
Transformando um problema climático em um líquido útil
Dióxido de carbono costuma ser visto apenas como um gás residual que aquece nosso planeta, mas a indústria também pode convertê‑lo em metanol, um líquido que armazena energia e serve como bloco de construção para combustíveis e produtos químicos. Este artigo examina um dos catalisadores de trabalho que tornam essa conversão possível, observando seus átomos se rearranjarem em tempo real sob condições realistas para entender o que o mantém rápido, eficiente e duradouro.
O cavalo de batalha da produção de metanol
Por décadas, indústrias têm dependido de uma mistura de cobre, óxido de zinco e alumina para transformar misturas de hidrogênio e óxidos de carbono em metanol em escala massiva. Engenheiros sabem que o cobre realiza o principal trabalho químico, enquanto o zinco melhora dramaticamente o desempenho, mas exatamente como esses ingredientes cooperam nas minúsculas superfícies onde ocorrem as reações permanecia surpreendentemente elusivo. Métodos tradicionais por raios X fazem médias sobre bilhões de partículas, apagando as mudanças locais que ocorrem em nanopartículas individuais enquanto o catalisador é aquecido, resfriado e exposto a diferentes misturas gasosas.
Observando nanopartículas em ação
Os pesquisadores usaram microscopia eletrônica de transmissão operando, uma técnica que permite aquecer o catalisador industrial real em uma pequena célula preenchida com gás enquanto simultaneamente o imagina em escala nanométrica e monitora os produtos da reação. Partindo de um precursor oxidado, eles acompanharam como pequenos cristais de óxido de cobre e óxido de zinco emergem à medida que o material é ativado em hidrogênio, e então como o cobre é gradualmente reduzido à forma metálica. Ao mesmo tempo, espécies de zinco parcialmente reduzidas tornam‑se móveis e se espalham, formando uma fina camada que umedece as nanopartículas de cobre. Essa remodelação em escala nanométrica depende fortemente da temperatura e da composição do gás, e não pode ser capturada examinando o catalisador apenas antes ou depois da reação.
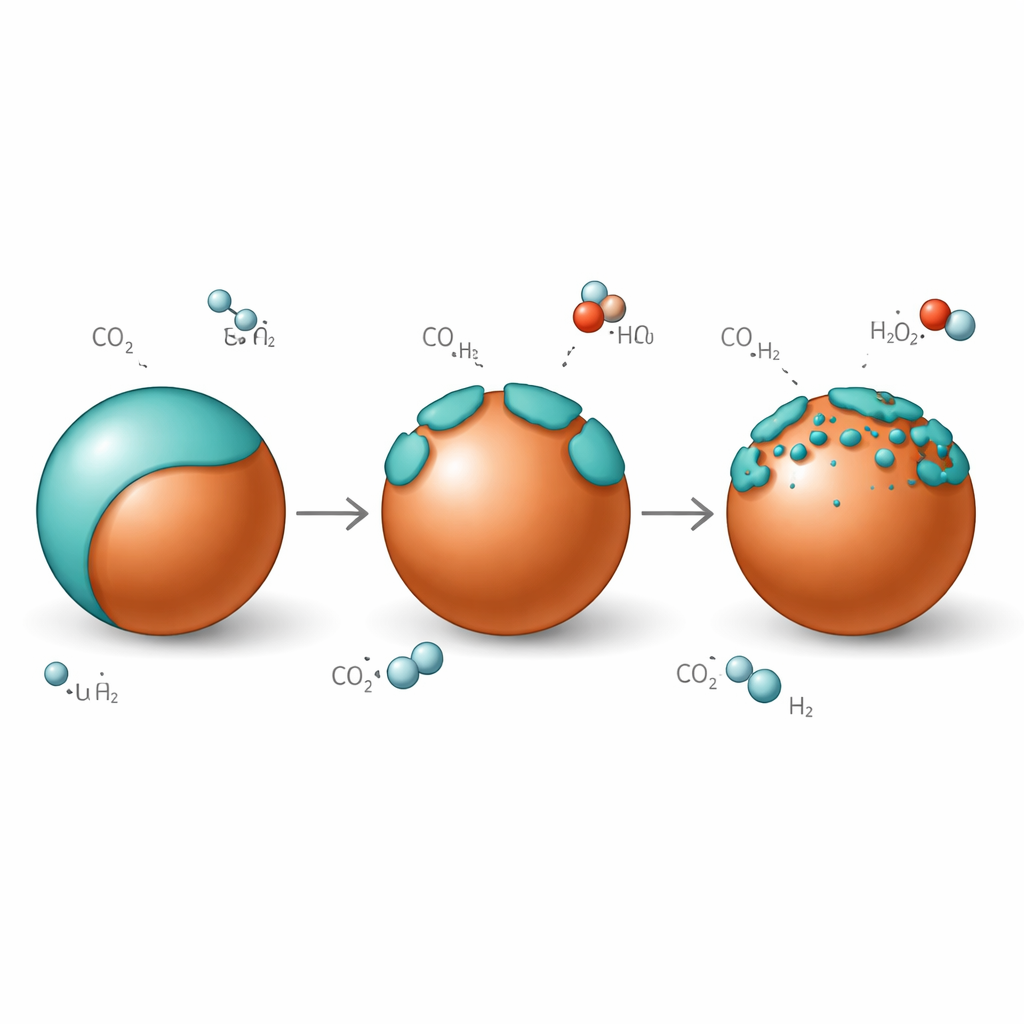
Uma pele respirante sobre o cobre
Sob condições de reação em que dióxido de carbono e hidrogênio fluem sobre o catalisador, a camada rica em zinco não permanece fixa. Em baixa temperatura, as partículas de cobre estão quase totalmente envolvidas por uma cobertura de óxido de zinco estilo grafítico. Quando a temperatura é elevada para a faixa de trabalho da síntese de metanol, essa cobertura "se abre": a pele contínua se fragmenta em ilhas, expondo bordas de cobre–óxido de zinco que são especialmente boas em ativar o dióxido de carbono. Quando o sistema é resfriado novamente, a cobertura fecha sobre o cobre com quase a mesma espessura, mostrando que essa molhabilidade é reversível e não um processo de degradação unidirecional. A espessura da concha rica em zinco também é ajustada pela quantidade de dióxido de carbono presente na alimentação gasosa, com mais CO2 promovendo uma cobertura mais espessa.
Uma troca delicada entre liga e óxido
Além da pele superficial, o zinco também pode se dissolver no cobre para formar uma liga cobre–zinco, outro estado considerado cataliticamente ativo. Ao acompanhar pequenas mudanças no espaçamento entre átomos de cobre por difração eletrônica enquanto mediam simultaneamente água e monóxido de carbono saindo do reator, a equipe descobriu que essa liga é transitória. Em temperaturas mais altas, a liga começa a se formar, expandindo ligeiramente a rede do cobre, mas à medida que água aparece pela reação reversa de deslocamento de água‑gás, o zinco é rapidamente reoxidado de volta a óxido de zinco na superfície. O catalisador, assim, shuttleia átomos de zinco entre estados metálicos e oxidados, criando um ciclo contínuo de formação de liga e crescimento e abertura da sobrecamada que depende sensivelmente do equilíbrio local entre hidrogênio, dióxido de carbono e água.
Por que essa dança em escala nanométrica importa
Para um observador leigo, a conclusão é que o catalisador funciona melhor não quando permanece em um único estado perfeitamente ordenado, mas quando oscila entre dois: liga de cobre–zinco e cobre revestido com óxido de zinco. As condições de reação continuam empurrando o sistema numa direção, enquanto a água que ele produz puxa de volta, criando uma espécie de transição de fase frustrada onde ambos os estados coexistem e se interconvertem. Esse equilíbrio dinâmico parece gerar e renovar os sítios de borda especiais que são altamente ativos para converter dióxido de carbono e hidrogênio em metanol. Com o tempo, parte do zinco móvel fica presa em formas cristalinas mais estáveis que não participam mais dessa dança, o que pode ajudar a explicar por que os catalisadores perdem atividade lentamente. Entender e controlar esse reagrupamento delicado pode orientar o projeto de materiais mais duradouros e eficientes para reciclar dióxido de carbono em produtos e combustíveis úteis.
Citação: Boniface, M., Götsch, T., Dong, J. et al. Dynamics of a Cu/ZnO/Al2O3 catalyst revealed by operando transmission electron microscopy during CO2 hydrogenation. Nat Catal 9, 404–413 (2026). https://doi.org/10.1038/s41929-026-01514-x
Palavras-chave: hidrogenação de CO2, síntese de metanol, catalisador de cobre e zinco, TEM operando, dinâmica do catalisador