Clear Sky Science · it
Dinámica di un catalizzatore Cu/ZnO/Al2O3 rivelata mediante microscopia elettronica a trasmissione operando durante l’idrogenazione della CO2
Trasformare un problema climatico in un liquido utile
Il biossido di carbonio è spesso visto soltanto come un gas di scarto che riscalda il pianeta, ma l’industria può anche convertirlo in metanolo, un liquido che immagazzina energia e funge da precursore per carburanti e prodotti chimici. Questo articolo dà uno sguardo all’interno di uno dei catalizzatori di punta che rende possibile questa conversione, osservando gli atomi che si riorganizzano in tempo reale sotto condizioni realistiche per capire cosa lo mantiene veloce, efficiente e duraturo.
Il cavallo da lavoro della produzione di metanolo
Per decenni, gli impianti si sono affidati a una miscela di rame, ossido di zinco e allumina per trasformare miscele di idrogeno e ossidi di carbonio in metanolo su scala massiccia. Gli ingegneri sanno che il rame svolge il lavoro chimico principale, mentre lo zinco ne potenzia notevolmente le prestazioni, ma il modo preciso in cui questi ingredienti cooperano sulle piccole superfici dove avvengono le reazioni è rimasto sorprendentemente sfuggente. I metodi tradizionali a raggi X mediamente osservano miliardi di particelle, sfocando i cambiamenti locali che si producono nei singoli nanoparticelle quando il catalizzatore viene riscaldato, raffreddato e esposto a diverse miscele gassose.
Osservare i nanoparticelle in azione
I ricercatori hanno utilizzato la microscopia elettronica a trasmissione operando, una tecnica che permette di riscaldare il catalizzatore industriale reale in una piccola cella riempita di gas mentre lo si osserva in nanoscalo e si monitorano simultaneamente i prodotti della reazione. Partendo da un precursore ossidato, hanno seguito come emergono piccoli cristalli di ossido di rame e ossido di zinco durante l’attivazione in idrogeno, e come il rame venga gradualmente ridotto a forma metallica. Allo stesso tempo, specie di zinco parzialmente ridotte diventano mobili e si diffondono, formando una sottile pelle che impregna le nanoparticelle di rame. Questa riorganizzazione a nanoscalo dipende fortemente dalla temperatura e dalla composizione del gas, e non può essere catturata esaminando il catalizzatore soltanto prima o dopo la reazione.
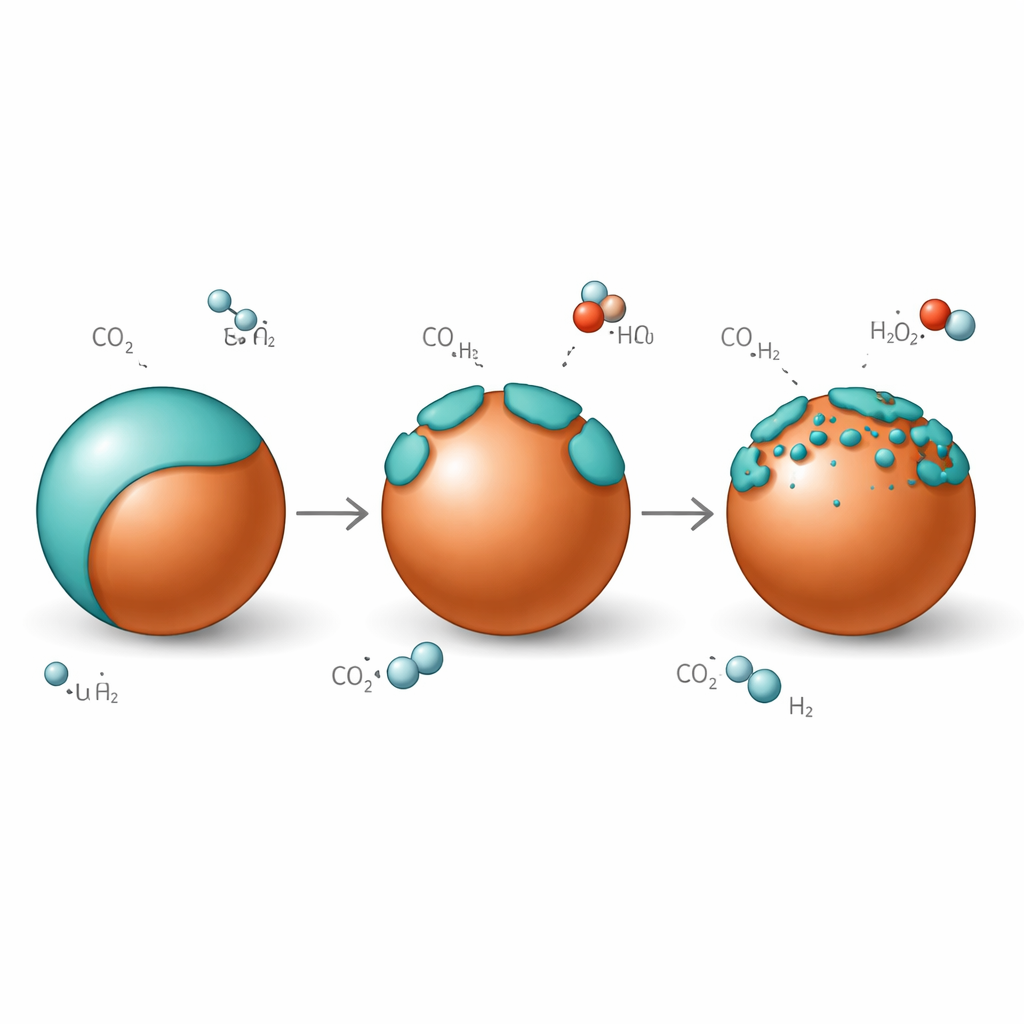
Una pelle che respira sul rame
Sotto le condizioni di reazione in cui biossido di carbonio e idrogeno scorrono sul catalizzatore, la pelle ricca di zinco non rimane fissa. A bassa temperatura, le particelle di rame sono quasi completamente avvolte da un sovrapposto strato di ossido di zinco grafitico. Quando la temperatura sale nell’intervallo operativo per la sintesi del metanolo, questo strato «si apre»: la copertura continua si frammenta in isole, esponendo bordi rame–ossido di zinco che sono particolarmente efficaci nell’attivare la CO2. Quando il sistema viene raffreddato, il sovrapposto si richiude sul rame con spessore quasi identico, mostrando che questo bagnamento è reversibile e non un processo degradativo unidirezionale. Lo spessore del guscio ricco di zinco è inoltre regolato dalla quantità di biossido di carbonio presente nel flusso gassoso: più CO2 porta a una copertura più spessa.
Un delicato scambio tra lega e ossido
Al di là della pelle superficiale, lo zinco può anche dissolversi nel rame per formare una lega rame‑zinco, un altro stato ritenuto cataliticamente attivo. Tracciando piccoli cambiamenti nella distanza tra atomi di rame tramite diffrazione elettronica mentre misuravano contemporaneamente acqua e monossido di carbonio che uscivano dal reattore, il gruppo ha scoperto che questa lega è transitoria. A temperature più elevate la lega inizia a formarsi, espandendo leggermente la reticolo del rame, ma quando compare l’acqua dalla reazione secondaria di scambio acqua‑gas inverso, lo zinco viene rapidamente riossidato a ossido di zinco in superficie. Il catalizzatore quindi shuttle‑a gli atomi di zinco avanti e indietro tra stati metallici e ossidati, creando un ciclo continuo di formazione della lega e crescita e apertura del sovrapposto che dipende in modo sensibile dal bilancio locale tra idrogeno, biossido di carbonio e acqua.
Perché questo ballo a nanoscalo è importante
Per un osservatore non esperto, la conclusione è che il catalizzatore funziona meglio non quando rimane in un unico stato perfettamente ordinato, ma quando oscilla tra due: la lega rame‑zinco e il rame ricoperto da ossido di zinco. Le condizioni di reazione spingono il sistema in una direzione, mentre l’acqua prodotta lo richiama indietro, creando una specie di transizione di fase frustrata in cui entrambi gli stati coesistono e si riconvertono. Questo equilibrio dinamico sembra generare e rinnovare i siti di bordo speciali che sono altamente attivi per convertire biossido di carbonio e idrogeno in metanolo. Col tempo, parte dello zinco mobile si blocca in forme cristalline più stabili che non partecipano più a questo ballo, il che può aiutare a spiegare perché i catalizzatori perdono lentamente attività. Comprendere e controllare questo delicato rimescolamento potrebbe guidare la progettazione di materiali più duraturi e più efficienti per riciclare la CO2 in prodotti e carburanti utili.
Citazione: Boniface, M., Götsch, T., Dong, J. et al. Dynamics of a Cu/ZnO/Al2O3 catalyst revealed by operando transmission electron microscopy during CO2 hydrogenation. Nat Catal 9, 404–413 (2026). https://doi.org/10.1038/s41929-026-01514-x
Parole chiave: idrogenazione della CO2, sintesi del metanolo, catalizzatore rame‑zinco, TEM operando, dynamica del catalizzatore