Clear Sky Science · fr
Dynamiques d’un catalyseur Cu/ZnO/Al2O3 révélées par microscopie électronique en transmission operando lors de l’hydrogénation du CO2
Transformer un problème climatique en liquide utile
Le dioxyde de carbone est souvent considéré uniquement comme un gaz résiduel qui réchauffe notre planète, mais l’industrie peut aussi le convertir en méthanol, un liquide qui stocke de l’énergie et sert de matière première pour des carburants et des produits chimiques. Cet article ouvre une fenêtre sur l’un des catalyseurs de base qui rendent cette conversion possible, observant ses atomes se réarranger en temps réel dans des conditions réalistes afin de comprendre ce qui le rend rapide, efficace et durable.
Le pilier de la production de méthanol
Depuis des décennies, les usines s’appuient sur un mélange de cuivre, d’oxyde de zinc et d’alumine pour transformer des mélanges d’hydrogène et d’oxydes de carbone en méthanol à grande échelle. Les ingénieurs savent que le cuivre effectue l’essentiel du travail chimique, tandis que le zinc améliore considérablement la performance, mais la manière exacte dont ces ingrédients coopèrent sur les petites surfaces où se déroulent les réactions reste étonnamment obscure. Les méthodes traditionnelles par rayons X moyennent l’information sur des milliards de particules, estompant les changements locaux qui affectent des nanoparticules individuelles lorsque le catalyseur est chauffé, refroidi et exposé à différents mélanges gazeux.
Observer des nanoparticules en action
Les chercheurs ont utilisé la microscopie électronique en transmission operando, une technique qui leur permet de chauffer le catalyseur industriel réel dans une petite cellule remplie de gaz tout en l’imageant au nanoscale et en surveillant les produits de la réaction. À partir d’un précurseur oxydé, ils ont suivi l’émergence de petits cristaux d’oxyde de cuivre et d’oxyde de zinc lors de l’activation en hydrogène, puis la réduction progressive du cuivre en forme métallique. Parallèlement, des espèces zinc partiellement réduites deviennent mobiles et se répandent, formant une fine peau qui mouille les nanoparticules de cuivre. Cette restructuration à l’échelle nanométrique dépend fortement de la température et de la composition du gaz, et ne peut pas être captée en examinant le catalyseur uniquement avant ou après la réaction.
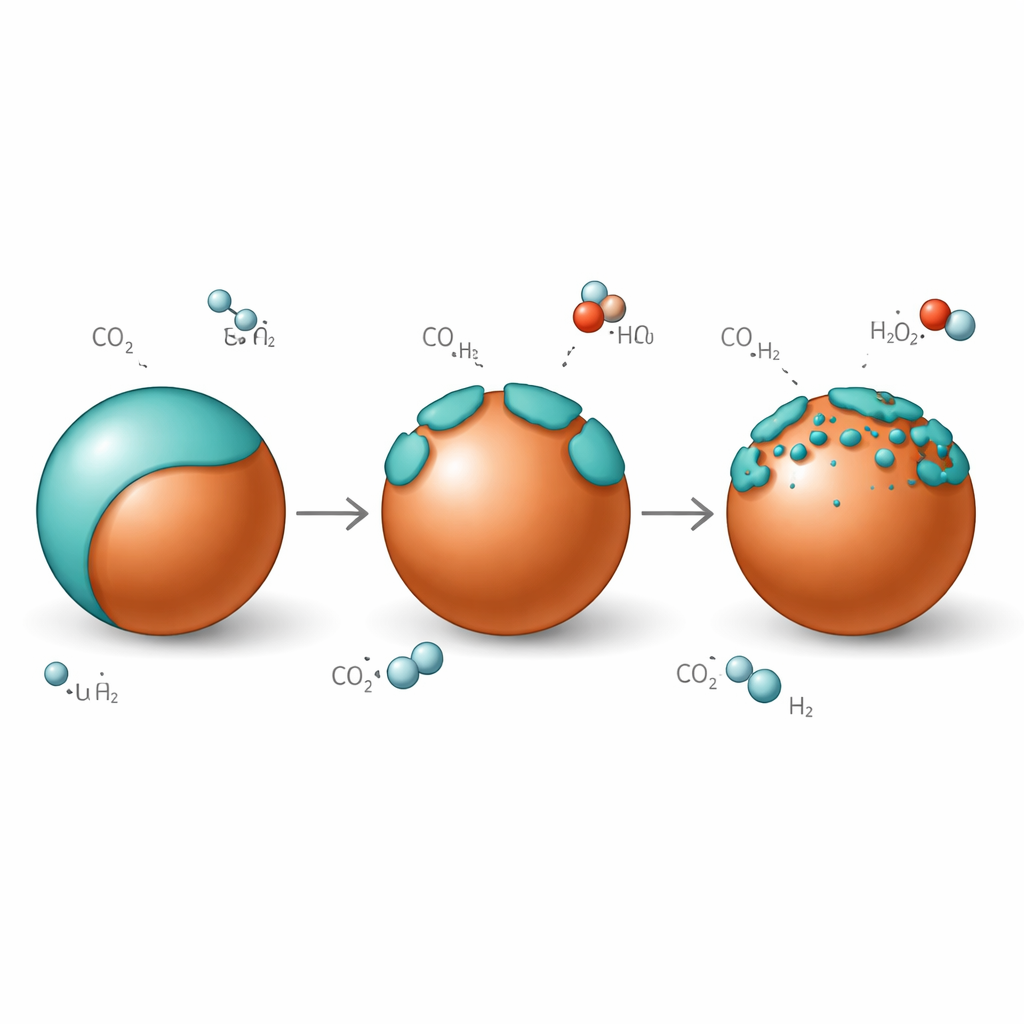
Une peau respirante sur le cuivre
Dans les conditions de réaction où du dioxyde de carbone et de l’hydrogène circulent sur le catalyseur, la peau riche en zinc ne reste pas figée. À basse température, les particules de cuivre sont presque entièrement enveloppées d’une couche d’oxyde de zinc graphitique. Lorsque la température monte dans la plage de travail de la synthèse du méthanol, cette surcouche « s’ouvre » : la peau continue se morcelle en îlots, exposant des bords cuivre–oxyde de zinc particulièrement efficaces pour activer le dioxyde de carbone. Lors du refroidissement, la surcouche se referme sur le cuivre avec presque la même épaisseur, montrant que ce mouillage est réversible et non une dégradation unidirectionnelle. L’épaisseur de la coquille riche en zinc est aussi modulée par la teneur en dioxyde de carbone du flux gazeux : davantage de CO2 entraîne une couverture plus épaisse.
Un délicat jeu entre alliage et oxyde
Au‑delà de la peau de surface, le zinc peut aussi se dissoudre dans le cuivre pour former un alliage cuivre–zinc, un autre état que l’on suppose catalytiquement actif. En suivant de minuscules variations de l’espacement entre atomes de cuivre via la diffraction électronique tout en mesurant simultanément l’eau et le monoxyde de carbone sortant du réacteur, l’équipe a découvert que cet alliage est transitoire. À des températures plus élevées l’alliage commence à se former, dilatant légèrement le réseau de cuivre, mais dès que de l’eau apparaît via la réaction de décalage inverse eau‑gaz‑carbonique, le zinc est rapidement réoxydé en oxyde de zinc à la surface. Le catalyseur fait ainsi commuter les atomes de zinc entre états métalliques et oxydés, créant un cycle continuel de formation d’alliage et de croissance puis ouverture de la surcouche, qui dépend finement de l’équilibre local entre hydrogène, dioxyde de carbone et eau.
Pourquoi cette danse nanométrique compte
Pour un observateur non spécialiste, la conclusion est que le catalyseur fonctionne mieux non pas quand il reste dans un seul état parfaitement ordonné, mais lorsqu’il oscille entre deux : l’alliage cuivre–zinc et le cuivre recouvert d’oxyde de zinc. Les conditions de réaction poussent le système dans un sens, tandis que l’eau produite le ramène, créant une sorte de transition de phase frustrée où les deux états coexistent et s’interconvertissent. Cet équilibre dynamique semble générer et renouveler des sites de bords particuliers, très actifs pour convertir le dioxyde de carbone et l’hydrogène en méthanol. Avec le temps, une partie du zinc mobile se fixe dans des formes cristallines plus stables qui ne participent plus à cette danse, ce qui pourrait expliquer la perte progressive d’activité des catalyseurs. Comprendre et contrôler ce réarrangement délicat pourrait guider la conception de matériaux plus durables et plus efficaces pour recycler le dioxyde de carbone en produits et carburants utiles.
Citation: Boniface, M., Götsch, T., Dong, J. et al. Dynamics of a Cu/ZnO/Al2O3 catalyst revealed by operando transmission electron microscopy during CO2 hydrogenation. Nat Catal 9, 404–413 (2026). https://doi.org/10.1038/s41929-026-01514-x
Mots-clés: hydrogénation du CO2, synthèse du méthanol, catalyseur cuivre‑zinc, TEM operando, dynamique des catalyseurs