Clear Sky Science · de
Dynamik eines Cu/ZnO/Al2O3‑Katalysators aufgezeigt durch operando‑Transmissionselektronenmikroskopie während der CO2‑Hydrierung
Aus einem Klimaproblem ein nützliches Flüssigprodukt machen
Kohlendioxid wird oft nur als Abgas gesehen, das unseren Planeten erwärmt. Die Industrie kann es jedoch auch in Methanol umwandeln — eine Flüssigkeit, die Energie speichert und als Baustein für Brennstoffe und Chemikalien dient. Dieser Artikel gewährt Einblicke in einen der Arbeitspferd‑Katalysatoren, der diese Umwandlung möglich macht, und verfolgt in Echtzeit unter realistischen Bedingungen, wie sich seine Atome neu ordnen, um zu verstehen, was ihn schnell, effizient und langlebig hält.
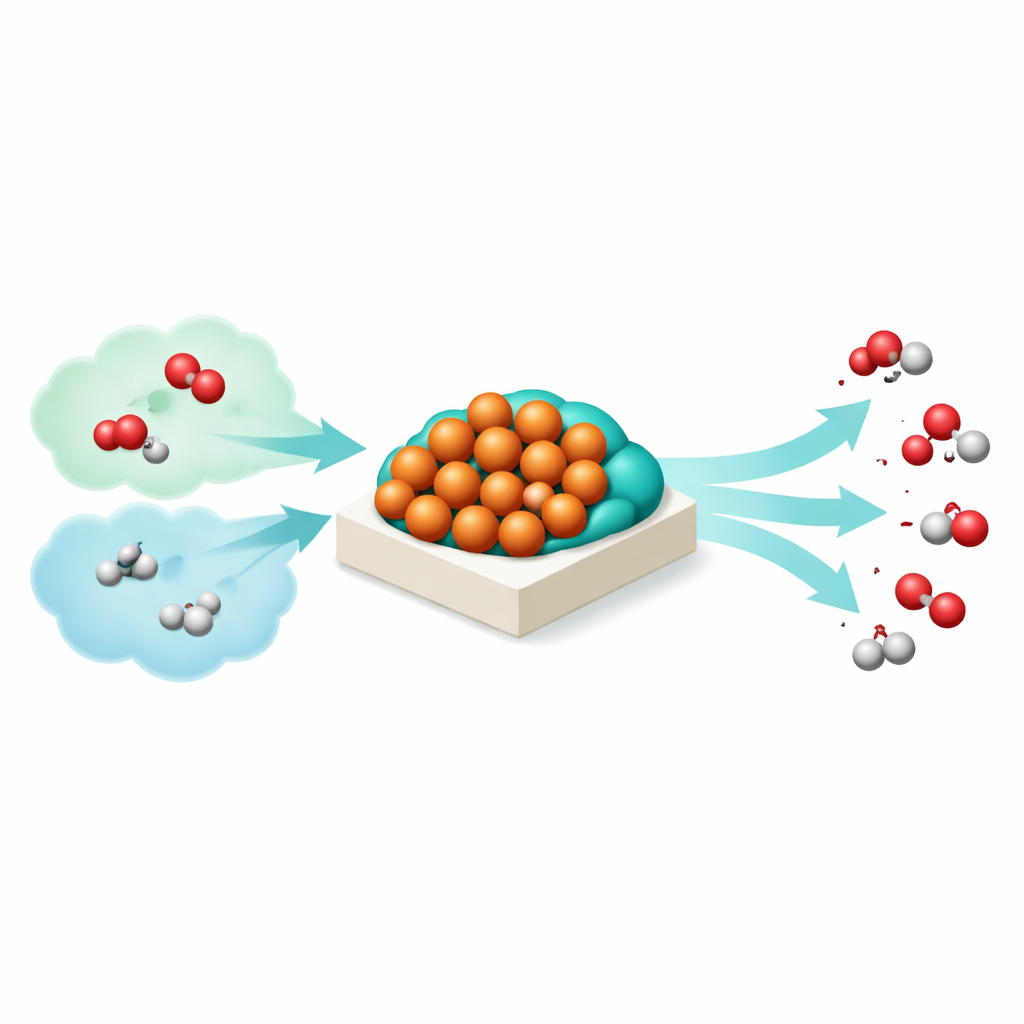
Das Arbeitspferd der Methanolproduktion
Seit Jahrzehnten setzen Fabriken eine Mischung aus Kupfer, Zinkoxid und Aluminiumoxid ein, um Wasserstoff‑ und Kohlenoxidemischungen großtechnisch in Methanol zu überführen. Ingenieure wissen, dass Kupfer die hauptsächliche chemische Arbeit leistet, während Zink die Leistung drastisch steigert. Wie genau diese Bestandteile jedoch auf den winzigen Reaktionsflächen zusammenwirken, blieb überraschend schwer fassbar. Traditionelle Röntgenmethoden mitteln über Milliarden von Partikeln und verwischen die lokalen Veränderungen, die an einzelnen Nanopartikeln auftreten, wenn der Katalysator erhitzt, abgekühlt und unterschiedlichen Gasgemischen ausgesetzt wird.
Nanopartikel bei der Arbeit beobachten
Die Forschenden nutzten operando‑Transmissionselektronenmikroskopie, eine Methode, mit der sie den realen industriellen Katalysator in einer winzigen gasgefüllten Zelle erhitzen und gleichzeitig nanoskalig abbilden sowie die Reaktionsprodukte überwachen können. Ausgehend von einem oxidierten Präparat verfolgten sie, wie sich kleine Kupfer‑ und Zinkoxidkristalle beim Aktivieren in Wasserstoff bilden und wie Kupfer allmählich zu metallischer Form reduziert wird. Gleichzeitig werden teilweise reduzierte Zinkarten mobil und verteilen sich, sodass sie eine dünne Haut bilden, die die Kupfernanopartikel benetzt. Diese nanoskalige Umgestaltung hängt stark von Temperatur und Gaszusammensetzung ab und lässt sich nicht erfassen, wenn man den Katalysator nur vor oder nach der Reaktion untersucht.
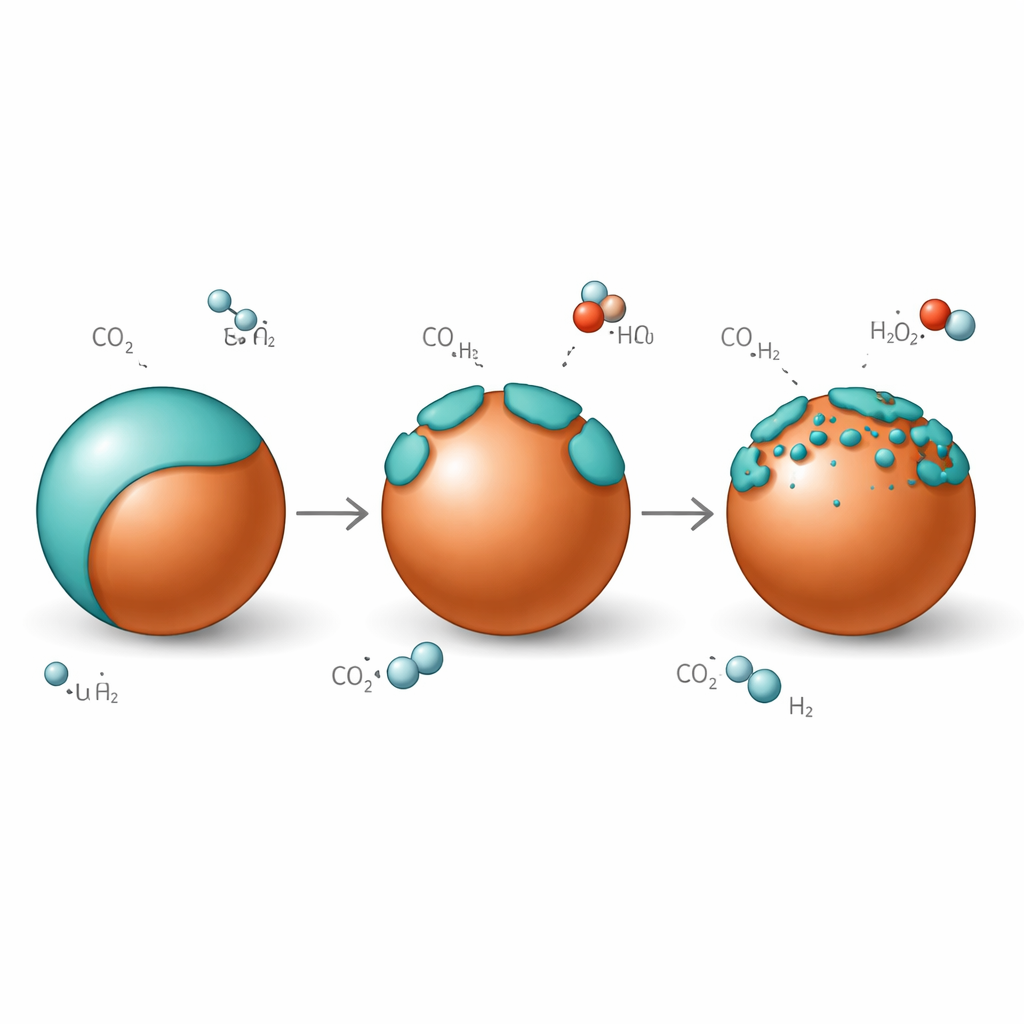
Eine atmende Haut auf Kupfer
Unter Reaktionsbedingungen, bei denen Kohlendioxid und Wasserstoff über den Katalysator strömen, bleibt die zinkreiche Haut nicht starr. Bei niedrigen Temperaturen sind Kupferpartikel fast vollständig von einer graphitähnlichen Zinkoxid‑Überlagerung umhüllt. Steigt die Temperatur in den Arbeitsbereich der Methanolsynthese, „öffnet“ sich diese Überlagerung: Die durchgehende Haut zerbricht in Inseln und legt Kupfer–Zinkoxid‑Kanten frei, die besonders gut darin sind, Kohlendioxid zu aktivieren. Beim erneuten Abkühlen schließt sich die Überlagerung mit nahezu gleicher Dicke wieder über dem Kupfer, was zeigt, dass diese Benetzung reversibel ist und keine einseitige Degradation darstellt. Die Dicke der zinkreichen Schale wird außerdem durch den Kohlendioxidanteil im Gasstrom gesteuert — mehr CO2 fördert eine dichtere Bedeckung.
Ein empfindliches Wechselspiel zwischen Legierung und Oxid
Jenseits der Oberflächenhaut kann Zink auch in Kupfer gelöst werden und eine Kupfer‑Zink‑Legierung bilden, einen weiteren Zustand, dem katalytische Aktivität zugeschrieben wird. Indem das Team winzige Änderungen der Kupfer‑Atomabstände mittels Elektronenbeugung verfolgte, während gleichzeitig Wasser und Kohlenmonoxid aus dem Reaktor gemessen wurden, fand es heraus, dass diese Legierung nur transient ist. Bei höheren Temperaturen beginnt sich die Legierung zu bilden und dehnt das Kupfergitter leicht aus, doch sobald aus der Gegenreaktion der Wassergasverschiebung Wasser entsteht, wird Zink an der Oberfläche rasch wieder zu Zinkoxid re‑oxidiert. Der Katalysator schaufelt somit Zinkatome zwischen metallischem und oxidiertem Zustand hin und her und schafft einen ständigen Zyklus aus Legierungsbildung sowie Überlagerungswachstum und ‑öffnung, der empfindlich vom lokalen Gleichgewicht aus Wasserstoff, Kohlendioxid und Wasser abhängt.
Warum dieser nanoskalige Tanz wichtig ist
Für eine nichtfachliche Beobachterin folgt die Schlussfolgerung, dass der Katalysator am besten arbeitet, wenn er nicht in einem einzigen, perfekt geordneten Zustand verharrt, sondern zwischen zwei Zuständen schwebt: Kupfer‑Zink‑Legierung und Kupfer mit einer Zinkoxid‑Beschichtung. Die Reaktionsbedingungen treiben das System in die eine Richtung, während das produzierte Wasser es zurückzieht und so eine Art frustrierte Phasenumwandlung erzeugt, in der beide Zustände koexistieren und ineinander übergehen. Dieses dynamische Gleichgewicht scheint die speziellen Kantenstellen zu erzeugen und zu erneuern, die besonders aktiv dafür sind, Kohlendioxid und Wasserstoff in Methanol umzusetzen. Mit der Zeit sperrt sich ein Teil des mobilen Zinks in stabilere kristalline Formen ein, die nicht mehr an diesem Tanz teilnehmen, was erklären könnte, warum Katalysatoren allmählich an Aktivität verlieren. Das Verständnis und die Kontrolle dieses feinen Umsortierens könnte die Entwicklung langlebigerer und effizienterer Materialien zum Recycling von Kohlendioxid in nützliche Produkte und Brennstoffe leiten.
Zitation: Boniface, M., Götsch, T., Dong, J. et al. Dynamics of a Cu/ZnO/Al2O3 catalyst revealed by operando transmission electron microscopy during CO2 hydrogenation. Nat Catal 9, 404–413 (2026). https://doi.org/10.1038/s41929-026-01514-x
Schlüsselwörter: CO2‑Hydrierung, Methanolsynthese, Kupfer‑Zink‑Katalysator, operando‑TEM, Katalysatordynamik