Clear Sky Science · pl
Dynamika katalizatora Cu/ZnO/Al2O3 ujawniona dzięki operando transmisyjnej mikroskopii elektronowej podczas hydrogenizacji CO2
Przekształcanie problemu klimatycznego w użyteczny płyn
Tlenek węgla(IV) bywa postrzegany głównie jako gaz odpadowy ocieplający planetę, lecz przemysł potrafi też przekształcić go w metanol — ciecz magazynującą energię i służącą jako budulec paliw i chemikaliów. Ten artykuł zagląda do jednego z kluczowych katalizatorów umożliwiających tę konwersję, obserwując w czasie rzeczywistym przestawianie się atomów w realistycznych warunkach, by zrozumieć, co utrzymuje go szybkim, wydajnym i trwałym.
Koń roboczy produkcji metanolu
Przez dekady zakłady przemysłowe polegały na mieszance miedzi, tlenku cynku i tlenku glinu, by przekształcać mieszaniny wodoru i tlenków węgla w metanol na wielką skalę. Inżynierowie wiedzą, że miedź wykonuje główną pracę chemiczną, podczas gdy cynk znacznie poprawia wydajność, ale to, jak te składniki współpracują na mikroskopijnych powierzchniach, gdzie zachodzą reakcje, pozostawało zaskakująco nieuchwytne. Tradycyjne metody rentgenowskie uśredniają sygnał po miliardach cząstek, zacierając lokalne zmiany występujące na pojedynczych nanocząstkach w miarę, jak katalizator jest ogrzewany, chłodzony i eksponowany na różne mieszaniny gazów.
Obserwacja nanocząstek w akcji
Naukowcy użyli operando transmisyjnej mikroskopii elektronowej, techniki pozwalającej ogrzewać rzeczywisty katalizator przemysłowy w maleńkiej, wypełnionej gazem komórce, jednocześnie obrazując go w skali nanometrów i monitorując produkty reakcji. Wyjściowo z utlenionego prekursoru śledzili, jak pojawiają się malutkie kryształy tlenku miedzi i tlenku cynku podczas aktywacji w wodorze, a następnie jak miedź stopniowo redukuje się do postaci metalicznej. Równocześnie częściowo zredukowane gatunki cynku stają się ruchome i rozprzestrzeniają się, tworząc cienką powłokę zwilżającą nanocząstki miedzi. To nanoskalowe przekształcanie silnie zależy od temperatury i składu gazu i nie da się go uchwycić, badając katalizator wyłącznie przed reakcją lub po niej.
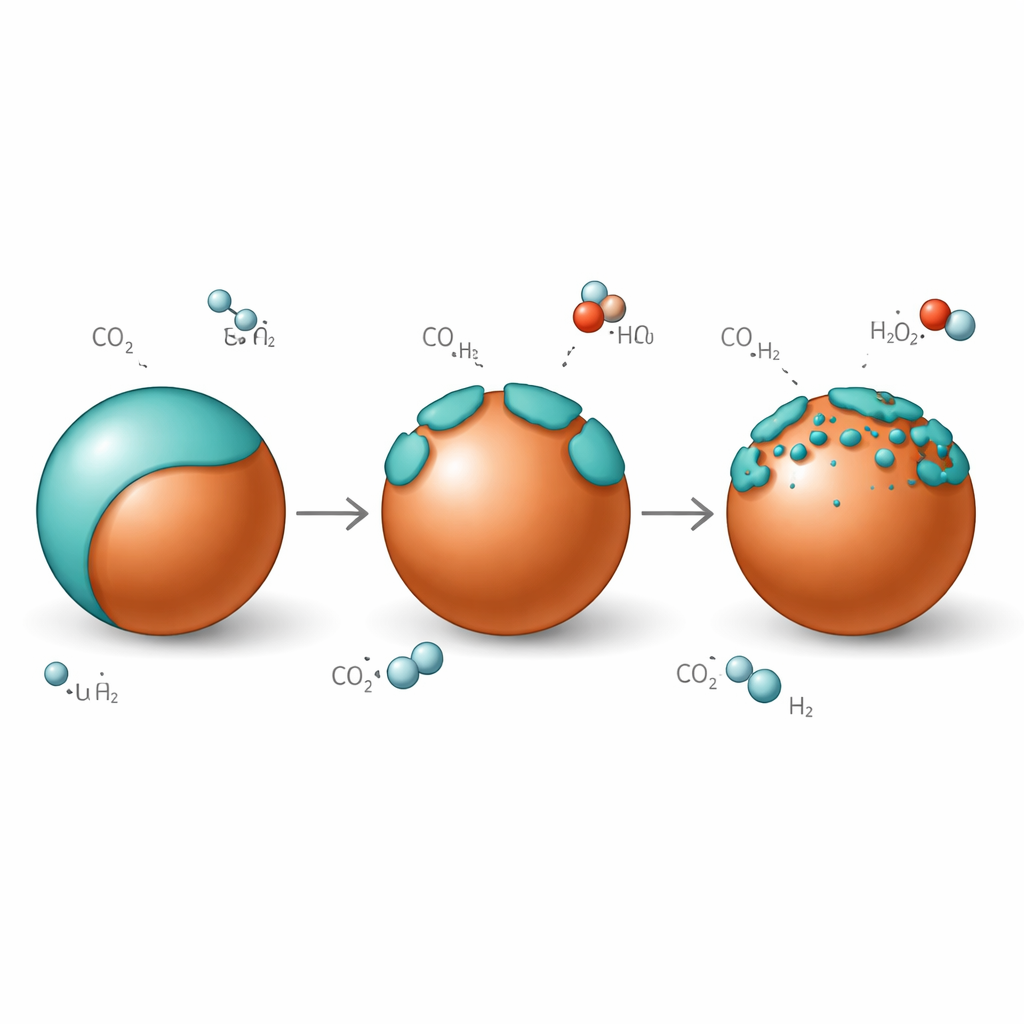
Oddychająca skóra na miedzi
W warunkach reakcyjnych, gdy nad katalizatorem przepływają tlenek węgla(IV) i wodór, bogata w cynk powłoka nie pozostaje nieruchoma. W niskiej temperaturze cząstki miedzi są niemal całkowicie owinięte grafitopodobną warstwą tlenku cynku. Po podniesieniu temperatury do zakresu pracy syntezy metanolu ta powłoka „otwiera się”: ciągła skóra rozpada się na wyspy, odsłaniając krawędzie miedź–tlenek cynku, które są szczególnie dobre w aktywowaniu CO2. Po ponownym ochłodzeniu powłoka zamyka się z powrotem nad miedzią z niemal tą samą grubością, co pokazuje, że to zwilżanie jest odwracalne, a nie jednokierunkową degradacją. Grubość skorupy bogatej w cynk jest też modulowana przez zawartość CO2 w zasilaniu gazowym — więcej CO2 sprzyja grubszemu pokryciu.
Delikatne przejścia między stopem a tlenkiem
Powyżej powierzchniowej powłoki cynk może także rozpuszczać się w miedzi, tworząc stop miedź–cynk, inny stan uznawany za aktywny katalitycznie. Śledząc drobne zmiany w odległościach między atomami miedzi za pomocą dyfrakcji elektronów, równocześnie mierząc wydzielającą się wodę i tlenek węgla, zespół odkrył, że ten stop jest przejściowy. W wyższych temperaturach stop zaczyna się tworzyć, nieco rozszerzając sieć miedzi, ale gdy z reakcji bocznej odwrotnego przejścia wodnego-gazowego pojawia się woda, cynk szybko ponownie utlenia się do tlenku cynku na powierzchni. Katalizator zatem przemieszcza atomy cynku tam i z powrotem między stanami metalicznymi i utlenionymi, tworząc ciągły cykl formowania stopu oraz wzrostu i otwierania powłoki, zależny wrażliwie od lokalnej równowagi wodoru, CO2 i wody.
Dlaczego ten nanoskalowy taniec ma znaczenie
Dla obserwatora niezaawansowanego wniosek jest taki, że katalizator działa najlepiej nie wtedy, gdy znajduje się w jednym, perfekcyjnie uporządkowanym stanie, lecz gdy oscyluje między dwoma: stopem miedź–cynk a miedzią pokrytą tlenkiem cynku. Warunki reakcyjne ciągle przesuwają system w jedną stronę, podczas gdy powstająca woda odciąga go z powrotem, tworząc rodzaj sfrustrowanego przejścia fazowego, w którym oba stany współistnieją i wzajemnie się przekształcają. Ta dynamiczna równowaga wydaje się generować i odnawiać specjalne miejsca krawędziowe, wyjątkowo aktywne w przekształcaniu CO2 i H2 w metanol. Z czasem część ruchomego cynku zamarza w bardziej stabilnych formach krystalicznych, które już nie biorą udziału w tym tańcu, co może tłumaczyć stopniowy spadek aktywności katalizatorów. Zrozumienie i kontrola tego delikatnego przetasowania może pokierować projektowaniem trwalszych, bardziej wydajnych materiałów do recyklingu CO2 w użyteczne produkty i paliwa.
Cytowanie: Boniface, M., Götsch, T., Dong, J. et al. Dynamics of a Cu/ZnO/Al2O3 catalyst revealed by operando transmission electron microscopy during CO2 hydrogenation. Nat Catal 9, 404–413 (2026). https://doi.org/10.1038/s41929-026-01514-x
Słowa kluczowe: hydrogenizacja CO2, synteza metanolu, katalizator miedź-cynk, operando TEM, dynamika katalizatora