Clear Sky Science · es
Dinámica de un catalizador Cu/ZnO/Al2O3 revelada mediante microscopía electrónica de transmisión operando durante la hidrogenación de CO2
Convertir un problema climático en un líquido útil
El dióxido de carbono suele considerarse únicamente un gas residual que calienta nuestro planeta, pero la industria también puede convertirlo en metanol, un líquido que almacena energía y sirve como bloque de construcción para combustibles y productos químicos. Este artículo se asoma al interior de uno de los catalizadores fundamentales que hacen posible esta conversión, observando cómo sus átomos se reorganizan en tiempo real bajo condiciones realistas para entender qué lo mantiene rápido, eficiente y duradero.
El caballo de batalla de la producción de metanol
Durante décadas, las plantas han confiado en una mezcla de cobre, óxido de zinc y alúmina para convertir mezclas de hidrógeno y óxidos de carbono en metanol a gran escala. Los ingenieros saben que el cobre realiza la mayor parte del trabajo químico, mientras que el zinc mejora el rendimiento de forma dramática, pero cómo cooperan exactamente estos ingredientes en las diminutas superficies donde ocurren las reacciones ha sido sorprendentemente esquivo. Los métodos tradicionales de rayos X promedian sobre miles de millones de partículas, difuminando los cambios locales que ocurren en nanopartículas individuales cuando el catalizador se calienta, enfría y se expone a diferentes mezclas de gases.
Observando nanopartículas en acción
Los investigadores utilizaron microscopía electrónica de transmisión operando, una técnica que les permite calentar el catalizador industrial real en una pequeña celda llena de gas mientras lo imagen a escala nanométrica y, al mismo tiempo, monitorizan los productos de la reacción. Partiendo de un precursor oxidado, siguieron cómo emergen pequeños cristales de óxido de cobre y óxido de zinc mientras el material se activa en hidrógeno, y cómo el cobre se reduce gradualmente a su forma metálica. Al mismo tiempo, especies de zinc parcialmente reducidas se vuelven móviles y se extienden, formando una fina capa que moja las nanopartículas de cobre. Este remodelado a escala nanométrica depende fuertemente de la temperatura y de la composición del gas, y no puede capturarse examinando el catalizador solo antes o después de la reacción.
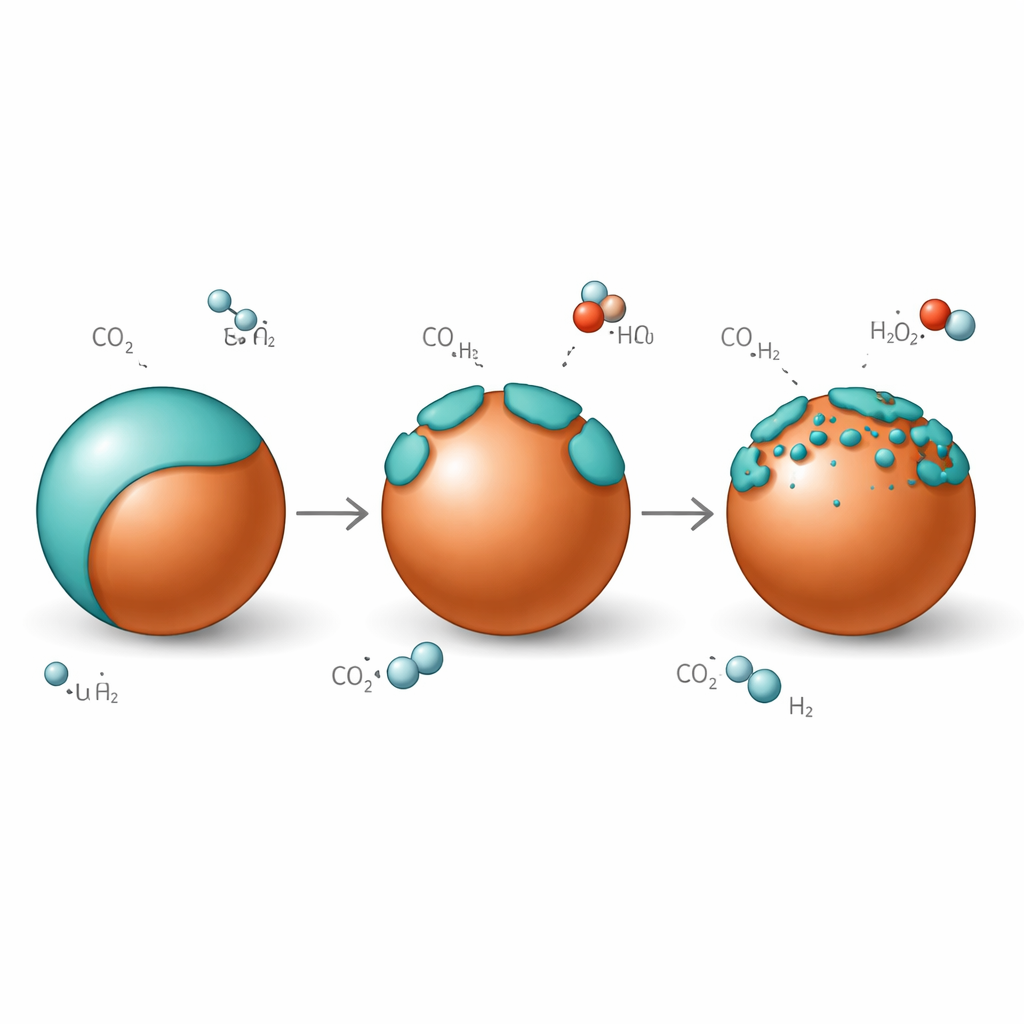
Una piel que respira sobre el cobre
Bajo las condiciones de reacción en las que dióxido de carbono e hidrógeno fluyen sobre el catalizador, la piel rica en zinc no permanece fija. A baja temperatura, las partículas de cobre están casi completamente envueltas por una sobrecapa graphítica de óxido de zinc. Cuando la temperatura se eleva hasta el rango de trabajo para la síntesis de metanol, esta sobrecapa se "abre": la piel continua se fragmenta en islas, exponiendo bordes cobre–óxido de zinc que son especialmente eficaces para activar el dióxido de carbono. Al enfriarse de nuevo, la sobrecapa vuelve a cerrarse sobre el cobre con casi el mismo espesor, lo que muestra que este mojado es reversible en lugar de ser un proceso de degradación irreversible. El grosor de la concha rica en zinc también se ajusta según la cantidad de dióxido de carbono presente en la corriente de gas, siendo una mayor concentración de CO2 la que induce una cobertura más gruesa.
Un delicado intercambio entre aleación y óxido
Más allá de la piel superficial, el zinc también puede disolverse en el cobre para formar una aleación cobre–zinc, otro estado que se cree catalíticamente activo. Al seguir pequeños cambios en el espaciamiento entre átomos de cobre mediante difracción electrónica mientras medían simultáneamente el agua y el monóxido de carbono que salen del reactor, el equipo descubrió que esta aleación es transitoria. A temperaturas más altas la aleación comienza a formarse, expandiendo ligeramente la red del cobre, pero cuando aparece agua por la reacción secundaria de desplazamiento de gas reversible, el zinc se reoxida rápidamente a óxido de zinc en la superficie. El catalizador, por tanto, traslada átomos de zinc continuamente entre estados metálicos y oxidados, creando un ciclo continuo de formación de aleación y crecimiento y apertura de la sobrecapa que depende de forma sensible del equilibrio local entre hidrógeno, dióxido de carbono y agua.
Por qué importa esta danza a escala nanométrica
Para un observador no especializado, la conclusión es que el catalizador funciona mejor no cuando permanece en un único estado perfectamente ordenado, sino cuando oscila entre dos: la aleación cobre–zinc y el cobre recubierto de óxido de zinc. Las condiciones de reacción empujan el sistema en una dirección, mientras que el agua que produce lo atrae de vuelta, creando una especie de transición de fase frustrada donde ambos estados coexisten e interconvierten. Este equilibrio dinámico parece generar y renovar los sitios de borde especiales que son muy activos para convertir dióxido de carbono e hidrógeno en metanol. Con el tiempo, parte del zinc móvil se fija en formas cristalinas más estables que ya no participan en esta danza, lo que puede ayudar a explicar por qué los catalizadores pierden actividad de forma gradual. Entender y controlar este delicado reordenamiento podría orientar el diseño de materiales más duraderos y eficientes para reciclar dióxido de carbono en productos y combustibles útiles.
Cita: Boniface, M., Götsch, T., Dong, J. et al. Dynamics of a Cu/ZnO/Al2O3 catalyst revealed by operando transmission electron microscopy during CO2 hydrogenation. Nat Catal 9, 404–413 (2026). https://doi.org/10.1038/s41929-026-01514-x
Palabras clave: hidrogenación de CO2, síntesis de metanol, catálisis cobre-zinc, TEM operando, dinámica del catalizador