Clear Sky Science · pt
Deficiência de 2’-5’ Oligoadenilato Synthetase-Like 1 (OASL1) em camundongos promove proteção antiviral contra infecção por vírus da pseudorábia associada ao aumento da produção de interferon tipo I
Por que isso importa para pessoas e animais
O vírus da pseudorábia pode soar como uma curiosidade da vida no campo, mas é um grande causador de morte em leitões, uma ameaça à indústria global de suínos e uma causa ocasional de infecções cerebrais graves em pessoas. Este estudo revela como uma das próprias proteínas "freio" do organismo, chamada OASL1, pode tornar esse vírus mais perigoso ao suprimir as defesas antivirais precoces. Ao remover esse freio em camundongos, os autores mostram que é possível melhorar dramaticamente a sobrevivência, reduzir danos cerebrais e diminuir os níveis virais, oferecendo pistas para tratamentos e vacinas melhores contra o vírus da pseudorábia e herpesvírus relacionados.
Um vírus resistente e de amplo alcance
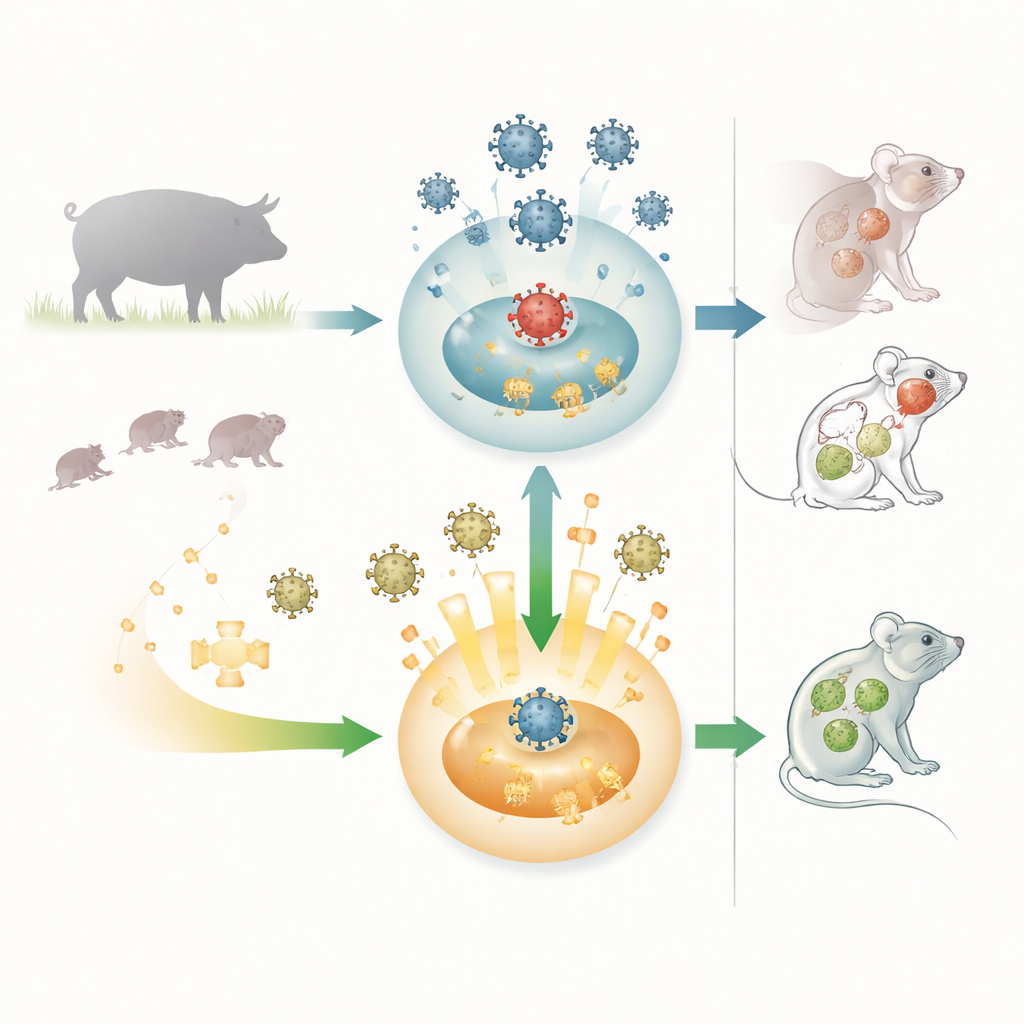
O vírus da pseudorábia é um herpesvírus cuja morada natural são os porcos, onde pode causar problemas respiratórios, falhas reprodutivas e morte quase certa em leitões recém‑nascidos. O vírus também pode infectar muitos outros mamíferos, incluindo animais de fazenda, animais de estimação e camundongos de laboratório, e quase todos esses hospedeiros acidentais morrem. Relatos recentes de infecções cerebrais humanas ligadas a variantes do vírus da pseudorábia levantaram preocupação de que esse patógeno animal possa ocasionalmente saltar para pessoas. Por causa desse amplo espectro de hospedeiros e da gravidade da doença, os pesquisadores querem entender como a primeira linha de defesa do corpo, o sistema imune inato, combate esse vírus — e como o vírus contra‑ataca.
O sistema de alarme do corpo e um freio interno
Quando um vírus de DNA como o da pseudorábia entra nas células, sensores especializados detectam o material genético viral e desencadeiam a produção de interferons do tipo I, uma família de potentes moléculas antivirais de alarme. Esses interferons ativam centenas de genes de defesa. Entre eles está o OASL1, uma proteína que não destrói vírus diretamente, mas ajusta a resposta. Trabalhos anteriores mostraram que OASL1 pode controlar a produção de IRF7, um interruptor chave para a produção de interferon, formando um circuito de retroalimentação negativa que evita que o sistema de alarme permaneça ligado por tempo demais. A questão central deste estudo foi o que acontece durante a infecção por pseudorábia se esse freio, OASL1, for removido.
Remover o freio protege os camundongos
Os pesquisadores compararam camundongos normais com camundongos geneticamente modificados para não expressar OASL1. Ambos os grupos receberam uma dose de vírus da pseudorábia que é normalmente letal. Todos os camundongos normais desenvolveram coceira intensa, feridas na pele, convulsões e paralisia, e todos morreram. Em contraste marcante, a maioria dos camundongos deficientes em OASL1 sobreviveu e manteve o peso corporal com sintomas muito mais leves. Quando a equipe mediu os níveis virais no baço, pulmões e cérebro, constatou que os camundongos sem OASL1 tinham cargas virais muito mais baixas. Exames de sangue mostraram que esses camundongos produziram maiores quantidades de interferons tipo I precocemente na infecção, sugerindo que uma resposta de alarme mais forte e mais rápida ajudou a controlar o vírus antes que ele se espalhasse amplamente.
Menos inflamação descontrolada, menos dano aos órgãos
Infecções virais graves podem desencadear uma "tempestade de citocinas", uma reação inflamatória avassaladora que danifica órgãos. Os cientistas mediram várias moléculas inflamatórias chave em tecidos e sangue. Camundongos normais infectados com o vírus da pseudorábia apresentaram altos níveis desses fatores no baço, pulmões e cérebro, juntamente com intensa infiltração de células inflamatórias. Em contraste, camundongos deficientes em OASL1 tiveram níveis muito mais baixos desses sinais inflamatórios. Ao microscópio, seus baços mantiveram células imunes em vez de perdê‑las por morte celular, seus pulmões exibiram alterações inflamatórias mais leves e seus cérebros mostraram muito menos degeneração de neurônios no hipocampo, uma região crítica para a memória. Assim, remover OASL1 não apenas ajudou a eliminar o vírus, mas também evitou inflamação excessiva e lesão tecidual.
Aproximando‑se do interruptor de controle chave
Para entender como OASL1 modela essa resposta, a equipe examinou IRF7, o interruptor que impulsiona a produção de interferon. Em camundongos sem OASL1, os níveis de IRF7 foram consistentemente mais altos no baço, pulmones, cérebro e em células imunes cultivadas, como macrófagos e microglia após a infecção, enquanto um fator relacionado, IRF3, mudou pouco. Essas células secretaram mais interferons tipo I e suportaram menos replicação viral. Quando os pesquisadores usaram RNA de interferência pequeno para reduzir especificamente IRF7 em macrófagos deficientes em OASL1, a resposta aumentada de interferon desapareceu e os níveis virais retornaram. Esse experimento mostrou que o efeito protetor da perda de OASL1 depende principalmente de liberar IRF7 para ativar plenamente o programa antiviral.
O que isso significa para o futuro
Em termos simples, OASL1 age como um freio de segurança interno que impede que o alarme antiviral toque por tempo demais. Durante a infecção pelo vírus da pseudorábia, esse freio entra em ação cedo e com força demais, dando espaço para o vírus se multiplicar e contribuindo para a gravidade da doença. Camundongos que não têm OASL1, ou cuja OASL1 é temporariamente silenciada em células imunes chave, montam uma resposta rápida de interferon dirigida por IRF7 que elimina o vírus de forma mais eficaz ao mesmo tempo em que evita uma tempestade de citocinas danosa. Essas descobertas sugerem que medicamentos administrados no momento certo que afrouxem esse freio — apenas durante a janela precoce crítica da infecção — poderiam ajudar a proteger porcos e possivelmente humanos contra a pseudorábia e herpesvírus relacionados. Qualquer terapia desse tipo precisaria, no entanto, ser finamente ajustada para evitar oscilar entre resposta imune insuficiente e excessiva.
Citação: Bao, T.H.T.N., Leya, M., Van, T.P. et al. 2’-5’ Oligoadenylate Synthetase-Like 1- (OASL1-) deficient mice promote antiviral protection against pseudorabies virus infection associated with enhanced production of type I interferon. Sci Rep 16, 13205 (2026). https://doi.org/10.1038/s41598-026-43144-0
Palavras-chave: vírus da pseudorábia, imunidade inata, interferon tipo I, OASL1, IRF7