Clear Sky Science · fr
Les souris déficientes en 2’-5’ oligoadénylate synthétase‑like 1 (OASL1-) favorisent la protection antivirale contre l’infection par le virus de la pseudoyeux associée à une production accrue d’interférons de type I
Pourquoi cela compte pour les humains et les animaux
Le virus de la pseudoyeux peut sembler une curiosité de la vie agricole, mais c’est un tueur majeur de porcelets, une menace pour l’industrie mondiale du porc et une cause occasionnelle d’infections cérébrales sévères chez l’homme. Cette étude révèle comment l’une des protéines « freins » de l’organisme, appelée OASL1, peut en réalité rendre ce virus plus dangereux en atténuant les premières défenses antivirales. En supprimant ce frein chez la souris, les auteurs montrent qu’il est possible d’améliorer drastiquement la survie, de réduire les lésions cérébrales et d’abaisser les charges virales, donnant des pistes pour de meilleurs traitements et vaccins contre le virus de la pseudoyeux et les herpèsvirus apparentés.
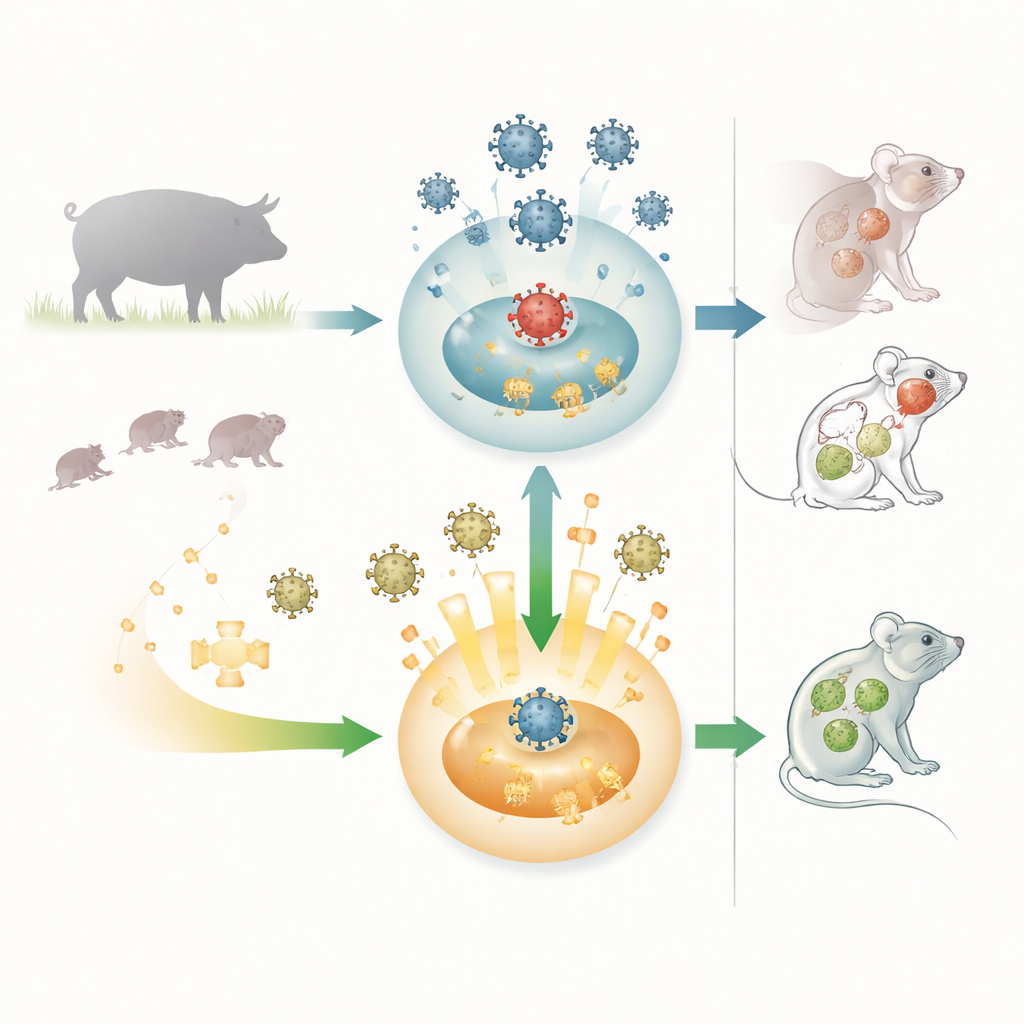
Un virus coriace et très diffus
Le virus de la pseudoyeux est un herpèsvirus dont l’hôte naturel est le porc, où il peut provoquer des troubles respiratoires, des échecs de reproduction et la quasi‑certitude de la mort chez les porcelets nouveau‑nés. Le virus peut aussi infecter de nombreux autres mammifères, animaux d’élevage, animaux de compagnie et souris de laboratoire, et presque tous ces hôtes accidentels meurent. Des signalements récents d’infections cérébrales humaines liées à des variants du virus ont suscité des inquiétudes quant à des franchissements occasionnels chez l’homme. En raison de cette large gamme d’hôtes et de la gravité des maladies, les chercheurs cherchent à comprendre comment la première ligne de défense de l’organisme, le système immunitaire inné, combat ce virus — et comment le virus riposte.
Le système d’alarme de l’organisme et un frein intégré
Quand un virus à ADN comme le virus de la pseudoyeux pénètre dans les cellules, des détecteurs spécialisés reconnaissent le matériel génétique viral et déclenchent la production d’interférons de type I, une famille de puissantes molécules d’alarme antivirale. Ces interférons activent des centaines de gènes de défense. Parmi eux se trouve OASL1, une protéine qui ne détruit pas directement les virus mais qui module la réponse. Des travaux antérieurs ont montré qu’OASL1 peut freiner la production d’IRF7, un élément clé du contrôle de la production d’interférons, formant une boucle de rétro‑contrôle négative qui empêche le système d’alarme de rester activé trop longtemps. La question centrale de cette étude était de savoir ce qui se passe lors d’une infection par la pseudoyeux si ce frein, OASL1, est supprimé.
Supprimer le frein protège les souris
Les chercheurs ont comparé des souris normales à des souris génétiquement modifiées pour être dépourvues d’OASL1. Les deux groupes ont reçu une dose de virus de la pseudoyeux habituellement létale. Toutes les souris normales ont développé des démangeaisons intenses, des lésions cutanées, des convulsions et une paralysie, et toutes sont mortes. Par contraste frappant, la plupart des souris déficientes en OASL1 ont survécu et conservé leur poids corporel avec des symptômes beaucoup plus légers. Lorsque l’équipe a mesuré les niveaux viraux dans la rate, les poumons et le cerveau, elle a constaté que les souris sans OASL1 avaient des charges virales beaucoup plus faibles. Les analyses sanguines ont montré que ces souris produisaient des quantités plus élevées d’interférons de type I tôt pendant l’infection, suggérant qu’une alarme plus forte et plus rapide a aidé à contrôler le virus avant qu’il ne puisse se propager largement.
Moins d’inflammation incontrôlée, moins de lésions d’organes
Les infections virales sévères peuvent déclencher une « tempête de cytokines », une réaction inflammatoire écrasante qui endommage les organes. Les scientifiques ont mesuré plusieurs molécules inflammatoires clés dans les tissus et le sang. Les souris normales infectées par le virus de la pseudoyeux présentaient des niveaux élevés de ces facteurs dans la rate, les poumons et le cerveau, accompagnés d’une importante infiltration de cellules inflammatoires. En revanche, les souris déficientes en OASL1 avaient des niveaux beaucoup plus faibles de ces signaux inflammatoires. Au microscope, leurs rates gardaient leurs cellules immunitaires au lieu de les perdre par mort cellulaire, leurs poumons présentaient des modifications inflammatoires plus légères et leurs cerveaux montraient beaucoup moins de dégénérescence des neurones dans l’hippocampe, une région critique pour la mémoire. Ainsi, la suppression d’OASL1 a non seulement aidé à éliminer le virus mais aussi prévenu une inflammation excessive et des lésions tissulaires.
Examen du commutateur de contrôle clé
Pour comprendre comment OASL1 façonne cette réponse, l’équipe a étudié IRF7, le commutateur de contrôle qui déclenche la production d’interférons. Chez les souris dépourvues d’OASL1, les niveaux d’IRF7 étaient systématiquement plus élevés dans la rate, les poumons, le cerveau et dans des cellules immunitaires en culture comme les macrophages et les microglies après infection, tandis qu’un facteur apparenté, IRF3, variait peu. Ces cellules sécrétaient davantage d’interférons de type I et supportaient moins de réplication virale. Lorsque les chercheurs ont utilisé de petits ARN interférents pour réduire spécifiquement IRF7 dans des macrophages déficients en OASL1, la réponse amplifiée en interférons a disparu et les niveaux viraux ont rebondi. Cette expérience a montré que l’effet protecteur de la perte d’OASL1 dépend principalement de la libération d’IRF7, permettant l’activation complète du programme antiviral.
Ce que cela implique pour l’avenir
En termes simples, OASL1 agit comme un frein de sécurité interne qui empêche l’alarme antivirale de sonner trop longtemps. Lors d’une infection par le virus de la pseudoyeux, ce frein se met en place trop tôt et trop fortement, laissant au virus la possibilité de se multiplier et contribuant à la gravité de la maladie. Les souris qui n’ont pas OASL1, ou dont OASL1 est temporairement silencé dans des cellules immunitaires clés, déclenchent une réponse rapide en interférons, pilotée par IRF7, qui élimine le virus plus efficacement tout en évitant une tempête de cytokines dommageable. Ces résultats suggèrent que des médicaments administrés de façon soigneusement chronométrée pour desserrer ce frein — uniquement durant la fenêtre critique de l’infection — pourraient aider à protéger les porcs et peut‑être les humains contre la pseudoyeux et les herpèsvirus apparentés. Toutefois, toute telle thérapie devrait être finement ajustée pour ne pas basculer d’une réponse immunitaire insuffisante à une réponse excessive.
Citation: Bao, T.H.T.N., Leya, M., Van, T.P. et al. 2’-5’ Oligoadenylate Synthetase-Like 1- (OASL1-) deficient mice promote antiviral protection against pseudorabies virus infection associated with enhanced production of type I interferon. Sci Rep 16, 13205 (2026). https://doi.org/10.1038/s41598-026-43144-0
Mots-clés: virus de la pseudoyeux, immunité innée, interféron de type I, OASL1, IRF7