Clear Sky Science · pl
Brak 2’-5’ oligoadenylanowego syntetazy-podobnego 1 (OASL1) u myszy sprzyja ochronie przeciwwirusowej przed zakażeniem wirusem pseudoprzeszczepu związanej z nasilonym wytwarzaniem interferonu typu I
Dlaczego to ma znaczenie dla ludzi i zwierząt
Wirus pseudoprzeszczepu może brzmieć jak ciekawostka ze świata gospodarstw, ale jest główną przyczyną śmierci prosiąt, zagrożeniem dla światowego przemysłu wieprzowego i okazjonalną przyczyną ciężkich zakażeń mózgu u ludzi. Badanie to ujawnia, w jaki sposób jeden z wewnętrznych „hamulców” organizmu, białko zwane OASL1, może w rzeczywistości zwiększać zagrożenie przez osłabianie wczesnych mechanizmów przeciwwirusowych. Usunięcie tego hamulca u myszy pozwoliło autorom znacznie poprawić przeżywalność, zmniejszyć uszkodzenie mózgu i obniżyć poziom wirusa, co daję wskazówki do lepszych terapii i szczepionek przeciwko wirusowi pseudoprzeszczepu i spokrewnionym herpeswirusom.
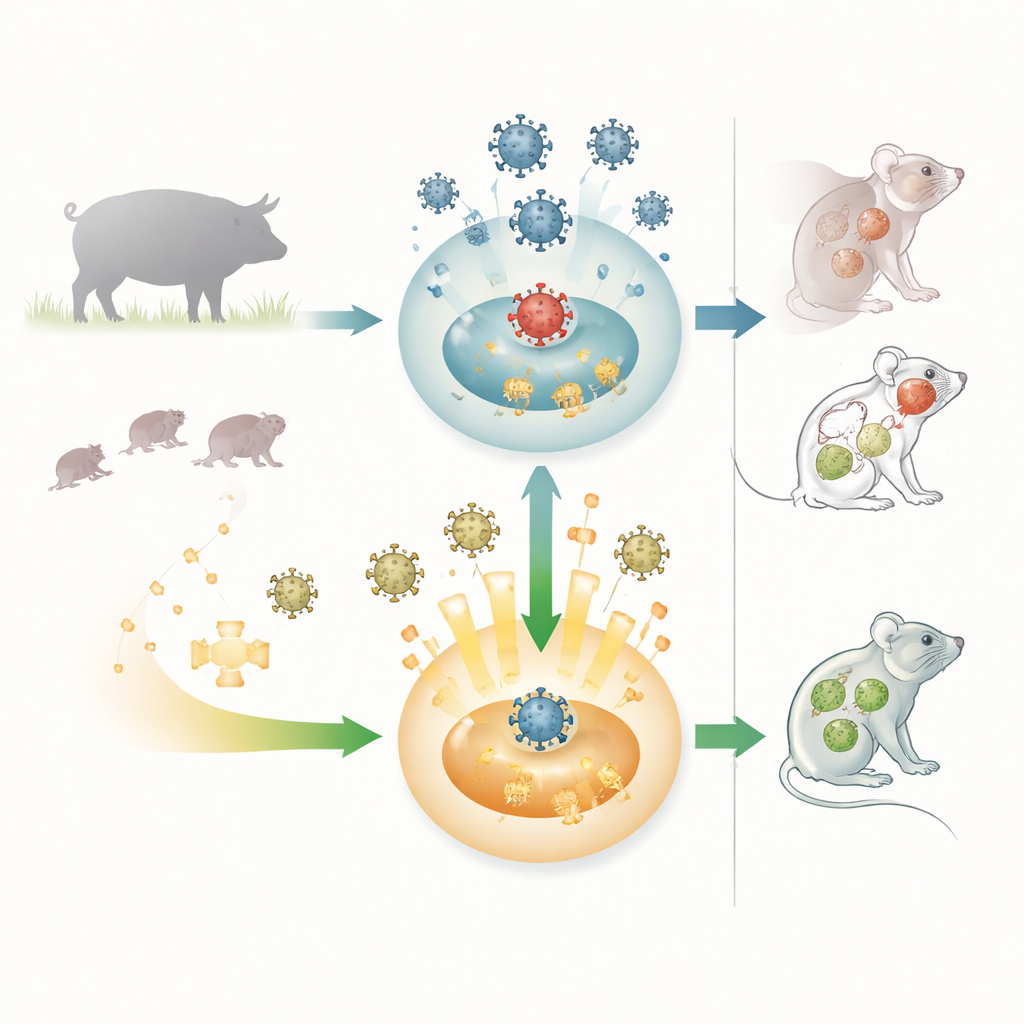
Trudny wirus o szerokim zasięgu
Wirus pseudoprzeszczepu to herpeswirus, którego naturalnym gospodarzem są świnie, gdzie może powodować problemy z oddychaniem, zaburzenia rozrodu i niemal pewną śmierć noworodków. Wirus może także zakażać wiele innych ssaków, w tym zwierzęta gospodarskie, zwierzęta domowe i myszy laboratoryjne, a niemal wszystkie te przypadkowe gospodarze giną. Ostatnie doniesienia o ludzkich zakażeniach mózgu powiązanych z wariantami wirusa pseudoprzeszczepu wzbudziły obawy, że patogen zwierzęcy może od czasu do czasu przenosić się na ludzi. Ze względu na szeroki zakres gospodarzy i ciężki przebieg choroby, badacze chcą zrozumieć, jak pierwsza linia obrony organizmu — system odporności wrodzonej — zwalcza ten wirus i jak wirus się przed tym broni.
System alarmowy organizmu i wbudowany hamulec
Gdy wirus DNA, taki jak wirus pseudoprzeszczepu, wnika do komórek, wyspecjalizowane czujniki wykrywają materiał genetyczny wirusa i uruchamiają produkcję interferonów typu I, rodziny silnych cząsteczek alarmowych o działaniu przeciwwirusowym. Interferony aktywują setki genów obronnych. Wśród nich jest OASL1, białko, które nie niszczy wirusów bezpośrednio, lecz precyzuje odpowiedź układu odpornościowego. Wcześniejsze badania wykazały, że OASL1 może hamować produkcję IRF7, kluczowego przełącznika kontrolującego wytwarzanie interferonu, tworząc pętlę ujemnego sprzężenia zwrotnego, która zapobiega nadmiernemu utrzymywaniu się alarmu. Głównym pytaniem tego badania było, co się dzieje podczas zakażenia wirusem pseudoprzeszczepu, gdy ten hamulec, OASL1, zostanie usunięty.
Usunięcie hamulca chroni myszy
Naukowcy porównali myszy normalne z myszami genetycznie zmodyfikowanymi, pozbawionymi OASL1. Obie grupy otrzymały dawkę wirusa pseudoprzeszczepu, która zwykle jest śmiertelna. Wszystkie myszy kontrolne rozwinęły silny świąd, rany skórne, drgawki i paraliż, a wszystkie padły. W uderzającym kontraście większość myszy pozbawionych OASL1 przeżyła i utrzymała masę ciała, wykazując znacznie łagodniejsze objawy. Kiedy zespół zmierzył poziomy wirusa w śledzionie, płucach i mózgu, stwierdzono, że myszy bez OASL1 miały znacznie niższe obciążenie wirusowe. Badania krwi wykazały, że te myszy produkowały większe ilości interferonów typu I we wczesnym okresie zakażenia, co sugeruje, że silniejsza, szybsza odpowiedź alarmowa pomogła opanować wirusa zanim zdążył się szeroko rozprzestrzenić.
Mniej wymykającego się spod kontroli zapalenia, mniej uszkodzeń narządów
Poważne zakażenia wirusowe mogą wywołać „burzę cytokin”, przytłaczającą reakcję zapalną, która uszkadza narządy. Naukowcy zmierzyli kilka kluczowych cząsteczek zapalnych w tkankach i krwi. Zainfekowane myszy kontrolne wykazywały wysokie poziomy tych czynników w śledzionie, płucach i mózgu, wraz z dużym napływem komórek zapalnych. W przeciwieństwie do tego, myszy pozbawione OASL1 miały znacznie niższe poziomy tych sygnałów zapalnych. Pod mikroskopem ich śledziony zachowały komórki odpornościowe zamiast tracić je na skutek śmierci komórkowej, w płucach odnotowano łagodniejsze zmiany zapalne, a w mózgach znacznie mniej degeneracji neuronów w hipokampie, regionie kluczowym dla pamięci. Zatem usunięcie OASL1 nie tylko pomogło oczyścić organizm z wirusa, lecz także zapobiegło nadmiernemu zapaleniu i uszkodzeniom tkanek.
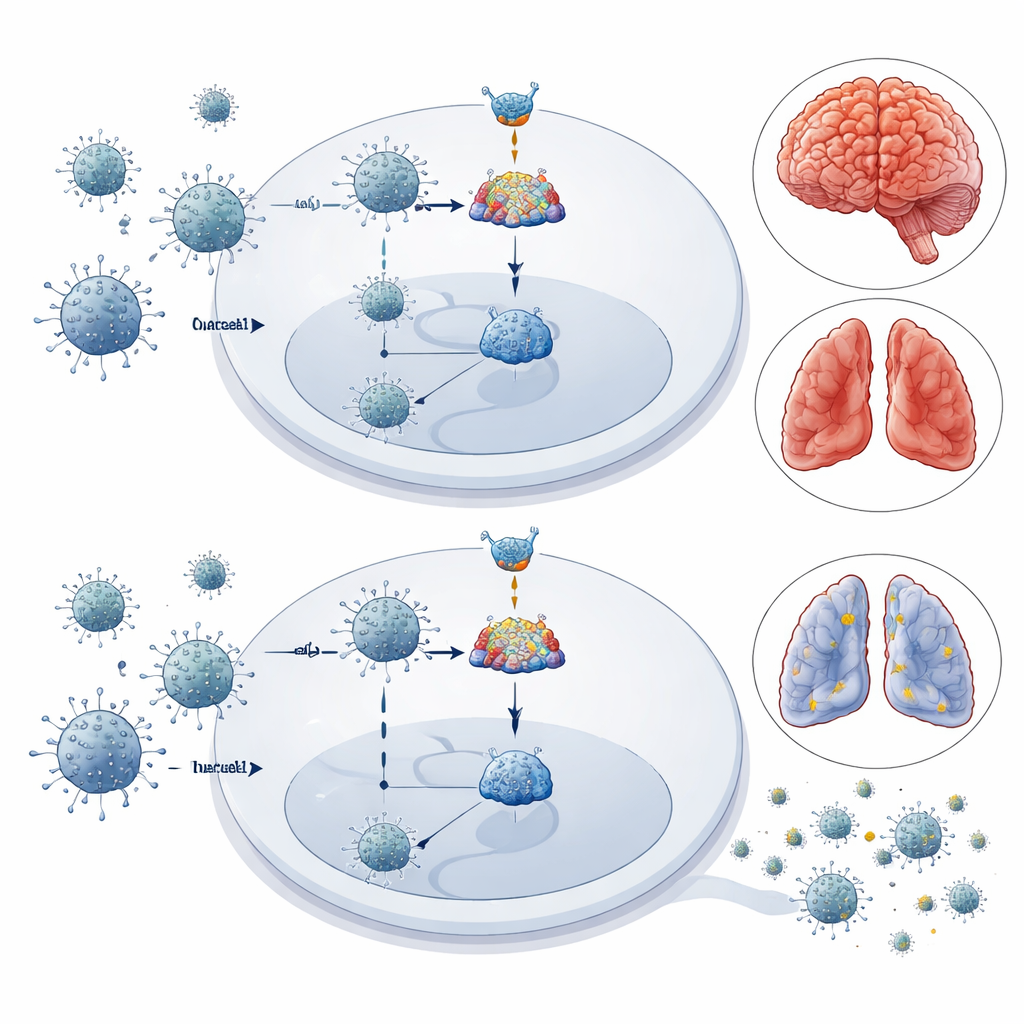
Przybliżenie kluczowego przełącznika
Aby zrozumieć, jak OASL1 kształtuje tę odpowiedź, zespół zbadał IRF7, przełącznik kontrolny napędzający produkcję interferonu. U myszy pozbawionych OASL1 poziomy IRF7 były konsekwentnie wyższe w śledzionie, płucach, mózgu oraz w hodowlach komórek odpornościowych, takich jak makrofagi i mikroglej, po zakażeniu, podczas gdy powiązany czynnik IRF3 zmieniał się niewiele. Te komórki wydzielały więcej interferonów typu I i wspierały mniejszą replikację wirusa. Gdy badacze zastosowali małe interferujące RNA, aby specyficznie stłumić IRF7 w makrofagach pozbawionych OASL1, wzmocniona odpowiedź interferonowa zniknęła, a poziomy wirusa ponownie wzrosły. To doświadczenie wykazało, że ochronny efekt utraty OASL1 zależy głównie od uwolnienia IRF7, aby w pełni aktywował program przeciwwirusowy.
Co to oznacza na przyszłość
Mówiąc obrazowo, OASL1 działa jak wewnętrzny hamulec bezpieczeństwa, który powstrzymuje alarm przeciwwirusowy przed zbyt długim wyciekiem. Podczas zakażenia wirusem pseudoprzeszczepu ten hamulec uruchamia się zbyt wcześnie i zbyt silnie, dając wirusowi pole do namnażania się i przyczyniając się do ciężkiego przebiegu choroby. Myszy pozbawione OASL1, lub u których OASL1 zostało tymczasowo wyciszone w kluczowych komórkach odpornościowych, uruchamiają szybką, napędzaną przez IRF7 odpowiedź interferonową, która skuteczniej eliminuje wirusa, jednocześnie unikając niszczącej burzy cytokin. Wyniki te sugerują, że ostrożnie dobrane leki poluzowujące ten hamulec — jedynie w krytycznym wczesnym oknie zakażenia — mogłyby pomóc chronić świnie, a być może i ludzi, przed wirusem pseudoprzeszczepu i pokrewnymi herpeswirusami. Każda taka terapia musiałaby być jednak starannie dostrojona, aby uniknąć przejścia od zbyt słabej odpowiedzi immunologicznej do zbyt silnej.
Cytowanie: Bao, T.H.T.N., Leya, M., Van, T.P. et al. 2’-5’ Oligoadenylate Synthetase-Like 1- (OASL1-) deficient mice promote antiviral protection against pseudorabies virus infection associated with enhanced production of type I interferon. Sci Rep 16, 13205 (2026). https://doi.org/10.1038/s41598-026-43144-0
Słowa kluczowe: wirus pseudoprzeszczepu, odporność wrodzona, interferon typu I, OASL1, IRF7